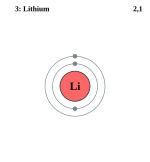
लिथियम
| लिथियम / Lithium रासायनिक तत्व | |
 | |
| रासायनिक चिन्ह: | Li |
| परमाणु संख्या: | 3 |
| रासायनिक शृंखला: | क्षार धातु |
 आवर्त सारणी में स्थिति
| |
 | |
| अन्य भाषाओं में नाम: | Lithium (अंग्रेज़ी), Литий (रूसी), リチウム (जापानी) |
लिथियम एक रासायनिक तत्व है। साधारण परिस्थितियों में यह प्रकृति की सबसे हल्की धातु और सबसे कम घनत्व-वाला ठोस पदार्थ है। रासायनिक दृष्टि से यह क्षार धातु समूह का सदस्य है और अन्य क्षार धातुओं की तरह अत्यंत अभिक्रियाशील (रियेक्टिव) है, यानि अन्य पदार्थों के साथ तेज़ी से रासायनिक अभिक्रिया कर लेता है। यदी इसे हवा में रखा जाये तो यह जल्दी ही वायु में मौजूद ऑक्सीजन से अभिक्रिया करने लगता है, जो इसके शीघ्र ही आग पकड़ लेने में प्रकट होता है। इस कारणवश इसे तेल में डुबो कर रखा जाता है। तेल से निकालकर इसे काटे जाने पर यह चमकीला होता है लेकिन जल्द ही पहले भूरा-सा बनकर चमक खो देता है और फिर काला होने लगता है। अपनी इस अधिक अभिक्रियाशीलता की वजह से यह प्रकृति में शुद्ध रूप में कभी नहीं मिलता बल्कि केवल अन्य तत्वों के साथ यौगिकों में ही पाया जाता है।[1] अपने कम घनत्व के कारण लिथियम बहुत हलका होता है और धातु होने के बावजूद इसे आसानी से चाकू से काटा जा सकता है। [2]
चित्र
[संपादित करें]-
तेल में लिथियम
-
लिथियम की गोलियाँ
-
पेटालाइट, लिथियम का एक खनिज
-
लिथियम क्लोराइड
-
लिथियम कार्बोनेट
इन्हें भी देखें
[संपादित करें]सन्दर्भ
[संपादित करें]- ↑ Krebs, Robert E. (2006). The History and Use of Our Earth's Chemical Elements: A Reference Guide. Westport, Conn.: Greenwood Press. ISBN 0-313-33438-2.
- ↑ Lide, D. R., ed. (2005). CRC Handbook of Chemistry and Physics (86th ed.). Boca Raton (FL): CRC Press. ISBN 0-8493-0486-5.





