सोना
| सोना / Gold रासायनिक तत्व | |
 | |
| रासायनिक चिन्ह: | Au |
| परमाणु संख्या: | 79 |
| रासायनिक शृंखला: | संक्रमण धातु |
 आवर्त सारणी में स्थिति
| |
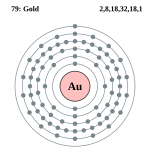 | |
| अन्य भाषाओं में नाम: | Gold (अंग्रेज़ी) |

सोना या स्वर्ण (Gold) अत्यंत चमकदार मूल्यवान धातु है। यह आवर्त सारणी के प्रथम अंतर्ववर्ती समूह (transition group) में ताम्र तथा रजत के साथ स्थित है। इसका केवल एक स्थिर समस्थानिक (isotope, द्रव्यमान 197) प्राप्त है। कृत्रिम साधनों द्वारा प्राप्त रेडियोधर्मी समस्थानिकों का द्रव्यमान क्रमश: 192, 193, 194, 195, 196, 198 तथा 199 है।
Introduction[संपादित करें]
'सोना एक धातु एवं तत्व है। शुद्ध सोना चमकदार पीले रंग का होता है जो कि बहुत ही आकर्षक रंग है। यह धातु बहुत कीमती है और प्राचीन काल से सिक्के बनाने, आभूषण बनाने एवं धन के संग्रह के लिये प्रयोग की जाती रही है। सोना घना, मुलायम, चमकदार, सर्वाधिक संपीड्य (malleable) एवं तन्य (ductile) धातु है। रासायनिक रूप से यह एक तत्व है जिसका प्रतीक (symbol) Au एवं परमाणु क्रमांक ७९ है। यह एक अंतर्ववर्ती धातु है। अधिकांश रसायन इससे कोई क्रिया नहीं करते। सोने के आधुनिक औद्योगिक अनुप्रयोग हैं - दन्त-चिकित्सा में, एलेक्ट्रॉनिकी में।
स्वर्ण के तेज से मनुष्य अत्यंत पुरातन काल से प्रभावित हुआ है क्योंकि बहुधा यह प्रकृति में मुक्त अवस्था में मिलता है। प्राचीन सभ्यताकाल में भी इस धातु को सम्मान प्राप्त था। ईसा से 2500 वर्ष पूर्व सिंधु घाटी की सभ्यताकाल में (जिसके भग्नावशेष मोहनजोदड़ो और हड़प्पा में मिले हैं) स्वर्ण का उपयोग आभूषणों के लिए हुआ करता था। उस समय दक्षिण भारत के मैसूर प्रदेश से यह धातु प्राप्त होती थी। चरकसंहिता में (ईसा से 300 वर्ष पूर्व) स्वर्ण तथा उसके भस्म का औषधि के रूप में वर्णन आया है। कौटिल्य के अर्थशास्त्र में स्वर्ण की खान की पहचान करने के उपाय धातुकर्म, विविध स्थानों से प्राप्त धातु और उसके शोधन के उपाय, स्वर्ण की कसौटी पर परीक्षा तथा स्वर्णशाला में उसके तीन प्रकार के उपयोगों (क्षेपण, गुण और क्षुद्रक) का वर्णन आया है। इन सब वर्णनों से यह ज्ञात होता है कि उस समय भारत में सुवर्णकला का स्तर उच्च था।
इसके अतिरिक्त मिस्र की सभ्यता के इतिहास में भी स्वर्ण के विविध प्रकार के आभूषण बनाए जाने की बात कही गई है और इस कला का उस समय अच्छा ज्ञान था।
मध्ययुग के कीमियागरों का लक्ष्य निम्न धातु (लोहे, ताम्र, आदि) को स्वर्ण में परिवर्तन करना था। वे ऐसे पत्थर पारस की खोज करते रहे जिसके द्वारा निम्न धातुओं से स्वर्ण प्राप्त हो जाए। इस काल में लोगों को रासायनिक क्रिया की वास्तविक प्रकृति का ज्ञान न था। अनेक लोगों ने दावे किये कि उन्होंने ऐसे गुर का ज्ञान पा लिया है जिसके द्वारा वे लौह से स्वर्ण बना सकते हैं जो बाद में सदैव मिथ्या सिद्ध हुए।
उपस्थिति[संपादित करें]
स्वर्ण प्राय: मुक्त अवस्था में पाया जाता है। यह उत्तम (noble) गुण का तत्व है जिसके कारण से उसके यौगिक प्राय: अस्थायी ही होते हैं। आग्नेय (igneous) चट्टानों में यह बहुत सूक्ष्म मात्रा में वितरित रहता है परंतु समय के साथ क्वार्ट्ज नलिकाओं (quartz veins) में इसकी मात्रा में वृद्धि हो गई है। प्राकृतिक क्रियाओं के फलस्वरूप कुछ खनिज पदार्थों में जैसे लौह पायराइट (Fe S2), सीस सल्फाइड (Pb S), चेलकोलाइट (Cu2 S) आदि अयस्कों के साथ स्वर्ण भी कुछ मात्रा में जमा हो गया है। यद्यपि इसकी मात्रा न्यून ही रहती है परंतु इन धातुओं का शोधन करते समय स्वर्ण की समुचित मात्रा मिल जाती है। चट्टानों पर जल के प्रभाव द्वारा स्वर्ण के सूक्ष्म मात्रा में पथरीले तथा रेतीले स्थानों में जमा होने के कारण पहाड़ी जलस्रोतों में कभी कभी इसके कण मिलते हैं। केवल टेल्डूराइल के रूप में ही इसके यौगिक मिलते हैं।
भारत में विश्व का लगभग दो प्रतिशत स्वर्ण प्राप्त होता है। मैसूर की कोलार की खानों से यह सोना निकाला जाता है। कोलार में स्वर्ण की 5 खानें हैं। इन खानों से स्वर्ण पारद के साथ पारदन (amalgamation) तथा सायनाइड विधि द्वारा निकाला जाता है। उत्तर में सिक्किम प्रदेश में भी स्वर्ण अन्य अयस्कों के साथ मिश्रित अवस्था में मिला करता है। बिहार के मानसून और सिंहभूम जिले में सुवर्णरेखा नदी में भी स्वर्ण के कण प्राप्य हैं।
दक्षिण अमरीका के कोलंबिया प्रदेश, मेक्सिको, संयुक्त राष्ट्र अमरीका के केलीफोर्निया तथा अलासका प्रदेश, आस्ट्रेलिया तथा दक्षिण अफ्रीका स्वर्ण उत्पादन के मुख्य केंद्र हैं। ऐसा अनुमान है कि यदि पंद्रहवीं शताब्दी के अंत से आज तक उत्पादित स्वर्ण को सजाकर रखा जाए तो लगभग 20 मीटर लंबा, चौड़ा तथा ऊँचा धन बनेगा। आश्चर्य तो यह है कि इतनी छोटी मात्रा के पदार्थ द्वारा करोड़ों मनुष्यों के भाग्य का नियंत्रण होता रहा है।
निर्माणविधि[संपादित करें]
स्वर्ण निकालने की पुरानी विधि में चट्टानों की रेतीली भूमि को छिछले तवों पर धोया जाता था। स्वर्ण का उच्च घनत्व होने के कारण वह नीचे बैठ जाता था और हल्की रेत धोवन के साथ बाहर चली जाती थी। हाइड्रालिक विधि (hydraulic mining) में जल की तीव्र धारा को स्वर्णयुक्त चट्टानों द्वारा प्रविष्ट करते हैं जिससे स्वर्ण से मिश्रित रेत जमा हो जाती है।
आधुनिक विधि द्वारा स्वर्णयुक्त क्वार्ट्ज (quartz) को चूर्ण कर पारद की परतदार ताम्र की थालियों पर धोते हैं जिससे अधिकांश स्वर्ण थालियों पर जम जाता है। परत को खुरचकर उसके आसवन (distillation) द्वारा स्वर्ण को पारद से अलग कर सकते हैं। प्राप्त स्वर्ण में अपद्रव्य वर्तमान रहता है। इसपर सोडियम सायनाइड के विलयन द्वारा क्रिया करने से सोडियम ऑरोसायनाइड बनेगा।
4 Au + 8 NaCN + O2 + 2 H2 O = 4 Na [ Au (C N)2] + 4 NaOH
इस क्रिया में वायुमंडल की ऑक्सीजन आक्सीकारक के रूप में प्रयुक्त होती है।
सोडियम ऑरोसायनाइड विलयन के विद्युत् अपघटन द्वारा अथवा यशद धातु की क्रिया से स्वर्ण मुक्त हो जाता है।
Zn + 2 Na [Au (C N)2] = Na2 [ Zn (CN)4] + 2 Au
सायनाइट विधि द्वारा ऐसे अयस्कों से स्वर्ण निकाला जा सकता है जिनमें स्वर्ण की मात्रा न्यूनतम हो। अन्य विधि के अनुसार अयस्क में उपस्थित स्वर्ण को क्लोरीन द्वारा गोल्ड क्लोराइड (Au Cl3) में परिणत कर जल में विलयित कर लिया जाता है। विलयन में हाइड्रोजन सल्फाइड (H2 S) प्रवाहित करने पर गोल्ड सल्फाइड बन जाता है जिसके दहन से स्वर्ण धातु मिल जाती है।
ऊपर बताई क्रियाओं से प्राप्त स्वर्ण में अपद्रव्य उपस्थित रहते हैं। इसके शोधन की आधुनिक विधि विद्युत् अपघटन पर आधारित है। इस विधि में गोल्ड क्लोराइड को तनु (dilute) हाइड्रोक्लोरिक अम्ल में विलयित कर लेते हैं। विलयन में अशुद्ध स्वर्ण के धनाग्र और शुद्ध स्वर्ण के ऋणाग्र के बीच विद्युत् प्रवाह करने पर अशुद्ध स्वर्ण विलयित हो ऋणाग्र पर जम जाता है।
गुणधर्म[संपादित करें]
स्वर्ण पीले रंग की धातु है। अन्य धातुओं के मिश्रण से इसके रंग में अंतर आ जाता है। इसमें रजत का मिश्रण करने से इसका रंग हल्का पड़ जाता है। ताम्र के मिश्रण से पीला रंग गहरा पड़ जाता है। मिनी गोल्ड में 8.33 प्रतिशत ताम्र रहता है। यह शुद्ध स्वर्ण से अधिक लालिमा लिए रहता है। प्लैटिनम या पेलैडियम के सम्मिश्रण से स्वर्ण में श्वेत छटा आ जाती है।
स्वर्ण अत्यंत कोमल धातु है। स्वच्छ अवस्था में यह सबसे अधिक धातवर्ध्य (malleable) और तन्य (ductile) धातु है। इसे पीटने पर 10-5 मिमी पतले वरक बनाए जा सकते हैं।
स्वर्ण के कुछ विशेष स्थिरांक निम्नांकित हैं :
संकेत (Au),
परमाणुसंख्या 79,
परमाणुभार 196.97,
गलनांक 1063° से.,
क्वथनांक 2970° से.
घनत्व 19.3 ग्राम प्रति घन सेमी,
परमाणु व्यास 2.9 एंग्स्ट्राम A°,
आयनीकरण विभव 9.2 इवों,
विद्युत प्रतिरोधकता 2.19 माइक्रोओहम् - सेमी.
स्वर्ण वायुमंडल ऑक्सीजन द्वारा प्रभावित नहीं होता है। विद्युत्वाहक-बल-शृंखला (electromotive series) में स्वर्ण का सबसे नीचा स्थान है। इसके यौगिक का स्वर्ण आयन सरलता से इलेक्ट्रान ग्रहण कर धातु में परिवर्तित हो जाएगा। स्वर्ण दो संयोजकता के यौगिक बनाता है, 1 और 3। 1 संयोजकता के यौगिकों को ऑरस (aurous) और 3 के यौगिकों को ऑरिक (auric) कहते हैं।
स्वर्ण नाइट्रिक, सल्फ्यूरिक अथवा हाइड्रोक्लोरिक अम्ल से नहीं प्रभावित होता परंतु अम्लराज (aqua regia) (3 भाग सांद्र हाइड्रोक्लोरिक अम्ल तथा 1 भाग सांद्र नाइट्रिक अम्ल का सम्मिश्रण) में घुलकर क्लोरोऑरिक अम्ल (H Au Cl4) बनाता है। इसके अतिरिक्त गरम सेलीनिक अम्ल (selenic acid) क्षारीय सल्फाइड अथवा सोडियम थायोसल्फेट में विलेय है।
यौगिक[संपादित करें]
स्वर्ण के 1 और 3 संयोजी यौगिक प्राप्त हैं। इसके अतिरिक्त इसके अनेक जटिल यौगिक भी बनाए गए हैं जिनमें इसकी संख्या उपसहसंयोजकता (co ordination number) 2 या 4 रहती है।
स्वर्ण का हाइड्रोक्साइड ऑरस हाइड्रोक्साइड (Au O H), ऑरस क्लोराइड (Au Cl) पर तनु पोटैशियम हाइड्राक्साइड (dil KOH) की क्रिया द्वारा प्राप्त होता है। यह गहरे बैंगनी रंग का चूर्ण है जिसे कुछ रासायनिक जलयुक्त ऑक्साइड (Au2 O) कहते हैं। यह स्वर्ण तथा क्रियाक्साइड (Au2 O3) में परिणत हो सकता है। ऑरस हाइड्रोक्साइड में शिथिल क्षारीय गुण वर्तमान हैं। यदि ऑरिक क्लोराइड (Au Cl3) अथवा क्लोरोआरिक अम्ल (HAuCl4) पर क्षारीय हाइड्रोक्साइड की क्रिया की जाए तो ऑरिक हाइड्राक्साइड {Au (OH)3} बनता है जिसे गरम करने पर आराइल हाइड्राक्साइड Au O (O H) आरिक ऑक्साइड (Au2 O3) और (Au2 O2) और तत्पश्चात् स्वर्ण धातु बच रहती है।
हेलोजन तत्वों से स्वर्ण अनेक यौगिक बनाता है। रक्तताप पर स्वर्ण फ्लोरीन से संयुक्त हो गोल्ड फ्लोराइड बनाता है। क्लोरीन के साथ दो यौगिक ऑरस क्लोराड (Au Cl) और ऑरिक क्लोराइड (Au Cl3) ज्ञात हैं। ऑरस क्लोराइड जल द्वारा अपघटित हो स्वर्ण और ऑरिक क्लोराइड (Au Cl) बना है और अधिक उच्च ताप पर पूर्णतय: विघटित हो जाता है। ब्रोमीन के साथ ऑरस ब्रोमाइड (Au Br) और ऑरिक ब्रोमाइड (Au Br3) बनते हैं। इनके गुण क्लोराइड यौगिकों की भाँति हैं। आयोडीन के साथ भी स्वर्ण के दो यौगिक ऑरस आयोडाइड (Au I) और ऑरिक आयोडाइड (Au I3) बनते हैं परंतु वे दोनों अस्थायी होते हैं।
वायु की उपस्थिति में स्वर्ण क्षारीय सायनाइड में विलयित हो जटिल यौगिक ऑरोसाइनाइड [ Au (C N)2] बनता है जिसमें स्वर्ण 1 संयोजी अवस्था में है। त्रिसंयोजी अवस्था के जटिल यौगिक { K Au (C N)4} भी ज्ञात हैं।
ऑरिक ऑक्साइड पर सांद्र अमोनिया की क्रिया से एक काला चूर्ण बनता है जिसे फ्लीमिनेटिंग गोल्ड (2 Au N. N H3. 3 H2 O) कहते हैं। यह सूखी अवस्था में विस्फोटक होता है।
स्वर्ण के कालायडी विलयन (colloidal solution) का रंग कणों के आकार पर निर्भर है। बड़े कणों के विलयन का रंग नीला रहता है। कणों का आकार छोटा होने पर क्रमश: लाल तथा नारंगी हो जाता है। क्लोरोऑरिक अम्ल विलयन में स्टैनश क्लोराइड (Sn Cl2) मिश्रित करने पर एक नीललोहित अवक्षेप प्राप्त होता है। इसे कैसियम नीललोहित (purple of cassius) कहते हैं। यह स्वर्ण का बड़ा संवेदनशील परीक्षण (delicate test) माना जाता है।
उपयोग[संपादित करें]
दुनिया भर में नये उत्पादित सोने की खपत गहने में लगभग 50%, निवेश में 40%, और इस उद्योग में 10% है
स्वर्ण का मुद्रा तथा आभूषण के निमित्त प्राचीन काल से उपयोग होता रहा है। स्वर्ण अनेक धातुओं से मिश्रित हो मिश्रधातु बनाता है। मुद्रा में प्रयुक्त स्वर्ण में लगभग 90 प्रतिशत स्वर्ण रहता है। आभूषण के लिए प्रयुक्त स्वर्ण में भी न्यून मात्रा में अन्य धातुएँ मिलाई जाती हैं जिससे उसके भौतिक गुण सुधर जाएँ। स्वर्ण का उपयोग दंतकला तथा सजावटी अक्षर बनाने में हो रहा है।
स्वर्ण के यौगिक फोटोग्राफी कला में तथा कुछ रासायनिक क्रियाओं में भी प्रयुक्त हुए हैं।
स्वर्ण की शुद्धता डिग्री अथवा कैरट में मापी जाती है। विशुद्ध स्वर्ण 1000 डिग्री अथवा 24 कैरट होता है।--- (र. चं. क.)
सोने का उत्खनन[संपादित करें]
सोने का खनन भारत में अत्यंत प्राचीन समय से हो रहा है। कुछ विद्वानों का मत है कि दसवीं शताब्दी के पूर्व पर्याप्त मात्रा में खनन हुआ था। गत तीन शताब्दियों में अनेक भूवेत्ताओं ने भारत के स्वर्णयुक्त क्षेत्रों में कार्य किया किंतु अधिकांशत: वे आर्थिक स्तर पर सोना प्राप्त करने में असफल ही रहे। भारत में उत्पन्न लगभग संपूर्ण सोना मैसूर राज्य के कोलार तथा हट्टी स्वर्णक्षेत्रों से निकलता है। अत्यंत अल्प मात्रा में सोना उत्तर प्रदेश, बिहार, उड़ीसा, पंजाब तथा मद्रास राज्यों में भी अनेक नदियों की मिट्टी या रेत में पाया जाता है किंतु इसकी मात्रा साधारणत: इतनी कम है कि इसके आधार पर आधुनिक ढंग का कोई व्यवसाय आर्थिक दृष्टि से प्रारंभ नहीं किया जा सकता। इन क्षेत्रों में कुछ स्थानों पर स्थानीय निवासी अपने अवकाश के समय में इस मिट्टी एवम् रेत को धोकर कभी कभी अल्प सोने की प्राप्ति कर लेते हैं।
कोलार स्वर्णक्षेत्र (Kolar Gold Field){KGF}[संपादित करें]
यह क्षेत्र मैसूर राज्य के कोलार जिले में मद्रास के पश्चिम की ओर 125 मील की दूरी पर स्थित है। समुद्र से 2,800 फुट की ऊँचाई पर यह क्षेत्र एक उच्च स्थली पर है। वैसे तो इस क्षेत्र का विस्तार उत्तर-दक्षिण में 50 मील तक है किंतु उत्पादन योग्य पटिट्का (Vein) की लंबाई लगभग 4 मील ही है। इस क्षेत्र में बालाघाट, नंदी दुर्ग, उरगाम, चैंपियन रीफ (Champion Reef) तथा मैसूर खानें स्थित हैं। खनन के प्रारंभ से मार्च 1951 के अंत तक 2,18,42,902 आउंस स्वर्ण, जिसका मूल्य 169.61 करोड़ रुपया हुआ, प्राप्त हुआ। कोलार क्षेत्र में कुल 30 पट्टिकाएँ हैं जिनकी औसत चौड़ाई 3-4 फुट है। इन पट्टिकाओं में सर्वाधिक स्वर्ण उत्पादक पट्टिका 'चैंपियन रीफ' है। इसमें नीले भूरे वर्ण का, विशुद्ध तथा कणोंवाला स्फटिक प्राप्त होता है। इसी स्फटिक के साहचर्य में सोना भी मिलता है। सोने के साथ ही टुरमेलीन (Tourmaline) भी सहायक खनिज के रूप में प्राप्त होता है। साथ ही साथ पायरोटाइट (Pyrotite), पायराइट, चाल्कोपायराइट, इल्मेनाइट, मैग्नेटाइट तथा शीलाइट (Shilite) आदि भी इस क्षेत्र की शिलाओं में मिलते हैं।
स्वर्ण उद्योग[संपादित करें]
कोलार (मैसूर) की सोने की खानों में पूर्णत: आधुनिक एवं वैज्ञानिक विधियों से कार्य होता है। यहाँ की चार खानें 'मैसूर', 'नंदीद्रुग', 'उरगाम' और 'चैपियनरीफ' संसार की सर्वाधिक गहरी खानों में से है। इन खानों में से दो तो सतह से लगभग 10,000 फुट की गहराई तक पहुँच चुकी हैं। इन खानों में ताप 148° फारेनहाइड तक चला जाता है अत: शीतोत्पादक यंत्रों की सहायता से ताप 118° फारेनहाइट तक कम करने की व्यवस्था की गई है। सन् 1953 में उरगाम खान बंद कर दी गई है। औसत रूप से कोलार में प्रति टन खनिज में लगभग पौने तीन माशे सोना पाया जाता है। द्वितीय विश्वयुद्ध से पूर्व विपुल मात्रा में सोने का निर्यात किया जाता था। सन् 1939 में 3,14,515 आउंस सोने का उत्पादन हुआ जिसका मूल्य 3,24,34,364 रुपये हुआ किंतु इसके पश्चात् स्वर्ण उत्पादन में अनियमित रूप से कमी होती चली गई है तथा सन् 1947 में उत्पादन घटकर 1,71,795 आउंस रह गया जिसका मूल्य 5,10,69,000 रुपए तक पहुँचा। कोलार स्वर्णक्षेत्र की खानों का राष्ट्रीयकरण हो गया है तथा मैसूर की राज्य सरकार द्वारा संपूर्ण कार्य संचालित होता है। कोलार विश्व का एक अद्वितीय एवं आदर्श खनन नगर है। यहाँ स्वर्ण खानों के कर्मचारियों को लगभग सभी संभव सुविधाएँ प्रदान की गई हैं। खानों में भी आपातकालीन स्थिति का सामना करने के लिए विशेष सुरक्षा दल (Rescue Teams) रहते हैं।
हैदराबाद में हट्टी में भी सोना प्राप्त हुआ है। इसी प्रकार केरल में वायनाड नामक स्थान पर सोना मिला था किंतु ये निक्षेप कार्य योग्य नहीं थे।
सोना चढ़ाना (Gilding)[संपादित करें]
किसी पदार्थ की सतह पर उसकी सुरक्षा अथवा अलंकरण हेतु यांत्रिक तथा रासायनिक साधनों से सोना चढ़ाया जाता है। यह कला बहुत ही प्राचीन है। मिस्रवासी आदिकाल ही में लकड़ी और हर प्रकार के धातुओं पर सोना चढ़ाने में प्रवीण तथा अभ्यस्त रहे। पुराने टेस्टामेंट में भी गिल्डिंग का उल्लेख मिलता है। रोम तथा ग्रीस आदि देशों में प्राचीन काल से इस कला को पूर्ण प्रोत्साहन मिलता रहा है। प्राचीन काल में अधिक मोटाई की सोने की पत्तियाँ प्रयोग में लाई जाती थीं। अत: इस प्रकार की गिल्डिंग अधिक मजबूत तथा चमकीली होती रही। पूर्वी देशों की सजावट की कला में इसका प्रमुख स्थान है- मंदिरों के गुंबजों तथा राजमहलों की शोभा बढ़ाने के लिए यह कला विशेषत: अपनाई जाती है। भारत में आज भी जिस विधि से सोना चढ़ाया जाता है इसकी प्राचीनता का एक सुंदर उदाहरण है।
आधुनिक गिल्डिंग में तरह तरह की विधियाँ प्रयोग में लाई जाती हैं और इनसे हर प्रकार के सतहों पर सोना चढ़ाया जा सकता है, जैसे तस्वीरों के फ्रेम, अलमारियों, सजावटी चित्रण, घर और महलों की सजावट, किताबों की जिल्दबाजी, धातुओं के अवरण, बटन बनाना, गिल्ड टाव ट्रेड, प्रिंटिग तथा विद्युत् आवरण, मिट्टी के बर्तनों, पोर्सिलेन, काँच तथा काँच की चूड़ियों की सजावट। टेक्सटाइल, चमड़े और पार्चमेंट पर भी सोना चढ़ाया जाता है तथा इन प्रचलित कामों में सोना अधिक मात्रा में उपभुक्त होता है।
सोना चढ़ाने की समस्त विधियाँ यांत्रिक अथवा रासायनिक साधनों पर निर्भर हैं। यांत्रिक साधनों से सोने की बहुत ही बारीक पत्तियाँ बनाते हैं और उसे धातुओं या वस्तुओं की सतह से चिपका देते हैं। इसलिए धातुओं की सतह को भली भाँति खुरचकर साफ कर लेते हैं। और उसे अच्छी तरह पालिश कर देते हैं। फिर ग्रीज तथा दूसरे अपद्रव्यों (Impurities) जो पालिश करते समय रह जाती है, गरम करके हटा देते हैं। बहुधा लाल ताप पर धातुओं की सतह पर बर्निशर से सोने की पत्तियों को दबाकर चिपका देते हैं। इसे फिर गरम करते हैं और यदि आवश्यकता हुई तो और पत्तियाँ रखकर चिपका देते हैं, तत्पश्चात् इसे ठंडा करके बर्निशर से रगड़ कर चमकीला बना देते हैं। दूसरी विधि में पारे का प्रयोग किया जाता है। धातुओं की सतह की पूर्ववत् साफकर अम्ल विलयन में डाल देते हैं। फिर उसे सतह की पूर्ववत् साफकर अम्ल विलयन में डाल देते हैं। फिर उसे बाहर निकालकर सुखाने के बाद झॉवा तथा सुर्खी से रगड़ कर चिकनाहट पैदा कर देते हैं। इस क्रिया के उपरांत सतह पर पारे की एक पतली पर्त पारदन कर देते हैं, तब इसे कुछ समय के लिए पानी में डाल देते हैं और इस प्रकार यह सोना चढ़ाने योग्य बन जाता है। सोने की बारीक पत्तियाँ चिपकाने से ये पारे से मिल जाती हैं। गरम करने के फलस्वरूप पारा उड़ जाता है और सोना भूरेपन की अवस्था में रह जाता है, इसे अगेट वर्निशर से रगड़कर चमकीला बना देते हैं। इस विधि में सोने का प्राय: दुगुना पारा लगता है तथा पारे की पुन: प्राप्ति नहीं होती।
रासायनिक गिल्डिंग में वे विधियाँ शामिल हैं जिनमें प्रयुक्त सोना किसी न किसी अवस्था में रासायनिक यौगिक के रूप में रहता है।
सोना चढ़ाना - चाँदी पर प्राय: सोना चढ़ाने के लिए, सोने का अम्लराज में विलयन बना लेते हैं और कपड़े की सहायता से विलयन को धात्विक सतह पर फैला देते हैं। फिर इसे जला देते हैं और चाँदी से चिपकी काली तथा भारी भस्म को चमड़े तथा अंगुलियों से रगड़कर चमकीला बना लेते हैं। अन्य धातुओं पर सोना चढ़ाने के लिए पहले उसपर चाँदी चढ़ा लेते हैं।
गीली सोनाचढ़ाई - गोल्ड क्लोराइड के पतले विलयन को हाईड्रोक्लोरिक अम्ल की उपस्थिति में पृथक्कारी कीप की मदद से ईथरीय विलयन में प्राप्त कर लेते हैं तथा एक छोटे बुरुश से विलयन को धातुओं की साफ सतह पर फैला देते हैं। ईथर के उड़ जाने पर सोना रह जाता है और गरम करके पालिश करने पर चमकीला रूप धारण कर लेता है।
आग सोनाचढ़ाई (fire Gilding) - इसमें धातुओं के तैयार साफ और स्वच्छ सतह पर पारे की पतली सी परत फैला देते हैं और उसपर सोने का पारदन चढ़ा देते हैं। तत्पश्चात् पारे को गरम कर उड़ा देते हैं और सोने की एक पतली पटल बच जाती है, जिसे पालिश कर सुंदर बना देते हैं। इसमें पारे की अधिक क्षति होती है और काम करनेवालों के लिए पारे का धुआँ अधिक अस्वस्थ्यकर है।
काष्ठ सोनाचढ़ाई - लकड़ी की सतह पर चाक या जिप्सम का लेप चढ़ाकर चिकनाहट पैदा कर देते हैं। फिर पानी में तैरती हुई सोने की बारीक पत्तियों का स्थामी विरूपण कर देते हैं। सूख जाने पर इसे चिपका देते हैं तथा दबाकर समस्थितीकरण कर देते हैं। इसके उपरांत यह सोने की मोटी चद्दरों की तरह दिखाई देने लगती है। दाँतेदार गिल्डिंग से इसमें अधिक चमक आ जाती है।
मिट्टी के बरतनों, पोर्सिलेन तथा क्राँच पर सोना चढ़ाने की कला अधिक लोकप्रिय है। सोने के अम्लराज विलयन को गरम कर पाउडर अवस्था में प्राप्त कर लेते हैं और इसमें बारहवाँ भाग विस्मथ आक्साइड तथा थोड़ी मात्रा में बोराक्स और गन पाउडर मिला देते हैं इस मिश्रण को ऊँट के बालवाले बुरुश से वस्तु पर यथास्थान चढ़ा देते हैं। आग में तपाने पर काले मैले रंग का सोना चिपका रह जाता है, जो अगेट बर्निशर से पालिश कर चमकाया जाता है। और फिर ऐसीटिक अम्ल से इसे साफ कर लेते हैं।
लोहा या इस्पात पर सोना चढ़ाने के लिए सतह को साफ कर खरोचने के पश्चात् उसपर लाइन बना देते हैं। फिर लाल ताप तक गरम कर सोने की पत्तियाँ बिछा देते हैं और ढंडा करने के उपरांत इसको अगेट बर्निशर से रगड़कर पालिश कर देते हैं। इस प्रकार इसमें पूर्ण चमक आ जाती है और इसकी सुंदरता अनुपम हो जाती है।
धातुओं पर विद्युत् आवरण की कला को आजकल अधिक प्रोत्साहन मिल रहा है। एक छोटे से नाद में गोल्ड सायनाइड और सोडियम सायनाइड का विलयन डाल देते हैं तथा सोने का ऐनोड और जिसपर सोना चढ़ाना होता है, उसका कैथोड लटका देते हैं। फिर विद्युत्प्राह से सोने का आवरण कैथोड पर चढ़ जाता है। विद्युत्-आवरणीय सोने का रंग अन्य धातुओं के निक्षेपण पर निर्भर है। अच्छाई, टिकाऊपन, सुंदरता तथा सजावट के लिए निम्न कोटि की धातुओं पर पहले ताँबे का विद्युत् आवरण करके चाँदी चढ़ाते हैं। तत्पश्चात् सोना चढ़ाना उत्तम होता है। इस ढंग से सोने की बारीक से बारीक परत का आवरण चढ़ाया जा सकता है तथा जिस मोटाई का चाहें सोने का विद्युत्आवरण आवश्यकतानुसार चढ़ा सकते हैं। इससे धातुओं की संक्षरण से रक्षा होती है तथा हर प्रकार की वस्तुओं पर सोने की सुंदर चमक आ जाती है।
इन्हें भी देखें[संपादित करें]
- सायनाइड विधि - स्वर्ण निर्माण की धातुकार्मिक तकनीक
