थैलियम
| थैलियम / Thallium रासायनिक तत्व | |
 | |
| रासायनिक चिन्ह: | Tl |
| परमाणु संख्या: | 81 |
| रासायनिक शृंखला: | संक्रमणोपरांत धातु |
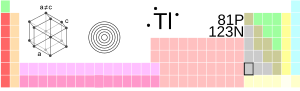 आवर्त सारणी में स्थिति
| |
 | |
| अन्य भाषाओं में नाम: | Thallium (अंग्रेज़ी) |
थैलियम (Thallium) एक रासायनिक तत्त्व है। यह आवर्त सारणी के तृतीय मुख्य समूह का अंतिम तत्व है। इसके दो स्थिर समस्थानिक प्राप्त हैं, जिनकी द्रव्यमान संख्याएँ २०३ एवं २०५ हैं। इसके अतिरिक्त इसके नौ अस्थिर समस्थानिक ज्ञात हैं। इनकी द्रव्यमान संख्याएँ १९९, २००, २०२, २०४, २०६, २०७, २०८, २०९ और २१० हैं। इनमें कुछ रेडियधर्मी अयस्कों में मिलते हैं और कुछ कृत्रिम साधनों द्वारा उपलब्ध हैं। इस तत्व की खोज अंग्रेज वैज्ञानिक विलियम क्रुक्स ने १८६१ ईo में एक विशेष सेलेनियम युक्त पायराइट (seleniferous pyrite) में वर्णक्रममापी (spectroscopic) उपकरण द्वारा की। उन्होंने भूर्जित (roasted) अयस्क की धूल के वर्णक्रममापी निरीक्षण में एक हल्के हरे रंग की रेखा देखी, जिसके कारण इस तत्व का नाम थैलियम रखा। इस तत्व को लैमी (Lamy) ने सर्वप्रथम पृथक् कर इसके गुणधर्म का निरीक्षण किया।
अनेक पायराइट अयस्कों में थैलियम न्यून मात्रा में वर्तमान रहता है। केवल क्रुसाइट (Crookesite) नामक अयस्क में यह १७% मात्रा में उपस्थित रहता है। सामान्यत: यह कुछ अयस्कों की चिमनी (flue) धूल, या सल्फ्यूरिक अम्ल बनते समय प्रकोष्ठ कीच (chamber mud), से निकाला जाता है। कीच को उबलते जल से उपचारित करने पर थैलियम सल्फेट का विलयन बन जाता है, जिसे छानकर हाइड्रोक्लोरिक अम्ल द्वारा क्लोराइड में परिवर्तित करते हैं। क्लोराइड को फिर सल्फ्यूरिक अम्ल की क्रिया द्वारा सल्फेट में परिणत करने से अन्य अपद्रव्य दूर हो जाते हैं। उबलते जल की क्रिया से केवल थैलियम सल्फेट ही घुलता है। विलयन के विद्युद्विश्लेषण अथवा यशद धातु की प्रक्रिया द्वारा थैलियम धातु मिलती है।
गुणधर्म[संपादित करें]
थैलियम नीले श्वेत रंग की धातु है। यह अति नम्र और लोचरहित होती है। इसके भौतिक गुणधर्म निम्नलिखित हैं :
- संकेत -- Tl
- परमाणु संख्या -- ८१,
- परमाणु भार -- २०४.३७,
- गलनांक -- ३०० डिग्री सेंo,
- क्वथनांक -- १,४६० डिग्री सेंo,
- घनत्व -- ११,८५ ग्राम प्रति घo सेंमीo,
- परमाणु व्यास -- ३.४२ ऐंगस्ट्रॉम।
यह एकपरमाणुक (monoatomic) अवस्था में रहता है। वायु में रखने पर इसपर ऑक्साइड की परत जम जाती है। थैलियम वायु और जल के संयुक्त प्रभाव से थैलियम हाइड्रॉक्साइड (TlOH) में परिणत हो जाता है। उच्च ताप पर यह जल का विघटन कर हाइड्रोजन मुक्त करता है। वायु में गरम करने पर थैलियम शीघ्र ऑक्सीकृत हो लाल या बैंगनी वाष्प उत्पन्न करता है।
थैलियम नाइट्रिक अम्ल अथवा सल्फ्यूरिक अम्ल में शीघ्र, परंतु हाइड्रोक्लोरिक अम्ल में मंद गति से, घुलता है।
यौगिक[संपादित करें]
थैलियम दो प्रकार के लवण बनाता है : एक और तीन संयोजकता के। थैलस लवण एक संयोजकता के एवं थैलिक तीन संयोजकता के लवण हैं।
थैलस हाइड्रॉक्साइड (TlOH) में क्षारीय गुण वर्तमान है। यह पीले रंग के मणिभ बनाता है, जो जल में शीघ्र घुल जाते हैं। इसको गरम करने पर काले रंग का ऑक्साइड (TlO2) बनता है। इसके अतिरिक्त एक संयोजिकता वाले लवण थैलस क्लोराइड (TlCl), थैलस कार्बोनेट (Tl2CO3), थैलस सल्फेट (Tl2SO4), थैलस नाइट्रेट (TINO3) सरलता से बनाए जा सकते हैं।
थैलियम को उच्च ताप (५०० से ७०० डिग्री सेंo) पर वायु या ऑक्सीजन में रखने पर थैलिक ऑक्साइड (Tl2O3) बनता है। इस संयोजकता के कुछ विशेष यौगिक हैं : थैलिक क्लोराइड (TICI3), थैलिक आयोडाइड (Tl I2), थैलिक सल्फेट [ Tl2 (SO4) 7H2 O ] थैलिक नाइट्रेट [ Tl (NO3)3 3H2O ] आदि।
उपयोग[संपादित करें]
काँच में थैलियम के यौगिक मिलाने से उसका अपवर्तनांक बढ़ जाता है, जिस कारण यह कुछ विशेष उपयोगी काच बनाने में काम आता है। थैलियम के यौगिक कार्बनिक संश्लेषण में उपयोगी माने गए हैं। थैलियम लवण विषैले होते हैं।
