रासायनिक यौगिक
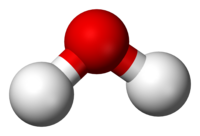
जब भिन्न तत्त्वों के दो या दो से अधिक परमाणु एक निश्चित अनुपात में संयोजित होते हैं, तब रासायनिक यौगिक का एक अणु प्राप्त होता है। किसी रासायनिक यौगिक के घटकों को भौतिक विधियों द्वारा सरल पदार्थों में पृथक नहीं किया जा सकता है। उन्हें पृथक करने हेतु रासायनिक विधियों का प्रयोग करना पड़ता है। जल, अमोनिया, कार्बन डाइऑक्साइड, शर्करा आदि यौगिकों के कुछ उदाहरण हैं।
प्रकार[संपादित करें]
कार्बनिक यौगिक[संपादित करें]
यह यौगिक कार्बन के द्वारा बना होता है । इसलिए कार्बन के यौगिक को कार्बनिक यौगिक के रूप में माना जाता है । ज्यादा से ज्यादा कार्बनिक यौगिक में हाइड्रोजन, ऑक्सीजन तथा इसके साथ- साथ विभिन्न प्रकार का तत्व पाया जाता है। कार्बन यौगिक हमेशा सहसंयोजक बंधन द्वारा बनता है।
कार्बनिक यौगिक को पिघलने या उबलने का समय बहुत ही कम रहता है, इसलिए इनका गलनांक एवं क्वथनांक कम ही रहता है । यदि कार्बनिक यौगिक की विद्युत चालकता के संबंध में कहा जाए तो कार्बनिक यौगिक ज्यादा से ज्यादा विद्युत के कुचालक होते हैं । यह यौगिक सभी प्रकार के जीवित प्राणियों में पाया जाता है तथा मृत्युपरांत इनका जैविक निम्नन एवं रसायनिक विघटन होने लगता है । इसलिए कृत्रिम विधि द्वारा इसे निकाला जा सकता है ।
अकार्बनिक यौगिक[संपादित करें]
इसे आमतौर पर रासायनिक यौगिक कहाँ जाता है । जिसमें कार्बन नहीं पाया जाता है । जिसके कारण कार्बन बॉन्ड का आभाव होता है ।
बुनियादी ऑक्साइड :- इसे बनने की प्रारम्भ, जब धातु ऑक्सीजन के साथ संयुक्त हो जाती है । यह सवभाविक एंव औधोगिक रूप से बन सकता है । हाइड्रोऑक्सीड को प्राप्त करने के लिए, पानी को ऑक्साइड से जोड़ा जाता है ।
एसिड ऑक्साइड एंव एनहाइड्रिड : गैर धात्विक तत्वों के साथ ऑक्सीजन को मिलने पर जो परिणाम प्राप्त होती है । वह एसिड ऑक्साइड के अंतर्गत आता है । जब हाइड्राइड बनाने की बात आती है । तो कुछ धात्विक तत्व के साथ हाइड्रोजन जोड़ा जाता है । जिसे जोड़ने के बाद हाइड्राइड प्राप्त होता है ।
एसिड: इसका अणु हाइड्रोजन से शुरू होता है । इसे भी निम्न प्रकार से विभाजन किया जा सकता है:-
हाइड्रोजन और अन्य प्रकार के धातु से बने हाइड्रैसिड्स, तथा ऑक्सीकाइड्स जो तैयार होता है । वह एक हाइड्राजाइड प्लस ऑक्सीजन होता है ।
आयनीय यौगिक[संपादित करें]
सहसंयोजक यौगिक[संपादित करें]
इन्हें भी देखें[संपादित करें]
- रासायनिक तत्व
- रासायनिक अभिक्रिया
- रासायनिक क्रांति
- रासायनिक आबन्ध
- अकार्बनिक यौगिकों की सूची
- रासायनिक सूत्र
- रासायनिक सूत्र कोश
- रासायनिक संरचना