"ऊष्माक्षेपी अभिक्रिया": अवतरणों में अंतर
Content deleted Content added
अनुनाद सिंह (वार्ता | योगदान) छो अनुनाद सिंह ने ऊष्माक्षेपी अभिक्रिया से पुनर्निर्देश हटाकर उष्माक्षेपी अभिक्रिया को उसपर ... |
Sanjeev bot (वार्ता | योगदान) छो सन्दर्भ की स्थिति ठीक की। |
||
| पंक्ति 7: | पंक्ति 7: | ||
:2H<sub>2</sub> (g) + O<sub>2</sub> (g) → 2H<sub>2</sub>O (g) |
:2H<sub>2</sub> (g) + O<sub>2</sub> (g) → 2H<sub>2</sub>O (g) |
||
:ΔH = −483.6 kJ/mol of O<sub>2</sub> |
:ΔH = −483.6 kJ/mol of O<sub>2</sub><ref> http://chemistry.osu.edu/~woodward/ch121/ch5_enthalpy.htm </ref> |
||
==सन्दर्भ== |
==सन्दर्भ== |
||
07:19, 31 अगस्त 2014 का अवतरण
| यह लेख एक आधार है। जानकारी जोड़कर इसे बढ़ाने में विकिपीडिया की मदद करें। |
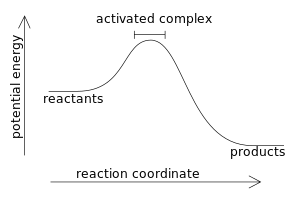
वह रासायनिक अभिक्रिया उष्माक्षेपी (exothermic reaction) कहलाती है जिसमें उष्मा के रूप में उर्जा प्राप्त होती है। इसके विपरीत रासायनिक अभिक्रिया उष्माशोषी कहलाती है। रासायनिक अभिक्रिया के रूप में व्यक्त करने पर -
- अभिकारक → उत्पाद + उर्जा (उष्मा के रूप में)
उदाहरण के लिए, हाइड्रोजन का जलना एक ऊष्माक्षेपी अभिक्रिया है।
- 2H2 (g) + O2 (g) → 2H2O (g)
- ΔH = −483.6 kJ/mol of O2[1]
