समस्थानिक
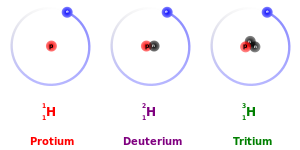
समस्थानिक (Isotope) एक ही तत्व के परमाणु जिनकी परमाणु संख्या समान होती हैं, परन्तु परमाणु भार अलग-अलग होता है, उन्हें समस्थानिक कहा जाता है। इनमें प्रत्येक परमाणु में समान प्रोटोन होते हैं। जबकि न्यूट्रॉन की संख्या अलग अलग रहती है। इस कारण परमाणु संख्या तो समान रहती है, लेकिन परमाणु का द्रव्यमान अलग अलग हो जाता है। समस्थानिक का अर्थ "समान स्थान" से है। आवर्त सारणी में तत्वों को परमाणु संख्या के आधार पर अलग अलग रखा जाता है, जबकि समस्थानिक में परमाणु संख्या के समान रहने के कारण उन्हें अलग नहीं किया गया है, इस कारण इन्हें समस्थानिक कहा जाता है।
परमाणु के नाभिक के भीतर प्रोटोन की संख्या को परमाणु संख्या कहा जाता है, जो बिना आयन वाले परमाणु के इलेक्ट्रॉन के बराबर होते हैं। प्रत्येक परमाणु संख्या किसी विशिष्ट तत्व की पहचान बताता है, लेकिन ऐसा समस्थानिक में नहीं होता है। इसमें किसी तत्व के परमाणु में न्यूट्रॉन की संख्या विस्तृत हो सकती है। प्रोटोन और न्यूट्रॉन की संख्या उस परमाणु का द्रव्यमान संख्या होता है और प्रत्येक समस्थानिक में द्रव्यमान संख्या अलग अलग होता है।
उदाहरण के लिए, कार्बन के तीन समस्थानिक कार्बन-12, कार्बन-13 और कार्बन-14 हैं। इनमें सभी का द्रव्यमान संख्या क्रमशः 12, 13 और 14 है। कार्बन में 6 परमाणु होता है, जिसका मतलब है कि कार्बन के सभी परमाणु में 6 प्रोटोन होते हैं और न्यूट्रॉन की संख्या क्रमशः 6, 7 और आठ है।
इतिहास [Histry]
[संपादित करें]रेडियोधर्मी समस्थानिक
[संपादित करें]समस्थानिक के होने की बात सबसे पहले 1913 में फ्रेडरिक सोड्डी ने बताई थी। उनके रेडियोधर्मी क्षय के अध्ययन से बताया कि यूरेनियम और सीसा के मध्य 40 अलग अलग रेडियोधर्मी तत्व हैं, जबकि आवर्त सारणी में यूरेनियम से सीसा तक मात्र 11 तत्वों को ही रखा गया है।
समस्थानिकों की सूची
[संपादित करें]| परमाणु क्रमांक | प्रतीक | परमाणु भार (कोष्ठक में प्रतिशत) |
|---|---|---|
| 1 | H | 1 (99,985), 2 (0,015) |
| 2 | He | 4 (99,99987), 3 (0,00013) |
| 3 | Li | 7 (92,6), 6 (7,4) |
| 4 | Be | 9 (100) |
| 5 | B | 11 (81,2), 10 (18,8) |
| 6 | C | 12 (98,89), 13 (1,11) |
| 7 | N | 14 (99,63), 15 (0,37) |
| 8 | O | 16 (99,759), 17 (0,037), 18 (0,204) |
| 9 | F | 19 (100) |
| 10 | Ne | 20 (90,92), 21 (0,26), 22 (8,82) |
| 11 | Na | 23 (100) |
| 12 | Mg | 24 (78,8), 25 (10,1), 26 (11,1) |
| 13 | Al | 27 (100) |
| 14 | Si | 28 (92,17), 29 (4,71), 30 (3,12) |
| 15 | P | 31 (100) |
| 16 | S | 32 (95), 33 (0,75), 34 (4,2), 36 (0,017) |
| 17 | Cl | 35 (75,53), 37 (24,47) |
| 18 | Ar | 40 (99,60), 36 (0,337), 38 (0,063) |
| 19 | K | 39 (93,2), 41 (6,8), 40a (0,0119) |
| 20 | Ca | 40 (96,9), 42 (0,64), 43 (0,14), 44 (2,1), 46 (0,0032), 48 (0,18) |
| 21 | Sc | 45 (100) |
| 22 | Ti | 48 (73,8), 46 (8,0), 47 (7,4), 49 (5,5), 50 (5,3) |
| 23 | V | 51 (99,75), 50a (0,25) |
| 24 | Cr | 52 (83,7), 50 (4,4), 53 (9,5), 54 (2,4) |
| 25 | Mn | 55 (100) |
| 26 | Fe | 56 (91,6), 54 (5,9), 57 (2,20), 58 (0,33) |
| 27 | Co | 59 (100) |
| 28 | Ni | 58 (68,0), 60 (26,2), 61 (1,1), 62 (3,7), 64 (1,0) |
| 29 | Cu | 63 (69,0), 65 (31,0) |
| 30 | Zn | 64 (48,9), 66 (27,8), 67 (4,1), 68 (18,6), 70 (0,63) |
| 31 | Ga | 69 (60,1), 71 (39,9) |
| 32 | Ge | 70 (20,5), 72 (27,4), 73 (7,8), 74 (36,5), 76 (7,8) |
| 33 | As | 75 (100) |
| 34 | Se | 74 (0,93), 76 (9,1), 77 (7,5), 78 (23,6), 80 (49,9), 82 (9,0) |
| 35 | Br | 79 (50,6), 81 (49,4) |
| 36 | Kr | 78 (0,35), 80 (2,27), 82 (11,6), 83 (11,5), 84 (57,0), 86 (17,3) |
| 37 | Rb | 85 (72,2), 87a (27,8) |
| 38 | Sr | 84 (0,55), 86 (9,8), 87 (7,0), 88 (82,7) |
| 39 | Y | 89 (100) |
| 40 | Zr | 90 (51,5), 91 (11,2), 92 (17,1), 94 (17,4), 96 (2,8) |
| 41 | Nb | 93 (100) |
| 42 | Mo | 92 (15,7), 94 (9,3), 95 (15,7), 96 (16,5), 97 (9,5), 98 (23,8), 100 (9,5) |
| 43 | Tc | कोई स्थायी समस्थानिक नहीं है। |
| 44 | Ru | 96 (5,6), 98 (1,9), 99 (12,7), 100 (12,7), 101 (17,0), 102 (31,5), 104 (18,6) |
| 45 | Rh | 103 (100) |
| 46 | Pd | 102 (1,0), 104 (11,0), 105 (22,2), 106 (27,3), 108 (26,7), 110 (11,8) |
| 47 | Ag | 107 (51,4), 109 (48,6) |
| 48 | Cd | 106 (1,22), 108 (0,88), 110 (12,4), 111 (12,8), 112 (24,0), 113 (12,3), 114 (28,8), 116 (7,6) |
| 49 | In | 113 (4,2), 115a (95,8) |
| 50 | Sn | 112 (1,02), 114 (0,69), 115 (0,38), 116 (14,3), 117 (7,6), 118 (24,1), 119 (8,5), 120 (32,5), 122 (4,8), 124 (6,1) |
| 51 | Sb | 121 (57), 123 (43) |
| 52 | Te | 120 (0,091), 122 (2,5), 123a (0,88), 124 (4,6), 125 (7,0), 126 (18,7), 128 (31,8), 130 (34,4) |
| 53 | I | 127 (100) |
| 54 | Xe | 124 (0,094), 126 (0,092), 128 (1,92), 129 (26,4), 130 (4,1), 131 (21,2), 132 (26,9), 134 (10,4), 136 (8,9) |
| 55 | Cs | 133 (100) |
| 56 | Ba | 130 (0,101), 132 (0,097), 134 (2,42), 135 (6,6), 136 (7,8), 137 (11,3), 138 (71,7) |
| 57 | La | 138a (0,089), 139 (99,911) |
| 72 | Hf | 174 (0,18), 176 (5,2), 177 (18,5), 178 (27,1), 179 (13,8), 180 (35,2) |
| 73 | Ta | 180a (0,012), 181 (99,988) |
| 74 | W | 180 (0,14), 182 (26,2), 183 (14,3), 184 (30,7), 186 (28,7) |
| 75 | Re | 185 (37,1), 187a (62,9) |
| 76 | Os | 184 (0,018), 186 (1,59), 187 (1,64), 188 (13,3), 189 (16,1), 190 (26,4), 192 (41,0) |
| 77 | Ir | 191 (38,5), 193 (61,5) |
| 78 | Pt | 192 (0,78), 194 (32,8), 195 (33,7), 196 (25,4), 198 (7,2) |
| 79 | Au | 197 (100) |
| 80 | Hg | 196 (0,15), 198 (10,0), 199 (16,9), 200 (23,1), 201 (13,2), 202 (29,8), 204 (6,8) |
| 81 | Tl | 203 (29,5), 205 (70,5) |
| 82 | Pb | 204 (1,3), 206 (26), 207 (21), 208 (52) |
| 83 | Bi | 209a (100) |
