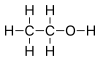
इथेनॉल
| इथेनॉल | |
|---|---|
 | |
 |
 |
| आईयूपीएसी नाम | इथेनॉल |
| अन्य नाम | Ethyl alcohol; grain alcohol; pure alcohol; hydroxyethane; drinking alcohol; ethyl hydrate |
| पहचान आइडेन्टिफायर्स | |
| सी.ए.एस संख्या | [64-17-5] |
| RTECS number | KQ6300000 |
| SMILES | |
| कैमस्पाइडर आई.डी | |
| गुण | |
| आण्विक सूत्र | C2H6O |
| मोलर द्रव्यमान | 46.06844(232) g/mol |
| दिखावट | colorless clear liquid |
| घनत्व | 0.789 g/cm³, liquid |
| गलनांक |
−114.3 °C (158.8 K) |
| क्वथनांक |
78.4 °C, 173.1 F (351.6 K) |
| जल में घुलनशीलता | Fully miscible |
| अम्लता (pKa) | 15.9 |
| श्यानता | 1.200 mPa·s (cP) at 20.0 °C |
| Dipole moment | 5.64 fC·fm (1.69 D) (gas) |
| खतरा | |
| EU वर्गीकरण | Highly Flammable (F) |
| NFPA 704 | |
| R-फ्रेसेज़ | R11 साँचा:R20 साँचा:R21 आर-२२ R36 |
| S-फ्रेसेज़ | (एस२), साँचा:S7, S16 |
| स्फुरांक (फ्लैश पॉइन्ट) | 286.15 K (13 °C or 55.4 °F) |
| Related compounds | |
| जहां दिया है वहां के अलावा, ये आंकड़े पदार्थ की मानक स्थिति (२५ °से, १०० कि.पा के अनुसार हैं। ज्ञानसन्दूक के संदर्भ | |
एथेनॉल (Ethanol) एक प्रसिद्ध अल्कोहल है। इसे एथिल अल्कोहल भी कहते हैं।
इथेनॉल(एल्कोहोल) निर्माण की विधियां[संपादित करें]
इसको तैयार करने की दो विभिन्न विधियाँ हैं :
(१) संश्लेषण विधि-एथिलीन गैस को सांद्र सल्फ़्यूरिक अम्ल में शोषित कराने से एथिल हाइड्रोजन सल्फ़ेट बनता है जो जल के साथ उबालने पर उद्धिघटित (हाइड्रोलाइज़) होकर एथिल ऐल्कोहल देता है। इस विधि का प्रचलन अभी अधिक नहीं है।
(२) किण्वीकरण विधि- इसके द्वारा किसी भी शक्करमय पदार्थ (गन्ने की शक्कर, ग्लूकोस, शोरा, महुए का फूल आदि) या स्टार्चमय पदार्थ (आलू, चावल, जौ, मकई आदि) से ऐल्कोहल व्यापारिक मात्रा में बनाते हैं। इस अभिक्रिया को मोटे तौर पर निम्नलिखित प्रकार से लिखा जा सकता है-[1]:
- C6H12O6 → 2 C2H5OH + 2 CO2
साधारणत: ऐल्कोहल शीरे से, जो शक्कर और चुकंदर के मिलों में व्यर्थ बचा पदार्थ है, बनाया जाता है। शीरे में लगभग ३० से ३५ प्रतिशत तक गन्ने की शक्कर तथा लगभग इतना ही ग्लुकोस और फ्रुंक्टोस घुला रहता है। शोरे में इतना ही जल मिलाया जाता है जितने से उसका आपेक्षिक घनत्व १.०३ से लेकर १.०४ तक हो जाता है। जीवाणुओं तथा अन्य अनावश्यक किण्वों की वृद्धि रोकने के लिए इस घोल में सल्फ़्यूरिक अम्ल की कुछ बूंदें डाल देते हैं। अब इसमें थोड़ा सा यीस्ट डालकर इसे ३०°-४०° सेंटीग्रेड ताप पर रख देते हैं। लगभग ४०-५० घंटों में किण्वीकरण समाप्त हो जाता है। इस प्रकार से शीरे की लगभग ९५% शक्कर विच्छिन्न होकर ऐल्कोहल और कार्बन-डाइ-आक्साइड में परिवर्तित हो जाती है।
स्टार्चमय पदार्थों को पहले छोटे-छोटे टुकड़े कर या पानी के साथ पीसकर तप्त भाप में उबालते हैं। स्टार्चमय पदार्थ लेई की तरह हो जाता है; इसे हलवा (अंग्रेजी में मैश) कहते हैं। मैश में थोड़ा माल्ट निष्कर्ष मिलाकर ५५°-६०° सेंटीग्रेड ताप पर रख देते हैं। माल्ट निष्कर्ष में विद्यमान डायस्टेस-एंज़ाइम द्वारा स्टार्च का उद्विघटन होकर माल्टोस बनता है। इस क्रिया में लगभग आध घंटा लगता है और जो द्रव इस प्रकार मिलता है उसे क्वाथ (अंग्रेजी में वर्ट) कहते हैं। क्वाथ को उबालकर इसमें विद्यमान डायस्टेस को नष्ट कर देते हैं; इसे २०° सें. ताप तक ठंडा कर इसमें यीस्ट डालते हैं और फिर इसे २०°-३७° सें. के बीच रख छोड़ते हैं। यीस्ट में विद्यमान माल्टेस-एंज़ाइम माल्टोस को उद्विघटित कर ग्लूकोस में परिवर्तित करता है। इस ग्लूकोस को फिर ज़ाइमेस-एंज़ाइम द्वारा विघटित कर एल्कोहल प्राप्त करते हैं। इस प्रकार से एल्कोहल बनाने में ३-४ दिन लगते हैं।
किण्वीकरण के बाद जो द्रव मिलता है उसे धोवन (वाश) कहते हैं; इसमें एल्कोहल लगभग १०-१५% तक होता है; इसका प्रभाजित आसवन करने पर जो द्रव मिलता है उसमें लगभग ९५.६% एल्कोहल होता है; इसको रेक्टिफ़ायड स्परिट कहते हैं। प्रभाजित आसवन के लिए कई प्रकार के भभके उपयोग में आते हैं। भारत तथा इंग्लैंड में कॉफे भभके का अधिक प्रचलन है; इसके द्वारा एक ही बार में आसवन से रेक्टिफ़ायड स्पिरिट प्राप्त की जाती है। इस गैलन शीरे से लगभग ०.४ गैलन रेक्टिफ़ायड स्पिरिट प्राप्त होता है। इस रेक्टिफ़ायड स्पिरिट में एल्कोहल के अतिरिक्त थोड़ी मात्रा में ऐसिटेल्डिहाइड, ग्लिसरीन, सकसिनिक अम्ल और फ़्यूज़ेल तेल अशुद्धि के रूप में रहते हैं। इन अशुद्धियों को अलग करने के लिए इसको पहले लकड़ी के कोयले के छन्ने द्वारा छानते हैं और फिर प्रभाजित आसवन द्वारा प्रथम, द्वितीय और अंतिम स्रव-अंश प्रात करते हैं जिनमें क्रमश: ऐसिटैल्डिहाइड, रेक्टिफ़ायड स्पिरिट तथा फ़्यूज़ेल तेल रहता है।
रेक्टिफ़ायड स्पिरिट से जलरहित विशुद्ध ऐल्कोहल बनाने की साधारण विधि यह है कि इसमें थोड़ा बरी का चूना डाल देते हैं; एक दो दिन के बाद ऐल्कोहल को निथारकर आसवन पात्र में रखकर सोडियम या कैल्सियम के ताज़े कटे छोटे-छोटे थोड़े से टुकड़े डालकर इसे तुरंत आसवित करते हैं। ग्राहक पात्र में हवा से जलवाष्प न जा सके इसके लिए उसमें कैल्सियम क्लोराइड से भरी हुई एक नली लगा दी जाती है। व्यापारिक विधि में रेक्टिफ़ायड स्पिरिट में बेंज़ीन मिलाकर बेंज़ीन, ऐल्कोहल और जल तीनों के समक्वाथी त्रय-मिश्रण को गर्म करते हैं। ऐल्कोहल में जितना जल रहता है वह सब इस त्रय-मिश्रण के रूप में ६४.९° सें. तक बाहर निकल जाता है। मिश्रण में अब केवल बेंज़ीन और ऐल्कोहल रह जाता है। इस द्वय-मिश्रण के ६८.३° सें. पर आसवित होकर निकल जाने पर विशुद्ध ऐल्कोहल ७८.३ सें. पर आसवित होता है।
साधारणत: पेय ऐल्कोहल पर भारी कर लगाया जाता है। उद्योगविस्तार के लिए औद्योगिक ऐल्कोहल का सस्ता मिलना आवश्यक है। इसलिए उसपर कर या तो नहीं लगता है या बहुत कम। लोग उसे पी सकें, इस उद्देश्य से प्रत्येक देश में करमुक्त ऐल्कोहल में कुछ ऐसे विषैले और अस्वास्थ्यकर पदार्थों को मिलाते हैं जिससे वह अपेय हो जाए किंतु अन्य कार्यों अनुपयुक्त न होने पाए। अधिकांश देशें में रेक्टिफ़ायड स्पिरिट में ५ से १० प्रतिशत तक मेथिल ऐल्कोहल और ०.५% पिरीडीन मिला देते हैं और उसे मेथिलेटेड स्पिरिट कहते हैं। मेथिल ऐल्कोहल के कारण ही मेथिलेटेड स्पिरिट नाम पड़ा है। किंतु आजकल बहुत से विकृत ऐल्कोहलों में मेथिल ऐल्कोहल बिल्कुल नहीं रहता। भारत में विकृत स्पिरिट में साधारणत: ०.५% पिरीडीन और ०.५% पतला रबर स्राव रहता है।
सभी प्रकार की मदिरा में एथिल ऐल्कोहल होता है। कुछ प्रचलित आसुत (डिस्टिल्ड) मदिराओं के नाम ह्विस्की, ब्रांडी, रम जिन और बॉडका हैं। इनको क्रमानुसार जौ, अंगूर, शीरा, मकई और नीवारिका से बनाते हैं और इनमें ऐल्कोहल क्रमानुसार ४०, ४०, ४०, ३५-४० और ४५ प्रतिशत होता है। वियर, वाइन, शैपेन, पोर्ट, शेरी और साइडर कुछ मुख्य निरासुत मदिराएँ हैं; वियर जौ से तथा और सब दूसरी सब अंगूर से बनाई जाती हैं; इनमें ऐल्कोहल की मात्रा ३ से २० प्रतिशत तक होती है।
मदिरा तथा अन्य ऐल्कोहलीय द्रवों में ऐल्कोहल की मात्रा ज्ञात करने की विधि को ऐल्कोहलमिति कहते हैं। इसके लिए एक तालिका तैयार कर ली जाती है जिसमें विभिन्न आपेक्षिक घनत्वों के ऐल्कोहललीय द्रवों में विभिन्न तापों पर ऐल्कोहल की प्रतिशत मात्रा दी रहती है। अज्ञात ऐल्कोहलीय द्रव का आपेक्षिक घनत्व हाइड्रोमीटर से तथा ताप तापमापी से ज्ञात कर तालिका की सहायता से उस द्रव में उपस्थित ऐल्कोहल की प्रतिशत मात्रा ज्ञात कर ली जाती है। कर लगाने की सुविधा के लिए एक निश्चित प्रतिशत के ऐल्कोहलीय द्रव को प्रामाणिक मान लिया गया है; इसको प्रूफ़ स्पिरिट कहते हैं; इसमें मात्रा के अनुसार ४९.३% तथा आयतन के अनुसार ५७.१% ऐल्कोहल रहता है। अन्य ऐल्कोहलीय द्रवों की सांद्रता प्रूफ़ स्पिरिट के आधार पर व्यक्त की जाती है।
ऐल्कोहलीय किण्वीकरण में ऐल्कोहल के अतिरिक्त निम्नलिखित मूल्यवान् पदार्थ भी सहउत्पाद (बाई प्रॉडक्ट) के रूप में प्राप्त होते हैं :
- १. कार्बन डाइ-आक्साइड- किण्वीकरण के समय यह गैस अधिक मात्रा में निकलती है। साधारणत: इसे ठंडा कर ठोस में परिवर्तित करके शुष्क हिम के नाम से बाजार में बेचते हैं। इसका उपयोग बहुत ठंडक पैदा करने के लिए होता है।
- २. एर्गाल या टार्टार - शक्करयुकत पदार्थों का किण्वीकरण जिस पात्र में होता है उसकी भीतरी दीवारों पर एक मटमैल रंग की कड़ी पपड़ी जम जाती है। इसको एर्गाल या टार्टार कहते हैं। इसमें मुख्य रूप से पोटैशियम हाइड्रोजन टारटरेट रहता है जिससे टारटरिक अम्ल अधिक मात्रा में बनाई जाती है।
- ३. वाश के आसवन के प्रथम अंश ऐसिटैल्डिहाइड तथा दूसरे उड़नशील एस्टर होते हैं।
- ४. फ़्यूज़ेल तेल - यह अधिक अणुभारवाले ऐक्लाकोहलों का मिश्रण होता है। इसमें से आइसो अमाइल ऐल्कोहल को प्रभालित आसवन द्वारा पृथक् कर लेते हैं, क्योंकि यह एक उत्तम विलेयक है।
- ५. निर्जीव धोवन - आसवन द्वारा ऐल्काहल को धोवन (वाश) में से अलग करने के बाद जो शेष द्रव तलछट के रूप में बच रहता है उसे निर्जीव धोवन कहते हैं। स्टार्चमय पदार्थों की चर्बी तथा प्रोटीन का अधिकांश भाग अविघटित रूप में निर्जीव धोवन में रहता है, इसलिए यह जानवरों के पौष्टिक चारे के लिए उपयोग में आता है।
उपयोगिता[संपादित करें]
उद्योग में एथिल ऐल्कोहल की उपयोगिता इसकी अत्युत्तम विलेयक शक्ति के कारण है। इसका उपयोग वार्निश, पालिश, दवाओं के घोल तथा निष्कर्ष, ईथर, क्लोरोफ़ार्म, कृत्रिम रंग, पारदर्शक साबुन, इत्र तथा फल की सुगंधों का निष्कर्ष और अन्य रासायनिक यौगिक बनाने में होता है। पीने के लिए विभिन्न मदिराओं के रूप में, घावों को धोने में जीवाणुनाशक के रूप में तथा प्रयोगशाला में घोलक के रूप में इसका उपयोग होता है। पीने को औषधियों में यह डाला जाता है और मरे हुए जीवों को संरक्षित रखने में भी इसका उपयोग होता है। रेआन ऐसिटेट उद्योग के लिए ऐसीटिक अम्ल की पूर्ति मैंगनीज़ पराक्साइड तथा सल्फ़्यूरिक अम्ल की उपस्थिति में ऐल्कोहल का आक्सीकरण करके होती है, क्योंकि यह क्रिया शीघ्र होती है और इससे ऐसीटिक अम्ल तथा ऐसिटैल्डिहाइड प्राप्त होते हैं। स्पिरिट लैंप तथा स्टोव में और मोटर इंजनों में पेट्रोल के साथ इसको ईंधन के रूप में जलाते हैं। इसके अधिक उड़नशील न होने के कारण मोटर को चलाने में कठिनाई न हो इस उद्देश्य से इसमें २५% ईथर या पेट्रोल मिलाते हैं।
सन्दर्भ[संपादित करें]
- ↑ SAFFIOTI, WALDEMAR; Fundamentos de Química; Companhia Editora Nacional; São Paulo, Brasil; 1968
बाहरी कड़ियाँ[संपादित करें]
- ऐथनॉल पर पॉलिसी लाएगी सरकार, होगी 'बड़ी' बचत (Feb 27, 2017)
- Ethanol Information
- Molview from bluerhinos.co.uk See Ethanol in 3D
- National Institute of Standards and Technology chemical data on ethanol
- ChEBI – biology related
- पेट्रोल में मिश्रण के लिए एथनॉल कीमतों में संशोधन को मंजूरी (Oct 13th 2016)
| यह लेख कार्बनिक यौगिक के बारे में एक आधार है। जानकारी जोड़कर इसे बढ़ाने में विकिपीडिया की मदद करें। |


