"ऊष्माक्षेपी अभिक्रिया": अवतरणों में अंतर
Content deleted Content added
छो बॉट: पुनर्प्रेषण ठीक कर रहा है |
Rescuing 2 sources and tagging 0 as dead.) #IABot (v2.0.1 |
||
| पंक्ति 7: | पंक्ति 7: | ||
:2H<sub>2</sub> (g) + O<sub>2</sub> (g) → 2H<sub>2</sub>O (g) |
:2H<sub>2</sub> (g) + O<sub>2</sub> (g) → 2H<sub>2</sub>O (g) |
||
:ΔH = −483.6 kJ/mol of O<sub>2</sub><ref> http://chemistry.osu.edu/~woodward/ch121/ch5_enthalpy.htm </ref> |
:ΔH = −483.6 kJ/mol of O<sub>2</sub><ref>{{Cite web |url=http://chemistry.osu.edu/~woodward/ch121/ch5_enthalpy.htm |title=संग्रहीत प्रति |access-date=5 सितंबर 2013 |archive-url=https://web.archive.org/web/20130708030319/http://chemistry.osu.edu/~woodward/ch121/ch5_enthalpy.htm |archive-date=8 जुलाई 2013 |url-status=dead }}</ref> |
||
Example- emission of light |
Example- emission of light |
||
H+ + OH- H2O |
H+ + OH- H2O |
||
| पंक्ति 15: | पंक्ति 15: | ||
== बाहरी कड़ियाँ == |
== बाहरी कड़ियाँ == |
||
* [http://www.gcsescience.com/rc24.htm GCSE Science: Reactions] |
* [https://web.archive.org/web/20081121211747/http://www.gcsescience.com/rc24.htm GCSE Science: Reactions] |
||
[[श्रेणी:उष्मारसायन]] |
[[श्रेणी:उष्मारसायन]] |
||
03:02, 16 जून 2020 का अवतरण
| यह लेख एक आधार है। जानकारी जोड़कर इसे बढ़ाने में विकिपीडिया की मदद करें। |
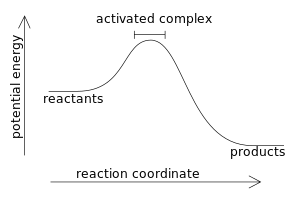
वह रासायनिक अभिक्रिया उष्माक्षेपी (exothermic reaction) कहलाती है जिसमें उष्मा के रूप में उर्जा प्राप्त होती है। इसके विपरीत रासायनिक अभिक्रिया उष्माशोषी कहलाती है। रासायनिक अभिक्रिया के रूप में व्यक्त करने पर -
- अभिकारक → उत्पाद + उर्जा (उष्मा के रूप में)
उदाहरण के लिए, हाइड्रोजन का जलना एक ऊष्माक्षेपी अभिक्रिया है।
- 2H2 (g) + O2 (g) → 2H2O (g)
- ΔH = −483.6 kJ/mol of O2[1]
Example- emission of light H+ + OH- H2O
सन्दर्भ
- ↑ "संग्रहीत प्रति". मूल से 8 जुलाई 2013 को पुरालेखित. अभिगमन तिथि 5 सितंबर 2013.
