हेपरिन

| |

| |
| सिस्टमैटिक (आईयूपीएसी) नाम | |
|---|---|
| see Heparin structure | |
| परिचायक | |
| CAS संख्या | 9005-49-6 |
| en:PubChem | 772 |
| en:DrugBank | APRD00056 |
| en:ChemSpider | 17216115 |
| रासायनिक आंकड़े | |
| सूत्र | C12H19NO20S3 |
| आण्विक भार | 12000–15000 g/mol |
| फ़ार्मओकोकाइनेटिक आंकड़े | |
| जैव उपलब्धता | nil |
| उपापचय | hepatic |
| अर्धायु | 1.5 hrs |
| उत्सर्जन | ? |
| इस लेख में सत्यापन हेतु अतिरिक्त संदर्भ अथवा स्रोतों की आवश्यकता है। कृपया विश्वसनीय स्रोत जोड़कर इस लेख में सुधार करें। स्रोतहीन सामग्री को चुनौती दी जा सकती है और हटाया भी जा सकता है। (अप्रैल 2010) स्रोत खोजें: "हेपरिन" – समाचार · अखबार पुरालेख · किताबें · विद्वान · जेस्टोर (JSTOR) |
हेपरिन (प्राचीन ग्रीक ηπαρ से (हेपर), यकृत), जिसे अखंडित हेपरिन के रूप में भी जाना जाता है, एक उच्च-सल्फेट ग्लाइकोसमिनोग्लाइकन, व्यापक रूप से एक थक्का-रोधी इंजेक्शन के रूप में प्रयोग किया जाता है और किसी भी ज्ञात जैविक अणु घनत्व से इसमें सबसे ज्यादा ऋणात्मक चार्ज है। [1] इसका इस्तेमाल विभिन्न प्रयोगात्मक और चिकित्सा उपकरणों जैसे टेस्ट ट्यूब और गुर्दे की डायलिसिस मशीनों पर थक्का-रोधी आंतरिक सतह बनाने के लिए किया जाता है। फ़ार्मास्युटिकल ग्रेड हेपरिन को मांस के लिए वध किये जाने वाले जानवरों, जैसे शूकरीय (सुअर) आंत या गोजातीय (गाय) फेफड़े के म्युकोसल ऊतकों से प्राप्त किया जाता है। [2] [तथ्य वांछित]
हालांकि चिकित्सा में इसका उपयोग मुख्य रूप से थक्कारोध के लिए किया जाता है, शरीर में इसकी वास्तविक क्रियात्मक भूमिका अस्पष्ट बनी हुई है, क्योंकि रक्त विरोधी स्कंदन को अधिकांशतः हेपरन सल्फेट प्रोटियोग्लाइकन्स द्वारा हासिल किया जाता है जिसे अंतःस्तरीय कोशिकाओं से प्राप्त किया जाता है। [3] हेपरिन आम तौर पर मास्ट कोशिका के स्रावी बीजाणु के भीतर संग्रहीत रहता है और सिर्फ ऊतक चोट की जगहों पर वस्कुलेचर में जारी होता है। यह प्रस्तावित है कि थक्कारोध के बजाय, हेपरिन का मुख्य उद्देश्य ऐसी जगहों पर हमलावर बैक्टीरिया और अन्य बाह्य तत्वों से रक्षा करना है। [4] इसके अलावा, यह व्यापक रूप से विभिन्न प्रजातियों में संरक्षित है, जिनमें शामिल हैं कुछ अकशेरुकी जीव जिनमें ऐसी ही समान रक्त जमाव प्रणाली नहीं है।
हेपरिन संरचना[संपादित करें]
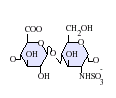
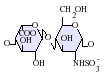
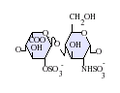
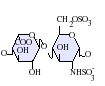
देशी हेपरिन एक बहुलक है जिसका आणविक भार 3 kDa से 30 kDa तक होता है, हालांकि अधिकांश वाणिज्यिक हेपरिन निर्माण का औसत आण्विक भार 12 kDa से 15 kDa के बीच होता है। [5] हेपरिन, कार्बोहाइड्रेट के (जिसमें शामिल है निकट सम्बन्धी अणु हेपारन सल्फेट)ग्लाइकोसमिनोग्लाइकन परिवार का एक सदस्य है जो एक परिवर्तनशील-सल्फेटकृत डाईसैकराइड इकाई से बना है। [6] मुख्य डाईसैकराइड इकाइयां जो हेपरिन में होती हैं उन्हें नीचे दिखाया गया हैं। सबसे आम डाईसैकराइड इकाई एक 2-O-सल्फेटकृत इडुरोनिक एसिड और 6-O-सल्फेटकृत, N-सल्फेटकृत ग्लुकोसेमाइन, IdoA(2S)-GlcNS (6S) से बनी होती है। उदाहरण के लिए, यह गोमांस के फेफड़ों से 85% के हेपरिन का निर्माण करता है और शूकरीय आंत्रिक मुकोसा से 75% बनाता है। [7] कुछ दुर्लभ डाईसैकराइड होते हैं जिन्हें नीचे नहीं दिखाया गया है जिसमें 3-O-सल्फेटकृत ग्लुकोसमाइन (GlcNS(3S,6s)) होता है या एक मुक्त अमीन समूह (GlcNH3+). शारीरिक स्थितियों के तहत, एस्टर और अमाइड सल्फेट समूहों से प्रोटोन हटा दिया जाता है और ये एक हेपरिन नमक के गठन के लिए धनात्मक-चार्ज काउन्टीरियन को आकर्षित करते हैं। ऐसा इसी रूप में होता है कि हेपरिन को आम तौर पर एक थक्का-रोधी के रूप में दिया जाता है।
हेपरिन की एक इकाई ("हॉवेल यूनिट") शुद्ध हेपरिन की 0.002 mg की मात्रा के लगभग बराबर की मात्रा है, इतनी ही मात्रा की आवश्यकता एक बिल्ली के तरल रक्त को 24 घंटे के लिए 0 °C पर रखने के लिए आवश्यक होती है। [8]
लघुरूप[संपादित करें]
- GlcA = β-D-ग्लुकुरोनिक एसिड
- IdoA = α-L-इडुरोनिक एसिड
- IdoA(2S) = 2-O-सल्फो-α-L-इडुरोनिक एसिड
- GlcNAc = 2-डिओक्सी-2-एसेटामीडो-α-D-ग्लुकोपाइरानोज़िल
- GlcNS = 2-डिओक्सी-2-सल्फामीडो-α-D-ग्लुकोपाइरानोज़िल
- GlcNS(6s) = 2-डिओक्सी-2-सल्फामीडो-α-D-ग्लुकोपाइरानोज़िल-6-O-सल्फेट
तीन आयामी संरचना[संपादित करें]
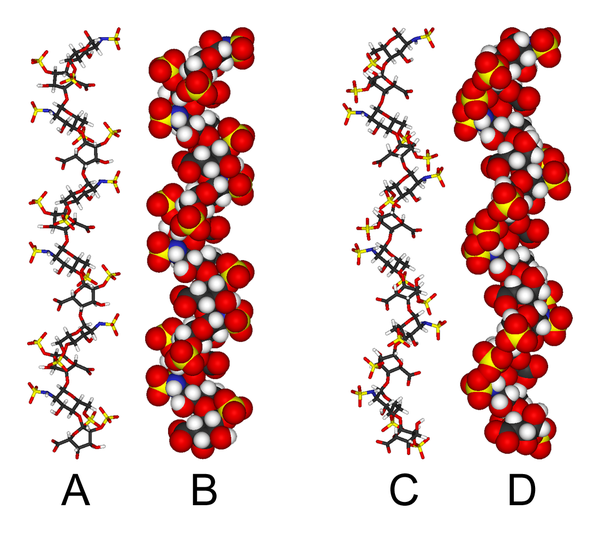
हेपरिन की त्रि-आयामी संरचना इस बात से जटिल हो जाती है कि इडुरोनिक एसिड दोनों में से किसी एक निम्न-ऊर्जा गठन में मौजूद हो सकता है जब इसे एक औलिगोसैक्राइड के अन्दर एक आंतरिक रूप से रखा जाता है। गठनात्मक संतुलन, आसन्न ग्लुकोसेमाइन शर्करा के सल्फेशन स्थिति द्वारा प्रभावित होता है। [9] फिर भी, हेपरिन के एक डोडेकासैकराइड की घोल संरचना जो पूरी तरह से छह GlcNS(6S)-IdoA(2S) के दोहराव इकाइयों से गठित है, उसका निर्धारण NMR स्पेक्ट्रोस्कोपी और आण्विक मॉडलिंग तकनीक के संयोजन के इस्तेमाल से किया जाता है। [10] दो मॉडल का निर्माण किया गया, एक जिसमें सभी IdoA(2S), 2S0 (A और B नीचे) गठन में थे और दूसरा जिसमें वे 1C4 गठन में हैं (C और D नीचे). लेकिन ऐसा कोई सबूत नहीं है कि जिससे यह सुझाव दिया जाए कि इन गठनों के बीच परिवर्तन एक ठोस शैली में घटित होते है। ये मॉडल, प्रोटीन डेटा बैंक कोड के अनुरूप हैं 1HPN.
ऊपर की छवि में:
- A = 1HPN (सभी IdoA(2S)) अवशिष्ट 2S0 गठन में Jmol viewer
- B = वैन डेर वाल्स रेडिअस A का स्पेस फिलिंग मॉडल
- C = 1HPN (सभी IdoA(2S)) अवशिष्ट 1C4 गठन में Jmol viewer
- D = वैन डेर वाल्स त्रिज्या C का स्पेस फिलिंग मॉडल
इन मॉडलों में, हेपरिन एक पेचदार गठन अपनाता है, जिसका घुमाव, सल्फेट समूहों के गुच्छों को पेचदार धुरी के दोनों ओर करीब 17 एंगस्ट्रोम (1.7 nm) के एक नियमित अंतराल पर रखता है।
नामकरण, वर्गीकरण और संहिताकरण[संपादित करें]
| इस अनुभाग को विस्तार की ज़रूरत है। |
चिकित्सकीय प्रयोग[संपादित करें]
हेपरिन एक स्वाभाविक रूप से मौजूद रहने वाला थक्का-रोधी है जिसका उत्पादन बैसोफिल और मास्ट ऊतक द्वारा किया जाता है। [11] हेपरिन एक थक्का-रोधी के रूप में कार्य करता है, जहां यह थक्कों और मौजूदा थक्कों को खून के भीतर विस्तारित होने से रोकता है। जबकि हेपरिन उन थक्कों को नहीं तोड़ता है जो पहले से बन गए हैं (ऊतक प्लाज्मीनोजेन उत्प्रेरक के विपरीत), यह शरीर के प्राकृतिक थक्का लाइसिस तंत्र को बन चुके थक्कों को तोड़ने के लिए सामान्य रूप से कार्य करने की अनुमति देता है। हेपरिन को आम तौर पर, निम्नलिखित स्थितियों के लिए थक्का-रोधन के लिए प्रयोग किया जाता है:
- एक्यूट कोरोनरी सिंड्रोम, जैसे, NSTEMI
- अलिंद विकम्पन
- गहन-शिरा घनास्त्रता और फुफ्फुसीय अन्त:शल्यता
- हार्ट सर्जरी के लिए कार्डियोपल्मोनरी बाईपास
- अतिरिक्त-कायिक जीवन समर्थन के लिए ECMO सर्किट
हेपरिन और इसके निम्न आणविक भार के व्युत्पन्न (जैसे इनोक्सापारिन, डाल्टपारिन, टीन्ज़ापारिन), रोगियों में गहन-शिरा घनास्त्रता और फुफ्फुसीय अन्तःशल्यता को रोकने में प्रभावी हैं,[12][13] लेकिन ऐसा कोई सबूत नहीं है इनमें से कोई भी एक मृत्यु को रोकने में अधिक प्रभावी है। [14] हेपरिन, एंजाइम प्रावरोधक एंटीथ्रोम्बिन III (AT) में बंध जाता है और एक गठनात्मक परिवर्तन को पैदा करता है जो प्रतिक्रियाशील साईट लूप के लचीलेपन में वृद्धि के माध्यम से इसके सक्रियण को फलित करता है। [15] सक्रिय AT फिर थ्रोम्बिन और रक्त के थक्के में शामिल अन्य प्रोटीज़ को निष्क्रिय कर देता है, सबसे खासकर कारक Xa को। AT द्वारा इन प्रोटीज़ का निष्क्रियन दर, हेपरिन के बंधन की वजह से 1000-गुना बढ़ सकता है। [16]
AT, हेपरिन बहुलक में निहित एक विशिष्ट पेंटासैक्राइड सल्फेशन अनुक्रम से बंधता है
GlcNAc/NS(6S)-GlcA-GlcNS(3S,6S)-IdoA(2S)-GlcNS(6S)
हेपरिन-बंधन पर AT में गठनात्मक परिवर्तन, कारक Xa के उसके निषेध में मध्यस्थता करता है। थ्रोम्बिन निषेध के लिए, हालांकि, थ्रोम्बिन को हेपरिन बहुलक से ऐसे साईट पर बंधन करना चाहिए जो पेंटासैक्राइड के नज़दीक है। हेपरिन का उच्च-ऋणात्मक चार्ज घनत्व, थ्रोम्बिन के साथ इसकी अत्यंत मज़बूत विद्युत-स्थैतिक अंतर्क्रिया करने में योगदान देता है। [1] AT, थ्रोम्बिन और हेपरिन के बीच त्रिगुट संकुल का गठन, थ्रोम्बिन की निष्क्रियता में फलित होता है। इस कारण से थ्रोम्बिन के खिलाफ हेपरिन की गतिविधि आकार-निर्भर है, जहां प्रभावी गठन के लिए त्रिगुट संकुल को कम से कम 18 सैक्राइड इकाइयों की आवश्यकता होती है। [17] इसके विपरीत, कारक विरोधी Xa गतिविधि को केवल पेंटासैक्राइड बाध्यकारी साइट की आवश्यकता होती है।

आकार के इस अंतर ने निम्न-आणविक भार वाले हेपरिन (LMWHs) को प्रेरित किया और अधिक हाल में फार्मास्युटिकल थक्का-रोधी के रूप में फोंडापारिनक्स को। निम्न-आणविक भार वाले हेपरिन और फोंडापारिनक्स, थ्रोम्बिन-विरोधी (IIa) गतिविधि के बजाय कारक-विरोधी Xa गतिविधि को लक्षित करते हैं, जहां उनका लक्ष्य जमाव के एक अधिक सूक्ष्म विनियमन और एक बेहतर चिकित्सीय सूचकांक को आसान करना है। फोंडापारिनक्स की रासायनिक संरचना बाईं तरफ दिखाई गई है। यह एक सिंथेटिक पेंटासैक्राइड है जिसकी रासायनिक संरचना, AT बाध्यकारी पेंटासैक्राइड अनुक्रम के लगभग समान है जिसे पौलिमेरिक हेपरिन और हेपारन सल्फेट में पाया जा सकता है।
LMWH और फोंडापारिनक्स के साथ, ऑस्टियोपोरोसिस और हेपरिन-जनित थ्रोम्बोसाइटोंपीनिया (HIT) का खतरा कम होता है। APTT की मॉनिटरिंग की भी जरूरत नहीं है और यह बेशक थक्का-रोधी प्रभाव को प्रतिबिंबित नहीं करता है, क्योंकि APTT, कारक Xa में परिवर्तन के प्रति असंवेदनशील है।
हेपारन सल्फेट का एक मिश्रण, डानापेरोइड, डर्माटन सल्फेट और कौनड्रॉयटिन सल्फेट को उन रोगियों के लिए थक्का-रोधी के रूप में इस्तेमाल किया जा सकता है जिनमें HIT विकसित हो चुका है। क्योंकि डानापेरोइड में हेपरिन या हेपरिन के टुकड़े नहीं होते, हेपरिन-जनित एंटीबॉडी के साथ डानापेरोइड की पार-अभिक्रियाशीलता को 10% से कम सूचित किया गया है। [18]
हेपरिन के प्रभाव को लैब में आंशिक थ्रोम्बोप्लास्टिन समय (aPTT) द्वारा मापा जाता है, (वह समय जितनी देर में रक्त प्लाज्मा थक्का बनता है).
दवा देना[संपादित करें]
हेपरिन को आन्त्रेतर दिया जाता है क्योंकि इसके उच्च नकारात्मक चार्ज और बड़े आकार के कारण इसे आंत द्वारा अवशोषित नहीं किया जाता है। हेपरिन को नसों के द्वारा या अवत्वचीय (त्वचा के नीचे) तरीके से अंतःक्षिप्त किया जा सकता है; रक्तगुल्म के गठन की संभावना की वजह से अंतर्पेशीय इंजेक्शन (मांसपेशी में) से परहेज किया जाता है। लगभग एक घंटे के लघु जैविक अर्ध-जीवन के कारण, हेपरिन को अक्सर दिया जाना चाहिए या एक सतत सेवन के रूप में होना चाहिए। हालांकि, निम्न-आणविक भार वाले हेपरिन (LMWH) की दैनिक एक खुराक की अनुमति दी गई है, इस प्रकार इसके लगातार सेवन की आवश्यकता नहीं होती है। अगर लंबी अवधि के लिए थक्का-रोधन की आवश्यकता है, तो हेपरिन को अक्सर थक्का-रोधी चिकित्सा की शुरुआत करने के लिए तब तक इस्तेमाल होता है जब तक कि मौखिक लिया जाने वाला वारफेरिन अपना प्रभाव नहीं शुरू कर देता.
इसे प्रदान करने का विवरण अमेरिकन कॉलेज ऑफ़ चेस्ट फिसीशियन द्वारा नैदानिक अभ्यास दिशा निर्देश में उपलब्ध है:[19]
- Non-weight-based heparin dose adjustment[मृत कड़ियाँ]
- Weight-based-heparin dose adjustment[मृत कड़ियाँ]
प्रतिकूल प्रतिक्रिया[संपादित करें]
हेपरिन का एक गंभीर पार्श्व-प्रभाव है हेपरिन प्रेरित थ्रोम्बोसाइटोपेनिया (HIT). HIT, प्रतिरक्षा सम्बन्धी प्रतिक्रिया के कारण होता है जो प्लेटलेट्स को प्रतिरक्षा सम्बन्धी प्रतिक्रिया का निशाना बनाता है, जो प्लेटलेट की गिरावट में फलित होता है। इसी कारण थ्रोम्बोसाइटोपेनिया होता है। यह स्थिति आम तौर पर विच्छेदन पर उलट जाती है और इससे सामान्यतः सिंथेटिक हेपरिन के उपयोग से बचा जा सकता है। थ्रोम्बोसाइटोपेनिया का एक सौम्य रूप भी है जो हेपरिन के आरंभिक उपयोग से जुड़ा है और जो हेपरिन को रोके बिना हल हो जाता है।
हेपरिन उपचार के दो गैर-रक्तस्रावी पार्श्व-प्रभाव हैं। पहला है सीरम अमीनोट्रांस्फेरेज़ स्तर, जिसे हेपरिन लेने वाले करीब 80% रोगियों में सूचित किया गया है। यह विषमता, यकृत रोग के साथ सम्बंधित नहीं है और यह दवा बंद कर देने के बाद गायब हो जाती है। अन्य जटिलता है हाइपरकलेमिया, जो हेपरिन लेने वाले 5% से 10% रोगियों में होती है और यह हेपरिन-प्रेरित अल्डोस्टरोन दबाव का परिणाम है। हेपरिन चिकित्सा की शुरुआत के कुछ ही दिनों के भीतर हाइपरकलेमिया दिखाई दे सकता है। अधिक दुर्लभता के साथ, लम्बे उपयोग के कारण दुष्प्रभाव के रूप में एलोपेसिया और ऑस्टियोपोरोसिस पनप सकते हैं।
जैसा कि कई दवाओं के साथ होता है, हेपरिन की अतिमात्रा घातक हो सकती है। सितम्बर 2006 में, हेपरिन को तब विश्वव्यापक प्रचार मिला जब समय से पहले जन्मे 3 शिशुओं की मृत्यु हो गई जब उन्हें इंडियानापोलिस अस्पताल में गलती से हेपरिन की अतिमात्रा दे दी गई। [20] प्रोटामिन सल्फेट (प्रति 100 इकाई हेपरिन में 1 mg जिसे चार घंटे से अधिक दिया गया) को हेपरिन के थक्का-रोधन की प्रतिक्रिया के लिए दिया गया। [21]
इतिहास[संपादित करें]
हेपरिन सबसे पुरानी दवाओं में से एक है जो आज भी व्यापक नैदानिक प्रयोग में है। इसकी खोज अमेरिकी फ़ूड एंड ड्रग एडमिनिस्ट्रेशन की स्थापना से पहले 1916 में हुई, हालांकि इसने नैदानिक परीक्षण में 1935 तक प्रवेश नहीं किया। [22] इसे मूल रूप से केनाइन जिगर कोशिकाओं से अलग किया गया था, इसलिए इसका नाम (हेपर या "ήπαρ" यूनानी भाषा में "जिगर" के लिए प्रयुक्त होता है). हेपरिन की खोज का श्रेय दो व्यक्तियों के अनुसंधान कार्यों को दिया जा सकता है: जे मेक्लियन और विलियम हेनरी हॉवेल.
1916 में, मेक्लियन, जो जॉन्स हॉपकिन्स विश्वविद्यालय में द्वितीय वर्ष का मेडिकल छात्र था हॉवेल के मार्गदर्शन में थक्का-समर्थक तैयारियों पर काम कर रहा था और उसने केनाइन जिगर कोशिका में वसा में घुलनशील फोस्फेटाइड थक्का-रोधी को अलग किया। 1918 में हॉवेल ने ही हेपरिन शब्द को गढ़ा (हेपर से, जिगर के लिए ग्रीक शब्द) 1918 में इस प्रकार के वसा-घुलनशील थक्का-रोधी के लिए। 1920 के दशक की शुरुआत में, हॉवेल ने एक पानी में घुलनशील पॉलीसैक्राइड थक्का-रोधी को अलग किया, उसे भी हेपरिन कहा गया, हालांकि यह पहले अलग किये गए फोस्फेटाइड से पृथक था। यह संभव है कि मेक्लियन के काम ने हॉवेल समूह के ध्यान को थक्का-रोधी को खोजने की तरफ खींचा, जो अंततः पॉलीसैक्राइड के आविष्कार में फलित हुआ। मेक्लियन ने एक सर्जन के रूप में काम किया। 67 वर्ष की आयु में स्थानिक अरक्तता सम्बन्धी हृदय रोग से उनकी मृत्यु हो गई। मरणोपरांत उन्हें नोबेल पुरस्कार के लिए मनोनीत करने का प्रयास असफल रहा।
1930 के दशक में, कई शोधकर्ताओं ने हेपरिन की पड़ताल की। कारोलिन्सका इंस्टीट्यूट के एरिक जोर्पेस ने 1935 में हेपरिन संरचना पर अपने अनुसंधान को प्रकाशित किया,[23] जिसने 1936 में स्वीडिश कंपनी विट्रम AB को अंतःशिरा प्रयोग के लिए पहला हेपरिन उत्पाद शुरू करने में सक्षम बनाया। 1933 और 1936 के बीच, कनॉट मेडिकल रिसर्च लेबोरेटरीज़ ने, जो उस वक्त टोरंटो विश्वविद्यालय का एक हिस्सा था, सुरक्षित, गैर-विषाक्त हेपरिन के उत्पादन की एक तकनीक को विकसित किया, जिसे एक नमक के घोल में रोगियों को दिया जा सकता था। हेपरिन का पहला मानव परीक्षण मई 1935 में शुरू हुआ और 1937 तक यह स्पष्ट था कि कनॉट का हेपरिन एक सुरक्षित, सुलभ और प्रभावी रक्त थक्का-रोधी है। 1933 से पहले हेपरिन उपलब्ध था, लेकिन अल्प मात्रा में और बहुत महंगा, विषाक्त और परिणामस्वरूप चिकित्सा में उपयोगी नहीं था। [24]
"द ऑरिजिन ऑफ़ द डिस्प्यूट ओवर द डिस्कवरी ऑफ़ हेपरिन" पर मार्कम का प्रपत्र हेपरिन की खोज और बाद के इतिहास का पूर्ण विवरण देता है। [25]
हेपरिन के लिए नवीन औषधि विकास के अवसर[संपादित करें]
जैसा कि नीचे तालिका में विवरण दिया गया है, हेपरिन सदृश संरचनाओं को रोगों की विस्तृत श्रृंखला के इलाज के लिए दवा के रूप में विकास की भरपूर क्षमताएं मौजूद हैं, जो उनके थक्का-रोधी के रूप में मौजूदा प्रयोग के अलावा है। [26][27]
| हेपरिन के प्रति संवेदनशील रोग की स्थिति | प्रयोगात्मक मॉडल में हेपरिन का प्रभाव | नैदानिक स्थिति | |
| वयस्क श्वसन संकट सिंड्रोम | वायुमार्ग में कोशिका सक्रियण और संचय को कम कर देता है, मध्यस्थों और साइटोक्सिक कोशिका उत्पादों को निष्प्रभावी कर देता है और पशु मॉडल में फेफड़ों की क्रिया में सुधार करता है | नियंत्रित नैदानिक परीक्षण है | |
| एलर्जी इन्सेफेलोमाईलिटिस | पशु मॉडल में प्रभावी | - | |
| एलर्जी रिनिटिस | वयस्क श्वसन संकट सिंड्रोम के लिए प्रभाव के रूप में, हालांकि किसी विशिष्ट नासिका मॉडल का परीक्षण नहीं किया गया है | नियंत्रित नैदानिक परीक्षण | |
| गठिया | कोशिका संचय को रोकता है, कोलाजेन विनाश और एन्जियोजिनेसिस | उपाख्यानात्मक रिपोर्ट | |
| दमा | वयस्क श्वसन संकट सिंड्रोम के लिए, लेकिन इसे प्रयोगात्मक मॉडल में फेफड़ों की क्रियाओं में सुधार करते दिखाया गया है | नियंत्रित नैदानिक परीक्षण | |
| कैंसर | ट्यूमर वृद्धि को रोकता है, मेटास्टेसिस और एन्जियोजिनेसिस और पशु मॉडल में अस्तित्व समय को बढ़ाता है | कई उपाख्यानात्मक रिपोर्टों | |
| विलंबित प्रकार हाइपरसेंसिटिविटी प्रतिक्रिया | पशु मॉडल में प्रभावी | - | |
| दाहक आंत्र रोग | सामान्य में दाहक कोशिका परिवहन को रोकता है। कोई विशिष्ट मॉडल का परीक्षण नहीं किया गया | नियंत्रित नैदानिक परीक्षण | |
| छिद्रपूर्ण मूत्राशयशोध | छिद्रपूर्ण मूत्राशयशोध के एक मानव प्रयोगात्मक मॉडल में प्रभावी | संबंधित अणु का अब नैदानिक इस्तेमाल होता है | |
| प्रत्यारोपण अस्वीकृति | पशु मॉडल में एलोग्रफ्ट अस्तित्व को लंबा करता है | - |
- कोई जानकारी उपलब्ध नहीं का संकेत देता है
रोग की विविध स्थितियों पर हेपरिन के प्रभाव के परिणामस्वरूप, कई दवाएं विकसित की जा रही हैं जिनकी आणविक संरचना, पौलिमेरिक हेपरिन श्रृंखला के हिस्सों में पाई जाने वाली संरचना के समान या मिलती-जुलती है। [26]
| औषध अणु | हेपरिन की तुलना में नई दवा का प्रभाव | जैविक गतिविधियां | |
| हेपरिन टेट्रासैक्राइड | गैर-थक्कारोधी, गैर-प्रतिरक्षा, मौखिक रूप से सक्रिय | एलर्जी-विरोधी | |
| पेंटोसन पौलीसल्फेट | पौधे से व्युत्पन्न, अल्प थक्का-रोधी गतिविधि, दाहक-विरोधी, मौखिक रूप से सक्रिय | दाहक-विरोधी, आसंजक-विरोधी, मेटास्टैटिक-विरोधी | |
| फोस्फोमानोपेंटानोज़ सल्फेट | हेपारनेज़ गतिविधि का शक्तिशाली अवरोधक | मेटास्टैटिक-विरोधी, एन्जियोजेनिक-विरोधी, दाहक-विरोधी | |
| चुनिंदा रासायनिक O-डीसल्फेटकृत हेपरिन | थक्का-रोधी गतिविधि का अभाव | दाहक-विरोधी, एलर्जी-विरोधी, आसंजक-विरोधी |
डी-पॉलीमेराईजेशन तकनीक[संपादित करें]
या तो रासायनिक या एंजाइमी डी-पौलीमेराईजेशन तकनीक या इन दोनों का संयोजन, संरचना और हेपरिन की क्रियाओं और हेपारन सल्फेट पर किये जाने वाले अधिकांश विश्लेषण में सन्निहित होता है।
एंजाइमी[संपादित करें]
एंजाइम जिनका परंपरागत रूप से इस्तेमाल हेपरिन या HS को पचाने के लिए होता है, वे स्वाभाविक रूप से मृदा जीवाणु पेडोबाक्टर हेपारिनस (पूर्वनाम फ्लेवोबैक्टीरियम हेपरिनम) द्वारा उत्पन्न होते हैं। [28] यह जीवाणु, या तो हेपरिन या HS को अपने एकमात्र कार्बन और नाइट्रोजन स्रोत के रूप में उपयोग करने में सक्षम है। ऐसा करने के लिए यह एंजाइमों की एक श्रृंखला का उत्पादन करता है जैसे लाइसेस, ग्लुकूरोनिडेज़, सल्फोइस्टारेज़ और सल्फामिडेज़.[29] मुख्य रूप से यह लाइसेस है जिसे हेपरिन/HS अध्ययन में प्रयोग किया जाता है। यह जीवाणु तीन लाइसेस को उत्पन्न करता है, हेपरिनेसिस I (साँचा:EC number), II (कोई EC नंबर सौंपा नहीं गया) और III (साँचा:EC number) और प्रत्येक में भिन्न सब्सट्रेट विशेषता है जैसा नीचे वर्णित है। [30][31]
| हेपरिनेज़ एंजाइम | सब्सट्रेट विशिष्टता | |
| हेपरिनेज़ I | GlcNS (±6s)-IdoA (2S) | |
| हेपरिनेज़ II | GlcNS/Ac(±6S)-IdoA(±2S) GlcNS/Ac(±6S)-GlcA | |
| हेपरिनेज़ III | GlcNS/Ac(±6S)-GlcA/IdoA (GlcA को तरजीह के साथ) |
लाइसेस, हेपरिन/HS को बीटा उन्मूलन तंत्र द्वारा खंडित करता है। यह कार्रवाई, युरोनेट अवशिष्ट के C4 और C5 के बीच एक असंतृप्त डबल बांड उत्पन्न करता है। [32][33] C4-C5 असंतृप्त युरोनेट को ΔUA या UA करार दिया गया। यह एक संवेदनशील UV क्रोमाफोर है (अधिकतम अवशोषण 232 nm) और एंजाइम पाचन की दर के पालन की अनुमति देता है साथ ही साथ एंजाइम पाचन द्वारा उत्पादित टुकड़े का पता लगाने के लिए एक सुविधाजनक तरीका प्रदान करता है।
रासायनिक[संपादित करें]
नाइट्रस एसिड को हेपरिन/HS को रासायनिक रूप से डी-पौलीमेराइज़ करने के लिए इस्तेमाल किया जा सकता है। नाइट्रस एसिड का इस्तेमाल pH 1.5 या 4 के एक उच्च pH पर किया जा सकता है। दोनों स्थितियों के तहत नाइट्रस एसिड, श्रृंखला के डीएमिनेटिव विदर को प्रभावित करता है। [34]

'उच्च' (4) और 'निम्न' (1.5) दोनों ही pH पर, डीएमिनेटिव विदर GlcNS-GlcA और GlcNS-IdoA के बीच होते हैं, सब उच्च pH में एक धीमी दर पर होते हैं। डीएमिनेशन अभिक्रिया और इसलिए श्रृंखला विदर, O-सल्फेशन का लिहाज किए बिना है जो दोनों में से किसी भी एक मोनोसैक्राइड इकाई द्वारा किया जाता है।
निम्न pH पर, डीएमिनेटिव विदर अकार्बनिक SO4 के जारी करने और GlcNS के अनहाइड्रोमनोज़ (aMan) में रूपांतरण में फलित होता है। निम्न pH नाइट्रस एसिड उपचार, N-सल्फेटकृत पौलीसैक्राइड को अलग करने में एक उत्कृष्ट तरीका है जैसे हेपरिन और HS को गैर-N-सल्फेटकृत पौलीसैक्राइड से जैसे कौड्रोइटिन सल्फेट और डर्माटन सल्फेट; कौड्रोइटिन सल्फेट और डर्माटन सल्फेट, नाइट्रस एसिड विदर के प्रति अतिसंवेदनशील हैं।
विकासवादी संरक्षण[संपादित करें]
गोजातीय और शूकरीय ऊतक के अलावा, जिसमें से फार्मास्युटिकल-ग्रेड हेपरिन को आम तौर पर निकाला जाता है, हेपरिन को निम्नलिखित प्रजातियों से भी निकाला और विशेषित किया जाता है:
6-11 प्रजातियों के भीतर हेपरिन की जैविक गतिविधि स्पष्ट नहीं है और इस विचार का आगे समर्थन करती है कि हेपरिन की मुख्य शारीरिक भूमिका, थक्का-रोधन नहीं है। इन प्रजातियों में, 1-5 में सूचीबद्ध प्रजातियों के समान किसी भी तरह की रक्त जमाव प्रणाली नहीं है। उपरोक्त सूची यह भी दर्शाती है कि कैसे हेपरिन, विभिन्न फाईला के अंतर्गत आने वाले विविध जीवों द्वारा उत्पादित समान संरचना वाले अणुओं के साथ बेहद विकासात्मक रूप से संरक्षित रही है।
अन्य उपयोग/जानकारी[संपादित करें]
- हेपरिन जेल (सामयिक) का कभी-कभी खेल चोटों के इलाज के लिए इस्तेमाल किया जा सकता है। यह ज्ञात है कि हिस्टामाइन का डिप्रोटोनेटेड रूप विशेष रूप से हेपरिन के साइट से बंधन करता है। [45] मास्ट कोशिकाओं से एक ऊतक चोट पर हिस्टामाइन के जारी होने से सूजन की प्रतिक्रिया फलित होती है। ऐसे सामयिक जेल के उपयोग के पीछे तर्क, जारी हुए हिस्टामाइन की गतिविधि को रोकना हो सकता है और इसलिए सूजन को कम करने में मदद हो सकती है।
- जब इसका ताम्बा नमक बनता है तो हेपरिन को एन्जियोजिनेसिस शुरू करने के लिए क्षमता का लाभ होता है। तांबा-मुक्त अणु, गैर-एन्जियोजेनिक हैं। [46][47] इसके विपरीत, हेपरिन एन्जियोजिनेसिस को रोक सकता है यदि इसे कोर्टिकोस्टेरोइड की उपस्थिति में प्रदान किया जाए.[48] यह एन्जियोजेनिक-विरोधी प्रभाव, हेपरिन के थक्का-रोधी गतिविधि से स्वतंत्र है। [49]
- टेस्ट ट्यूब, वैक्यूटेनर और केशिका ट्यूब जो थक्का-रोधी के रूप में हेपरिन के लिथियम नमक (लिथियम हेपरिन) का उपयोग करते हैं, आम तौर पर हरे रंग के स्टिकर और हरे रंग टॉप्स के साथ चिह्नित होते हैं। EDTA की तुलना में हेपरिन लाभ की स्थिति में है क्योंकि यह अधिकांश आयन के स्तर को प्रभावित नहीं करता है। हालांकि, यह दिखाया गया है कि आयनीकृत कैल्शियम का स्तर नीचे गिर सकता है यदि रक्त के नमूने में हेपरिन की संकेद्रता अत्यधिक उच्च हो। [50] हालांकि, हेपरिन, प्रतिरक्षा आमापन के साथ कुछ हस्तक्षेप कर सकता है। चूंकि आम तौर पर लिथियम हेपरिन का प्रयोग किया जाता है, एक व्यक्ति के लिथियम स्तर को इन नलियों से प्राप्त नहीं किया जा सकता है; इस उद्देश्य के लिए ऊपर से रॉयल-ब्लू वाले सोडियम हेपरिन युक्त वैक्यूटेनर का प्रयोग किया जाता है।
- हेपरिन-लेपित रक्त ऑक्सिजनेटर, फेफड़े-हृदय की मशीनों में इस्तेमाल के लिए उपलब्ध हैं। अन्य बातों के अलावा, माना जाता है ये विशेष ऑक्सिजनेटर समग्र जैविकअनुकूलता में सुधार करते हैं और देशी इंडोथेलिअम के समान विशेषताएं प्रदान करके होमिओस्टेसिस होस्ट करते हैं।
- RNA पॉलीमरेज़ पर DNA बाइंडिंग साइटों पर हेपरिन द्वारा कब्जा किया जा सकता है और प्रमोटर DNA के लिए पोलीमरेज़ बाइंडिंग को रोका जा सकता है। इस गुण को आणविक जैविक परीक्षणों की एक श्रृंखला में दोहन किया जाता है।
- आम नैदानिक प्रक्रियाओं में एक रोगी के DNA की PCR प्रवर्धन की आवश्यकता होती है, जिसे आसानी से हेपरिन उपचारित श्वेत रुधिर कोशिका से निकाला जाता है। यह एक संभावित खतरे को पैदा करता है, चूंकि हेपरिन को DNA के साथ निकाला जा सकता है और इसे PCR अभिक्रिया के साथ 50 μL अभिक्रिया मिश्रण में 0.002 U के निम्न स्तर तक हस्तक्षेप करते पाया गया है। [51]
- अप्रयुक्त हेपरिन को प्रोटीन शोधन में करीबी लिगेंड के रूप में इस्तेमाल किया जा सकता है। अप्रयुक्त हेपरिन का स्वरूप व्यापक रूप से भिन्न हो सकता है जो नैदानिक प्रयोजनों के लिए लेपित प्लास्टिक सतहों से लेकर क्रोमैटोग्राफी रेजिन तक हो सकता है। अप्रयुक्त हेपरिन के अधिकांश प्रकार को तीन तरीकों से इस्तेमाल किया जा सकता है। पहला है हेपरिन का इस्तेमाल विशिष्ट जमावट कारक को खोजने के लिए करना, या गैर-हेपरिन-बाइंडिंग प्रोटीन से अन्य प्रकार के हेपरिन-बाइंडिंग प्रोटीन को खोजना. विशिष्ट प्रोटीन को तब चयनात्मक रूप से हेपरिन से अलग किया जा सकता है जिसके लिए नमक की विभिन्न सांद्रता या नमक प्रवणता का इस्तेमाल किया जा सकता है। दूसरा उपयोग है हेपरिन का एक उच्च क्षमता धनायन एक्सचेंजर के रूप में इस्तेमाल. यह उपयोग, हेपरिन के अनिओनिक सल्फेट समूहों की उच्च संख्या का लाभ लेता है। ये समूह एक समग्र धनात्मक चार्ज वाले अणु या प्रोटीन पर कब्जा करते है, यानी जो जमाव में कोई भूमिका नहीं निभाते हैं और न्युक्लियोटाइड्स को नहीं बांधते. अप्रयुक्त हेपरिन का तीसरा उपयोग है RNA और DNA बाइंडिंग प्रोटीन का समूह-विशिष्ट शुद्धीकरण जैसे प्रतिलेखन कारक और/या वायरस कोट प्रोटीन. यह पद्धति, RNA और DNA से हेपरिन की समानता का लाभ लेती है, क्योंकि वह एक ऋणात्मक चार्ज वाली शर्करा-युक्त स्थूलअणु है।
- हेपरिन, फाइब्रिन को तोड़ती नहीं है, यह केवल फाइब्रिनोजेन के फाइब्रिन में रूपांतरण को रोकती है। केवल थ्रोम्बोलाइटिक्स एक थक्का को तोड़ सकता है।
संदूषण वापसी[संपादित करें]
दिसंबर 2007 में, US फूड एंड ड्रग एडमिनिस्ट्रेशन (FDA) ने हेपरिन के एक लदान को वापस बुला लिया, क्योंकि इस उत्पाद के कई बंद सिरिंजों में बैक्टीरिया का विकास (सेराटिया मार्सेसीन) हो चुका था। यह बैक्टीरिया, सेराटिया मार्सेसीन जीवन के लिए घातक चोटों और/या मृत्यु को फलित कर सकता है। [52]
मार्च 2008 में, FDA ने चीन से आयात किए गए कच्चे हेपरिन के भण्डार के संदूषण के कारण हेपरिन की प्रमुख वापसियों की घोषणा की। [53][54] FDA के अनुसार दूषित हेपरिन ने संयुक्त राज्य अमेरिका में 81 लोगों को मार दिया। संदूषक को कॉनड्रॉइटिन सल्फेट के "अति-सल्फेटकृत" व्युत्पन्न के रूप में पहचाना गया, शेलफिश से निकाला जाने वाला एक लोकप्रिय पूरक जिसका इस्तेमाल गठिया के लिए किया जाता था। [55]
अवैध उपयोग[संपादित करें]
मानव हत्या में प्रयोग[संपादित करें]
2006 में, पेटर ज़ेलेंका, चेक गणराज्य में एक नर्स ने जानबूझकर रोगियों को इसकी अधिक खुराक दे दी, जिससे 7 की मृत्यु हो गई और उसने अन्य 10 को मारने का प्रयास किया। [56]
अधिमात्रा मुद्दे[संपादित करें]
2007 में, सेडर्स-सिनाई मेडिकल सेंटर में एक नर्स ने अभिनेता डेनिस क्वेड के बारह दिन के जुड़वां शिशुओं को हेपरिन की एक खुराक दे दी, जो शिशुओं के लिए निर्धारित खुराक से 1,000 गुना अधिक थी। [57] यह अधिमात्रा, कथित तौर पर इसलिए दे दी गई क्योंकि उत्पाद के वयस्क और शिशु संस्करण की लेबलिंग और डिज़ाइन समान थे। क्वेड परिवार ने बाद में निर्माता, बैक्सटर हेल्थकेयर कार्पोरेशन पर मुकदमा दायर कर दिया,[58][59] और अस्पताल के साथ $750,000 पर सुलह की। [60] क्वेड की दुर्घटना से पहले, इंडियानापोलिस, इंडियाना में मेथोडिस्ट अस्पताल में छः नवजात शिशुओं को इसकी अधिमात्रा दी गई। इस गलती से तीन बच्चों की मृत्यु हो गई। [61]
जुलाई 2008 में, कॉर्पस क्रिस्टी, टेक्सास में स्थित क्रिस्टस स्पोन हॉस्पिटल साउथ में जन्मे जुड़वां बच्चे गलती से दी गई इस दवा की अधिमात्रा से मर गए। यह अधिमात्रा अस्पताल की फार्मेसी में मिश्रण में हुई एक त्रुटि के कारण थी और यह उत्पाद की पैकेजिंग या लेबलिंग से असंबंधित थी। [62]जुलाई 2008 के अनुसार [update], कि ये मौतें अधिमात्रा के कारण थीं या नहीं यह जांच के अधीन है। [63][64]
मार्च 2010 को, टेक्सास के एक दो वर्षीय प्रत्यारोपण रोगी को यूनिवर्सिटी ऑफ़ नेब्रास्का मेडिकल सेंटर में हेपरिन की एक घातक खुराक दी गई। उसकी मौत के आस-पास मंडराते सटीक हालात अभी भी जांच के विषय हैं। [65]
विष विज्ञान[संपादित करें]
खतरे का संकेत: रक्तस्राव का खतरा (विशेष रूप से अनियंत्रित रक्तचाप, जिगर की बीमारी और स्ट्रोक वाले रोगियों में), गंभीर जिगर की बीमारी, गंभीर उच्च रक्तचाप.
पार्श्व-प्रभाव: रक्तस्राव, थ्रोम्बोसाइटोपेनिया, पोटेशियम का वर्धित स्तर और गठिया
कम्पेंडियल स्थिति[संपादित करें]
| इस अनुभाग को विस्तार की ज़रूरत है। |
नोट और संदर्भ[संपादित करें]
- ↑ अ आ Cox, M. (2004). Lehninger, Principles of Biochemistry. Freeman. पृ॰ 1100. आई॰ऍस॰बी॰ऍन॰ 0-71674339-6. नामालूम प्राचल
|coauthors=की उपेक्षा की गयी (|author=सुझावित है) (मदद) - ↑ Linhardt RJ, Gunay NS. (1999). "Production and Chemical Processing of Low Molecular Weight Heparins". Sem. Thromb. Hem. 3: 5–16. PMID 10549711.
- ↑ Marcum JA, McKenney JB.; एवं अन्य (1986). "Anticoagulantly active heparin-like molecules from mast cell-deficient mice". Am. J. Physiol. 250 (5 Pt 2): H879–888. PMID 3706560. Explicit use of et al. in:
|author=(मदद) - ↑ Nader, HB; एवं अन्य (1999). "Heparan sulfates and heparins: similar compounds performing the same functions in vertebrates and invertebrates?". Braz. J. Med. Biol. Res. 32 (5): 529–538. PMID 10412563. डीओआइ:10.1590/S0100-879X1999000500005. Explicit use of et al. in:
|author=(मदद) - ↑ Francis CW, Kaplan KL (2006). "Chapter 21. Principles of Antithrombotic Therapy". प्रकाशित Lichtman MA, Beutler E, Kipps TJ; एवं अन्य (संपा॰). Williams Hematology (7th संस्करण). आई॰ऍस॰बी॰ऍन॰ 978-0071435918. मूल से 2 अक्तूबर 2019 को पुरालेखित. अभिगमन तिथि 23 अक्तूबर 2019. Explicit use of et al. in:
|editor=(मदद)सीएस1 रखरखाव: एक से अधिक नाम: editors list (link) - ↑ Bentolila, A.; एवं अन्य. "Synthesis and heparin-like biological activity of amino acid-based polymers". Wiley InterScience. मूल (Subscription required) से 8 फ़रवरी 2016 को पुरालेखित. अभिगमन तिथि 2008-03-10. Explicit use of et al. in:
|first=(मदद) - ↑ Gatti, G., Casu, B.; एवं अन्य (1979). "Studies on the Conformation of Heparin by lH and 13C NMR Spectroscopy" (PDF). Macromolecules. 12 (5): 1001–1007. डीओआइ:10.1021/ma60071a044. Explicit use of et al. in:
|author=(मदद)सीएस1 रखरखाव: एक से अधिक नाम: authors list (link)[मृत कड़ियाँ] - ↑ "Online Medical Dictionary". Centre for Cancer Education. 2000. मूल से 13 अगस्त 2007 को पुरालेखित. अभिगमन तिथि 2008-07-11.
- ↑ Ferro D, Provasoli A; एवं अन्य (1990). "Conformer populations of L-iduronic acid residues in glycosaminoglycan sequences". Carbohydr. Res. 195 (2): 157–167. PMID 2331699. डीओआइ:10.1016/0008-6215(90)84164-P. Explicit use of et al. in:
|author=(मदद) - ↑ Mulloy B, Forster MJ, Jones C, Davies DB. (1 जनवरी 1993). "NMR and molecular-modelling studies of the solution conformation of heparin". Biochem. J. 293 (Pt 3): 849–858. PMID 8352752. पी॰एम॰सी॰ 1134446.सीएस1 रखरखाव: एक से अधिक नाम: authors list (link)
- ↑ Guyton, A. C. (2006). Textbook of Medical Physiology. Elsevier Saunders. पृ॰ 464. आई॰ऍस॰बी॰ऍन॰ 0-7216-0240-1. नामालूम प्राचल
|coauthors=की उपेक्षा की गयी (|author=सुझावित है) (मदद) - ↑ Agnelli G, Piovella F, Buoncristiani P; एवं अन्य (1998). "Enoxaparin plus compression stockings compared with compression stockings alone in the prevention of venous thromboembolism after elective neurosurgery". N Engl J Med. 339 (2): 80–5. PMID 9654538. डीओआइ:10.1056/NEJM199807093390204. Explicit use of et al. in:
|author=(मदद)सीएस1 रखरखाव: एक से अधिक नाम: authors list (link) - ↑ Bergqvist D, Agnelli G, Cohen AT; एवं अन्य (2002). "Duration of prophylaxis against venous thromboembolism with enoxaparin after surgery for cancer". N Engl J Med. 346 (13): 975–980. PMID 11919306. डीओआइ:10.1056/NEJMoa012385. मूल से 5 जनवरी 2010 को पुरालेखित. अभिगमन तिथि 30 जून 2010. Explicit use of et al. in:
|author=(मदद)सीएस1 रखरखाव: एक से अधिक नाम: authors list (link) - ↑ Handoll HHG, Farrar MJ, McBirnie J, Tytherleigh-Strong G, Milne AA, Gillespie WJ (2002). "Heparin, low molecular weight heparin and physical methods for preventing deep vein thrombosis and pulmonary embolism following surgery for hip fractures". Cochrane Database Syst Rev. 4 (4): CD000305. PMID 12519540. डीओआइ:10.1002/14651858.CD000305.सीएस1 रखरखाव: एक से अधिक नाम: authors list (link)
- ↑ Chuang YJ, Swanson R.; एवं अन्य (2001). "Heparin enhances the specificity of antithrombin for thrombin and factor Xa independent of the reactive center loop sequence. Evidence for an exosite determinant of factor Xa specificity in heparin-activated antithrombin". J. Biol. Chem. 276 (18): 14961–14971. PMID 11278930. डीओआइ:10.1074/jbc.M011550200. Explicit use of et al. in:
|author=(मदद) - ↑ Bjork I, Lindahl U. (1982). "Mechanism of the anticoagulant action of heparin". Mol. Cell. Biochem. 48 (3): 161–182. PMID 6757715. डीओआइ:10.1007/BF00421226. मूल से 11 अप्रैल 2020 को पुरालेखित. अभिगमन तिथि 30 जून 2010.
- ↑ Petitou M, Herault JP, Bernat A, Driguez PA; एवं अन्य (1999). "Synthesis of Thrombin inhibiting Heparin mimetics without side effects". Nature. 398 (6726): 417–422. PMID 10201371. डीओआइ:10.1038/18877. Explicit use of et al. in:
|author=(मदद)सीएस1 रखरखाव: एक से अधिक नाम: authors list (link) - ↑ शालान्सकी, करेन. DANAPAROID (Orgaran) for Heparin-Induced Thrombocytopenia. Archived 2017-06-22 at the वेबैक मशीन वैंकूवर अस्पताल और स्वास्थ्य विज्ञान केन्द्र, फ़रवरी 1998 औषधि एवं चिकित्सा न्यूज़लैटर. 8 जनवरी 2007 को पुनःप्राप्त.
- ↑ Hirsh J, Raschke R (2004). "Heparin and low-molecular-weight heparin: the Seventh ACCP Conference on Antithrombotic and Thrombolytic Therapy". Chest. 126 (3 Suppl): 188S–203S. PMID 15383472. डीओआइ:10.1378/chest.126.3_suppl.188S.
- ↑ Kusmer, Ken (20 सितंबर 2006). "3rd Ind. preemie infant dies of overdose". Fox News (Associated Press). मूल से 18 अक्तूबर 2007 को पुरालेखित. अभिगमन तिथि 2007-01-08.
- ↑ आंतरिक चिकित्सा, जे एच स्टेंन, 635 पृष्ठ
- ↑ Linhardt RJ. (1991). "Heparin: An important drug enters its seventh decade". Chem. Indust. 2: 45–50.
- ↑ Jorpes E (1935). "The chemistry of heparin". The Biochemical Journal. 29 (8): 1817–30. PMID 16745848. पी॰एम॰सी॰ 1266692. नामालूम प्राचल
|month=की उपेक्षा की गयी (मदद) - ↑ Rutty, CJ. "Miracle Blood Lubricant: Connaught and the Story of Heparin, 1928–1937". Health Heritage Research Services. मूल से 23 अगस्त 2007 को पुरालेखित. अभिगमन तिथि 2007-05-21.
- ↑ Marcum JA (2000). "The origin of the dispute over the discovery of heparin". Journal of the History of Medicine and Allied Sciences. 55 (1): 37–66. PMID 10734720. मूल से 30 मई 2020 को पुरालेखित. अभिगमन तिथि 30 जून 2010. नामालूम प्राचल
|month=की उपेक्षा की गयी (मदद) - ↑ अ आ Lever R. and Page C.P. (2002). "Novel drug opportunities for heparin". Nat. Rev. Drug Discov. 1 (2): 140–148. PMID 12120095. डीओआइ:10.1038/nrd724.
- ↑ Coombe D.R. and Kett W.C. (2005). "Heparan sulfate-protein interactions: therapeutic potential through structure-function insights". Cell. Mol. Life Sci. 62 (4): 410–424. PMID 15719168. डीओआइ:10.1007/s00018-004-4293-7.
- ↑ Shaya D, Tocilj A.; एवं अन्य (2006). "Crystal structure of heparinase II from Pedobacter heparinus and its complex with a disaccharide product". J. Biol. Chem. 281 (22): 15525–15535. PMID 16565082. डीओआइ:10.1074/jbc.M512055200. Explicit use of et al. in:
|author=(मदद) - ↑ Galliher PM, Cooney CL.; एवं अन्य (1981). "Heparinase production by Flavobacterium heparinum". Appl. Environ. Microbiol. 41 (2): 360–365. PMID 7235692. पी॰एम॰सी॰ 243699. Explicit use of et al. in:
|author=(मदद) - ↑ Linhardt RJ, Turnbull JE.; एवं अन्य (1990). "Examination of the substrate specificity of heparin and heparan sulfate lyases". Biochemistry. 29 (10): 2611–2617. PMID 2334685. डीओआइ:10.1021/bi00462a026. Explicit use of et al. in:
|author=(मदद) - ↑ Desai UR, Wang HM. and Linhardt RJ. (1993). "Specificity studies on the heparin lyases from Flavobacterium heparinum". Biochemistry. 32 (32): 8140–8145. PMID 8347612. डीओआइ:10.1021/bi00083a012.
- ↑ Linker A, Hovingh P. (1972). "Isolation and characterization of oligosaccharides obtained from heparin by the action of heparinase". Biochemistry. 11 (4): 563–568. PMID 5062409. डीओआइ:10.1021/bi00754a013.
- ↑ Linhardt RJ, Rice KG.; एवं अन्य (1988). "Mapping and quantification of the major oligosaccharide components of heparin". Biochem. J. 254 (3): 781–787. PMID 3196292. पी॰एम॰सी॰ 1135151. Explicit use of et al. in:
|author=(मदद) - ↑ Shively JE, Conrad HE. (1976). "Formation of anhydrosugars in the chemical depolymerization of heparin". Biochemistry. 15 (18): 3932–3942. PMID 9127. डीओआइ:10.1021/bi00663a005.
- ↑ Warda M, Mao W.; एवं अन्य (2003). "Turkey intestine as a commercial source of heparin? Comparative structural studies of intestinal avian and mammalian glycosaminoglycans". Comp. Biochem. Physiol. B Biochem. Mol. Biol. 134 (1): 189–197. PMID 12524047. डीओआइ:10.1016/S1096-4959(02)00250-6. Explicit use of et al. in:
|author=(मदद) - ↑ Ototani N, Kikuchi M, Yosizawa Z. (1981). "Comparative studies on the structures of highly-active and relatively-inactive forms of whale heparin". J Biochem (Tokyo). 90 (1): 241–246. PMID 7287679.सीएस1 रखरखाव: एक से अधिक नाम: authors list (link)
- ↑ Warda M, Gouda EM.; एवं अन्य (2003). "Isolation and characterization of raw heparin from dromedary intestine: evaluation of a new source of pharmaceutical heparin". Comp. Biochem. Physiol. C Toxicol. Pharmacol. 136 (4): 357–365. PMID 15012907. डीओआइ:10.1016/j.cca.2003.10.009. Explicit use of et al. in:
|author=(मदद) - ↑ Bland CE, Ginsburg H.; एवं अन्य (1982). "Mouse heparin proteoglycan. Synthesis by mast cell-fibroblast monolayers during lymphocyte-dependent mast cell proliferation". J. Biol. Chem. 257 (15): 8661–8666. PMID 6807978. Explicit use of et al. in:
|author=(मदद) - ↑ Linhardt RJ, Ampofo SA.; एवं अन्य (1992). "Isolation and characterization of human heparin". Biochemistry. 31 (49): 12441–12445. PMID 1463730. डीओआइ:10.1021/bi00164a020. Explicit use of et al. in:
|author=(मदद) - ↑ Hovingh P, Linker A. (1982). "An unusual heparan sulfate isolated from lobsters (Homarus americanus)". J. Biol. Chem. 257 (16): 9840–9844. PMID 6213614.
- ↑ Hovingh P, Linker A. (1993). "Glycosaminoglycans in Anodonta californiensis, a freshwater mussel". Biol. Bull. 185 (2): 263–276. डीओआइ:10.2307/1542006. मूल से 16 जून 2011 को पुरालेखित. अभिगमन तिथि 30 जून 2010.
- ↑ Pejler G, Danielsson A.; एवं अन्य (1987). "Structure and antithrombin-binding properties of heparin isolated from the clams Anomalocardia brasiliana and Tivela mactroides". J. Biol. Chem. 262 (24): 11413–11421. PMID 3624220. Explicit use of et al. in:
|author=(मदद) - ↑ Dietrich CP, Paiva JF.; एवं अन्य (1999). "Structural features and anticoagulant activities of a novel natural low-molecular-weight heparin from the shrimp Penaeus brasiliensis". Biochim. Biophys. Acta. 1428 (2–3): 273–283. PMID 10434045. Explicit use of et al. in:
|author=(मदद) - ↑ अ आ Medeiros GF, Mendes, A.; एवं अन्य (2000). "Distribution of sulfated glycosaminoglycans in the animal kingdom: widespread occurrence of heparin-like compounds in invertebrates". Biochim. Biophys. Acta. 1475 (3): 287–294. PMID 10913828. Explicit use of et al. in:
|author=(मदद)सीएस1 रखरखाव: एक से अधिक नाम: authors list (link) - ↑ Chuang W, Christ MD, Peng J, Rabenstein DL. (2000). "An NMR and molecular modeling study of the site-specific binding of histamine by heparin, chemically-modified heparin, and heparin-derived oligosacchrides". Biochemistry. 39 (13): 3542–3555. PMID 10736153. डीओआइ:10.1021/bi9926025.सीएस1 रखरखाव: एक से अधिक नाम: authors list (link)
- ↑ Alessandri, G. Raju, K. and Gullino, PM. (1983). "Mobilization of capillary endothelium in-vitro induced by effectors of angiogenesis in-vivo". Cancer. Res. 43 (4): 1790–1797. PMID 6187439.सीएस1 रखरखाव: एक से अधिक नाम: authors list (link)
- ↑ Raju, K. Alessandri, G. Ziche, M. and Gullino, PM. (1982). "Ceruloplasmin, copper ions, and angiogenesis". J. Natl. Cancer. Inst. 69 (5): 1183–1188. PMID 6182332.सीएस1 रखरखाव: एक से अधिक नाम: authors list (link)
- ↑ Folkman J. (1985). "Regulation of angiogenesis: a new function of heparin". Biochem. Pharmacol. 34 (7): 905–909. PMID 2580535. डीओआइ:10.1016/0006-2952(85)90588-X.
- ↑ Folkman J. and Ingber DE. (1987). "Angiostatic steroids. Method of discovery and mechanism of action". Ann. Surg. 206 (3): 374–383. PMID 2443088. डीओआइ:10.1097/00000658-198709000-00016. पी॰एम॰सी॰ 1493178.
- ↑ Higgins, C. (2007). "The use of heparin in preparing samples for blood-gas analysis" (PDF). Medical Laboratory Observer. मूल (PDF) से 7 अक्तूबर 2011 को पुरालेखित. अभिगमन तिथि 30 जून 2010. नामालूम प्राचल
|month=की उपेक्षा की गयी (मदद) - ↑ Yokota M, Tatsumi N, Nathalang O, Yamada T, Tsuda I. (1999). "Effects of Heparin on Polymerase Chain Reaction for Blood White Cells". J. Clin. Lab. Anal. 13 (3): 133–140. PMID 10323479. डीओआइ:10.1002/(SICI)1098-2825(1999)13:3<133::AID-JCLA8>3.0.CO;2-0.सीएस1 रखरखाव: एक से अधिक नाम: authors list (link)
- ↑ AM2 PAT, Inc. Issues Nationwide Recall of Pre-Filled Heparin Lock Flush Solution USP (5 mL in 12 mL Syringes), Archived 2007-12-23 at the वेबैक मशीन, Am2pat, Inc प्रेस विज्ञप्ति, दिसम्बर 20, 2007 [not in citation given]
- ↑ CBS समाचार, Blood-thinning drug under suspicion Archived 2013-05-17 at the वेबैक मशीन
- ↑ FDA informational page Archived 2018-04-25 at the वेबैक मशीन FDA जांच के बारे में सूचना और लिंक.
- ↑ Zawisza, Julie (29 मार्च 2008). "FDA Media Briefing on Heparin" (PDF). U.S. Food and Drug Administration. मूल (PDF) से 4 नवंबर 2008 को पुरालेखित. अभिगमन तिथि 2008-04-23.
- ↑ Nurse committed murders to "test" doctors, Archived 2010-04-10 at the वेबैक मशीन, रेडियो प्राहा, 12 मई 2006
- ↑ ओर्नस्टेंन, चार्ल्स; गोर्मन, अन्ना. (21 नवम्बर 2007) लॉस एंजेल्स टाइम्स [[Report: Dennis Quaid's twins get accidental overdose|Report: Dennis Quaid's twins get accidental overdose[मृत कड़ियाँ]]]
- ↑ Dennis Quaid and wife sue drug maker Archived 2010-06-28 at the वेबैक मशीन, USA टुडे, 4 दिसम्बर 2007
- ↑ Dennis Quaid files suit over drug mishap, Archived 2012-02-19 at the वेबैक मशीन, लॉस एंजिल्स टाइम्स, 5 दिसम्बर 2007
- ↑ Quaid Awarded $750,000 Over Hospital Negligence Archived 2009-04-15 at the वेबैक मशीन, SFGate.com, 16 दिसम्बर 2008
- ↑ WTHR story Archived 2011-06-29 at the वेबैक मशीन मेथोडिस्ट अस्पताल अधिमात्रा के बारे में
- ↑ Statement by Dr. Richard Davis, Chief Medical Officer, CHRISTUS Spohn Health System,[मृत कड़ियाँ], 10 जुलाई 2008
- ↑ At a Glance Heparin Overdose at Hospital Archived 2008-10-25 at the वेबैक मशीन, डलास मॉर्निंग समाचार, 11 जुलाई. 2008
- ↑ "Officials Investigate Infants' Heparin OD at Texas Hospital. Archived 2017-09-11 at the वेबैक मशीन" ABC न्यूज. 11 जुलाई 2008. 24 जुलाई 2008 को पुनःप्राप्त.
- ↑ " Heparin Overdose Kills Toddler At Hospital, Staff Investigated. Archived 2018-09-20 at the वेबैक मशीन" "KETV ओमाहा." 31 मार्च 2010
इन्हें भी देखें[संपादित करें]
बाहरी कड़ियाँ[संपादित करें]
- लेख जिनमें मार्च 2010 से मृत कड़ियाँ हैं
- स्रोतहीन कथनों वाले सभी लेख मार्च 2010
- लेख जिन्हें अप्रैल 2010 से अतिरिक्त संदर्भ की आवश्यकता है
- लेख जिनमें अप्रैल 2010 से असत्यापित तथ्य हैं
- लेख जिन्हें अप्रैल 2010 से विस्तार की आवश्यकता है
- लेख जिनमें संभावित तिथि के आंकड़े प्रयोग हुए हैं-जुलाई 2008
- ग्लाइकोसमिनोग्लाइकन्स
- हेपरिन