"ऊष्माक्षेपी अभिक्रिया": अवतरणों में अंतर
Content deleted Content added
रोहित साव27 (वार्ता | योगदान) InternetArchiveBot के अवतरण 4820168पर वापस ले जाया गया : Reverted (ट्विंकल) टैग: किए हुए कार्य को पूर्ववत करना |
परिभाषा टैग: Reverted मोबाइल संपादन मोबाइल वेब संपादन |
||
| पंक्ति 11: | पंक्ति 11: | ||
H+ + OH- H2O |
H+ + OH- H2O |
||
वैसी रासायनिक अभिक्रिया जिसमे कोई पदार्थ टूटकर दो या दो से अधिक पदार्थो में टूट जाता है तथा उसमें उत्पाद के रूप में ऊर्जा प्रदान करता है उसे उसमच्छेपी अभिक्रिया कहते है। |
|||
== सन्दर्भ == |
|||
{{टिप्पणीसूची}} |
|||
== बाहरी कड़ियाँ == |
== बाहरी कड़ियाँ == |
||
09:25, 30 जनवरी 2021 का अवतरण
| यह लेख एक आधार है। जानकारी जोड़कर इसे बढ़ाने में विकिपीडिया की मदद करें। |
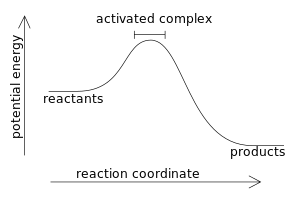
वह रासायनिक अभिक्रिया उष्माक्षेपी (exothermic reaction) कहलाती है जिसमें उष्मा के रूप में उर्जा प्राप्त होती है। इसके विपरीत रासायनिक अभिक्रिया उष्माशोषी कहलाती है। रासायनिक अभिक्रिया के रूप में व्यक्त करने पर -
- अभिकारक → उत्पाद + उर्जा (उष्मा के रूप में)
उदाहरण के लिए, हाइड्रोजन का जलना एक ऊष्माक्षेपी अभिक्रिया है।
- 2H2 (g) + O2 (g) → 2H2O (g)
- ΔH = −483.6 kJ/mol of O2[1]
Example- emission of light H+ + OH- H2O
वैसी रासायनिक अभिक्रिया जिसमे कोई पदार्थ टूटकर दो या दो से अधिक पदार्थो में टूट जाता है तथा उसमें उत्पाद के रूप में ऊर्जा प्रदान करता है उसे उसमच्छेपी अभिक्रिया कहते है।
बाहरी कड़ियाँ
- ↑ "संग्रहीत प्रति". मूल से 8 जुलाई 2013 को पुरालेखित. अभिगमन तिथि 5 सितंबर 2013.
