"ऊष्माक्षेपी अभिक्रिया": अवतरणों में अंतर
Content deleted Content added
टैग: मोबाइल संपादन मोबाइल वेब संपादन |
2405:204:120D:1216:2462:483D:68DA:E320 (वार्ता) द्वारा किए बदलाव 3705536 को पूर्... टैग: किए हुए कार्य को पूर्ववत करना |
||
| पंक्ति 14: | पंक्ति 14: | ||
== बाहरी कड़ियाँ == |
== बाहरी कड़ियाँ == |
||
* [http://www.gcsescience.com/rc24.htm GCSE Science: Reactions] |
* [http://www.gcsescience.com/rc24.htm GCSE Science: Reactions] |
||
[[श्रेणी:उष्मारसायन]] |
[[श्रेणी:उष्मारसायन]] |
||
02:02, 10 फ़रवरी 2018 का अवतरण
| यह लेख एक आधार है। जानकारी जोड़कर इसे बढ़ाने में विकिपीडिया की मदद करें। |
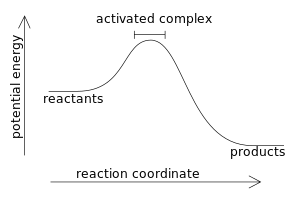
वह रासायनिक अभिक्रिया उष्माक्षेपी (exothermic reaction) कहलाती है जिसमें उष्मा के रूप में उर्जा प्राप्त होती है। इसके विपरीत रासायनिक अभिक्रिया उष्माशोषी कहलाती है। रासायनिक अभिक्रिया के रूप में व्यक्त करने पर -
- अभिकारक → उत्पाद + उर्जा (उष्मा के रूप में)
उदाहरण के लिए, हाइड्रोजन का जलना एक ऊष्माक्षेपी अभिक्रिया है।
- 2H2 (g) + O2 (g) → 2H2O (g)
- ΔH = −483.6 kJ/mol of O2[1]
