रसायन विज्ञान की शब्दावली
रसायन विज्ञान के प्रयोग रासायन शास्त्र की शब्दावली में रसायन विज्ञान से सम्बंधित कुछ शब्दों और परिभाषाओं की सूची है जिसमें रासायनिक नियम, चित्र एवं सूत्र, प्रयोगशाला उपकरण, शीशे के बर्तन और अन्य उपकरण शामिल हैं। रसायन विज्ञान पदार्थ के गुणधर्मों, संरचना एवं संयोजन के साथ-साथ किसी रासायनिक अभिक्रिया के दौरान इसमें होने वाले परिवर्तनों का अध्ययन करने वाला विज्ञान है। इसमें बड़ी मात्रा में पारिभाषिक शब्द और पर्याप्त मात्रा में शब्दजाल शामिल है।
नोट: आवर्त सारणी के सभी संदर्भ आईयूपीएसी की आवर्त सारणी की शैली को संदर्भित करते हैं।
स्वर से आरम्भ होने वाले[संपादित करें]
- अकाइरल (achiral)
- (अणु के) वे ज्यामितिय गुण जो उसके दर्पण प्रतिबिम्ब पर अध्यारोपणीय हो; काइरलता का अभाव।
- अकार्बनिक रसायन (inorganic chemistry)
- रसायन विज्ञान की वह शाखा जिसमें अकार्बनिक यौगिकों की अभिक्रिया और रासायनिक गुणधर्मों का अध्ययन किया जाता है। अकार्बनिक रसायन का विलोम।
- अक्रिय (inert)
- वह पदार्थ जो रासायनिक क्रिया न करे या बहुत कठ्नाई से रासायनिक क्रिया करे।
- अचक्रीय (acyclic)
- परमाणुओं की केवल रैखिक संरचना वाले यौगिक (विशेषतः हाइड्रोकार्बन में)।
- अंचल गलन (zone melting)
- किसी तत्व से अशुद्धता हटाने के लिए इसको पिघलाकर धीरे-धीरे सिलिका से निकालने की एक विधि।
- अकार्बनिक यौगिक (inorganic compound)
- वे रासायनिक यौगिक जिनमें कार्बन नहीं हो। यद्यपि इसके अपवाद भी होते हैं। कार्बनिक यौगिक के विपरीत।
- अणु (अणु)
- कुछ परमाणुओं के रासायनिक आबंधों से बनी वैद्युत रूप से उदासीन संरचना।
- अणु भार (molecular weight)
- अणुसंख्य गुणधर्म (colligative property)
- विलयन के वे गुण जो विलयन में विलय और विलायक के कणों की संख्या के अनुपात पर निर्भर करता है, और उपस्थित रासायनिक जाति की प्रकृति पर निर्भर नहीं करते। उदाहरण के लिये परासरण दाब, हिमांक अवनमन और क्वथनांक उन्नयन आदि अणुसंख्य गुणधर्म हैं।
- अंतःअणुक बल (intramolecular force)
- अंतराअणुक बल (intermolecular force)
- अधातु (non-metal)
- कोई भी रासायनिक तत्व जो धातु नहीं हो।
- अधिशोषण (adsorption)
- किसी पदार्थ (या तो गैस, द्रव या फिर घुला हुआ ठोस) के परमाणुओं, आयनों अथवा अणुओं का अन्य पदार्थ की सतह पर रासायनिक आसंजन जो पहले पदार्थ की झिल्ली अथवा फ़िल्म के रूप में परिणत हो और दोनों पदार्थों के मध्य दुर्बलता से बंधा हो। अधिशोषण अवशोषण से इस तरह भिन्न होता है कि यह अनन्य रूप से सतही घटना है जबकि अवशोषण में द्रव्य का पूर्ण आयतन शामिल होता है।
- अध्रुवी यौगिक (nonpolar compound)
- सहसंयोजी अणुओं वाला यौगिक जिसका कोई भी स्थायी द्विध्रुव आघूर्ण नहीं होता।[1]
- अनिश्चितता (uncertainty)
- वो धारणा जिसके अनुसार किसी मापन में किसी मात्रा का आकलन पुनरुत्पादनीय नहीं होता।
- अनिश्चितता सिद्धान्त (uncertainty principle)
- किसी कण की स्थिति को जानने पर इसका संवेग अनिश्चित हो जाता है जबकि कण के संवेग को जानने पर इसकी स्थिति अनिश्चित हो जाती है।
- अनुक्रमी तनूकरण (serial dilution)
- अनुनाद (resonance)
- अनुमापन (titration)
- मात्रात्मक रासायनिक विश्लेषण की प्रयोगशाला विधि जो परिचित विश्लेष्य की सान्द्रता को ज्ञात करने के काम आता है। यह प्रक्रिया ज्ञात सान्द्रता एवं आयतन के मानक विलयन के विशिष्ट अभिकारक को तैयार करने को शामिल करता है (इसे अनुमाप अथवा अनुमापक कहते हैं) तथा इसे किसी विश्लेष्य के विलयन (इसे अनुमापक कहते हैं) के साथ अभिक्रिया को अनुमत करता है जिससे बाद में सान्द्रता ज्ञात की जाती है।
- अनुमापी-फ्लास्क (volumetric flask)
- अन्तरराष्ट्रीय मात्रक प्रणाली (International System of Units अथवा SI)
- अन्य धातु (other metal)
- पी-खण्ड के धात्विक तत्वों में से कोई भी, जिनका सापेक्षिक गलनांक (सभी का 950 केल्विन से कम)) कम के रूप में चिह्नित किया जाता है और इनकी सापेक्ष विद्युत्-ऋणात्मकता का मान (सभी 1.6 से अधिक, संशोधित पॉलिंग) अधिक होता है।
- अपकेंदित्र (centrifuge)
- अपकेन्द्रण से आकार, आकृति और घनत्व के आधार पर पदार्थों को अलग करने के लिए काम में आने वाला यंत्र अथवा पदार्थ को समाहित करने वाले पात्र का केन्द्रीय अक्ष के चारों तरह बहुत ही तेज गति से घूर्णन।
- अपकेन्द्रण (centrifugation)
- एक प्रायोगिक तकनीक जिसमें अपकेन्द्रीय बल के अनुप्रयोग से विलयन से कणों को उनके आकार, आकृति एवं घनत्व के अनुसार अलग किया जाता है। बड़े और/अथवा सघन पदार्थ अपकेंदित्र की अक्ष से दूर चले जाते हैं जबकि छोटे और/अथवा कम घनत्व वाले पदार्थ अक्ष की तरफ चले जाते हैं।
- अपक्रांतिकता (reactivity)
- किसी रासायनिक पदार्थ के या तो स्वयं से या फिर अन्य पदार्थों के साथ रासायनिक अभिक्रिया में जाने की प्रवृत्ति, सामान्यतः या फिर दोनों पृथक प्रेक्षणों को सन्दर्भित करता है: कोई पदार्थ विशिष्ट परिस्थितियों में अभिक्रिया में शामिल होता है और कितना तेजी से अभिक्रिया करता है (अर्थात् अभिक्रिया दर)। उष्मागतिकीय रूप से किसी रासायनिक अभिक्रिया के होने का कारण अभिकर्मकों की तुलना में उत्पादों (समूह के रूप में) की मुक्त ऊर्जा का कम होना होता है, अतः ऊर्जा के पदों में उत्पाद अधिक "स्थायी" होते हैं लेकिन अपक्रांतिकता की अवधारण में उपयोग के अधार पर गतिक गुणकों को भी सन्निहित कर सकते है। रासायनिक स्थायित्व और रासायनिक संगतता सम्बंधित हैं लेकिन पृथक अवधारणायें हैं।
- अपक्रांतिकता शृंखला (reactivity series)
- धातुओं की शृंखला की आनुभाविक, परिकलित और संरचनात्मक विश्लेषी श्रेढ़ी, जिन्हें उनके सामान्य अपक्रांतिकता के उच्च से निम्न क्रम में व्यवस्थित किया जाता है तथा इनके अम्लों एवं जल के साथ अभिक्रिया के बारे में सूचना को काम में लिया जाता है व इस विधि से अयस्कों से इन्हें अलग करने के काम में लिया जाता है।
- अपचयन (reduction)
- रेडॉक्स अभिक्रिया में रासायनिक जाति की ऑक्सीकरण संख्या में कमी, सामान्यतः ऐसा इलेक्ट्रॉनों की वृद्धि से होता है। ऑक्सीकरण से विपरीत।
- अपचयन विभव (reduction potential)
- अपचायक (reducing agent)
- एक रासायनिक जाति जो एक अथवा अधिक इलेक्ट्रॉनों का ह्रास अथवा दान अन्य जाति को होती है, इसे रेडॉक्स अभिक्रिया में आक्सीकारक कहा जाता है अतः अन्य जाति के लिए यह अपचयन का कारण बनता है एवं खुद का ऑक्सीकरण करता है। अपचायी कर्मक की ऑक्सीकरण संख्या बढ़ती है जबकि आक्सीकारक की घटती है।[1]
- अपररूपता (allotrope)
- भिन्न भिन्न संरचना वाले तत्व (और अतएव भिन्न रूप), जैसेकार्बन (हीरा, ग्रेफाइट और फुलेरेन)।
- अभिकर्मक (reactant)
- रासायनिक अभिक्रिया के दौरान काम में आने वाले पदार्थ।
- अभिकारक (reagent)
- एक परीक्षण पदार्थ जिसे रासायनिक अभिक्रिया करवाने के लिए किसी निकाय में जोड़ा जाता है, अथवा किसी अभिक्रिया के घटित होने के लिए देखा जाता है।
- अभिक्रिया की कोटि (order of reaction)
- अभिक्रिया की दर (reaction rate)
- किसी रासायनिक अभिक्रिया में अभिकर्मकों को उत्पादों में परिवर्तित करने की गति।
- अभिक्रिया क्रिया-विधि (reaction mechanism)
- मूलभूत अभिक्रियाओं का क्रमानुगत अनुक्रम जो बड़ी रासायनिक अभिक्रिया द्वारा हो अथवा पूर्णतः परिवर्तन हो। एक पूर्ण क्रियाविधि वर्णित होनी चाहिये अथवा टूटने वाले आबंधों की व्याख्या हो और कौनसे निर्मित हुये हैं (एवं कौनसे क्रम में), इसी तरह अभिकर्मक, उत्पाद एवं उत्प्रेरक शामिल होते हैं; प्रत्येक की मात्रा; प्रतिघाती मध्यकों, सक्रियित संकुलों तथा संक्रमण अवस्थाओं; और प्रत्येक रासायनिक जाति के त्रिविम रसायन सभी को शामिल करते हैं। क्योंकि जटिल अभिक्रियाओं की विस्तृत प्रक्रियायें अधिकतर स्थितियों में प्रेक्षणीय नहीं होती, एक अभिक्रिया क्रियाविधि अक्सर उष्मागतिक साध्यता आधारित सैद्धान्तिक अनुमान होता है और प्रयोग से इसके पक्ष में थोड़ा संबल किया जा सकता है।
- अभिक्रिया दर स्थिरांक (reaction rate constant)
- अभिक्रिया-क्रम (work-up)
- वांछित उत्पाद अथवा किसी रासायनिक अभिक्रिया के उत्पाद को विलगित एवं विशुद्ध करने के लिए आवश्यक कार्यसाधन शृंखला।
- अमलगम (amalgam)
- पारे के साथ अन्य किसी धातु से मिलकर निर्मित मिश्रधातु।
- अमोनियामय (ammoniacal)
- ऐसे विलयन का वर्णन जिसमें विलायक जलीय अमोनिया हो।[1]
- अम्ल (acid)
- ऐसा यौगिक जिसे जब जल में घोला जाता है तो इसका पीएच मान 7.0 से कम हो जाता है अथवा हाइड्रोजन आयन देता है।
- अम्ल ऐनहाइड्राइट (acid anhydride)
- कोई भी रासायनिक यौगिक जो अम्ल से जल के अणु को हटाकर व्युत्पन्न किया जाता है। क्षार ऐनहाइड्राइड से अलग।
- अम्ल वियोजन स्थिरांक (acid dissociation constant) (Ka)
- किसी विलयन में अम्ल की प्रबलता का मात्रात्मक मापन अम्ल-क्षार अभिक्रियाओं के परिपेक्ष्य में रासायनिक वियोजन अभिक्रिया के लिए साम्य नियतांक के रूप में व्यक्त किया जाता है। इसे अक्सर 10-आधारी लघुगणकीय मान के रूप में दिया जाता है जिसे pKa के रूप में लिखते हैं।
- अम्ल–क्षारक निष्कर्षण (acid–base extraction)
- एक ऐसा यौगिक जिसे जब जल में मिलाया जाता है तो इसका पीएच मान 7.0 से कम हो जाता है और यह हाइड्रोजन आयन देता है।
- अम्लराज (aqua regia)
- नाइट्रिक अम्ल (HNO3) और हाइड्रोक्लोरिक अम्ल (HCl) का एक द्रव मिश्रण जिसका इष्टतम मोलर अनुपात 1:3 रखा जाता है, अतः ऐतिहासिक रसायनविदों ने इसका नामकरण अम्लराज के रूप में इसलिए किया क्योंकि यह सोना एवं प्लैटिनम जैसी उत्कृष्ट धातुओं को घोलने में सक्षम है।
- अयुग्मित इलेक्ट्रॉन (unpaired electron)
- अर्धचालक पदार्थ (semiconductor)
- वैद्युतीय रूप से चालक ठोस जिसकी चालकता चालकों एवं कुचालकों के मध्य होती है।
- अर्धांश (moiety)
- कोई भी नामित विशेषता समूह, शाखा अथवा अणु का बड़ा भाग जो अन्य प्रकार के कणों में भी समान रूप से पहचाने जा सकते हैं। प्रकार्यात्मक समूह अक्सर अर्धांशों की तुलना में छोटे और अधिक सामान्य होते हैं, जबकि प्रतिस्थापी और पार्श्व शृंखलायें अक्सर अर्धांशों के रूप में वर्गीकृत किये जा सकते हैं एवं इसके उल्ट भी।
- अल्केन (alkane)
- कोई भी संतृप्त अचक्रीय हाइड्रोकार्बन।
- अवक्षेप (precipitate)
- किसी विलयन में ठोस का निर्माण अथवा किसी रासायनिक अभिक्रिया के दौरान किसी अन्य ठोस में या किसी ठोस में विसरण के दौरान ठोस का निर्माण।
- अवपरमाणुक कण (subatomic particle)
- कोई भी कण जो परमाणु से छोटे होते हैं। इसके उदाहरणो में प्रोटॉन, न्यूट्रॉन और इलेक्ट्रॉन शामिल हैं।
- अवशोषण (absorption)
- 1. भौतिक अथवा रासायनिक प्रक्रम जिसमें किसी एक प्रावस्था में पदार्थ किसी अन्य प्रावस्था में अन्य पदार्थ के साथ मिल जाता है। अवशोषण और अधिशोषण अलग-अलग होते हैं, अधिशोषण की प्रक्रिया में पहला पदार्थ पूरे निकाय में मिल जाता है न कि केवल पृष्ठ पर चिपकता हो।
- 2. वह प्रक्रिया जिसमें पदार्थ (अक्सर परमाणुओं में बद्ध इलेक्ट्रॉन) विद्युतचुंबकीय विकिरण की ऊर्जा लेकर एवं इसको विभिन्न तरह की आन्तरिक ऊर्जा जैसे ऊष्मीय ऊर्जा में परिवर्तित कर लेता है। इस तरह के अवशोषण स्पेक्ट्रमी प्रकाशमिति का मूलभूत सिद्धान्त है।
- अवशोषणांक (absorbance)
- अविस्तारात्मक गुणधर्म (extensive property)
- A physical quantity whose value is proportional to the size of the system it describes or to the quantity of पदार्थ in the system. Examples include द्रव्यमान, आयतन, एन्थैल्पी, and एन्ट्रॉपी. Contrast अविस्तारात्मक गुणधर्म.
- अविस्तारात्मक गुणधर्म (intensive property)
- एक भौतिक राशि जिसका मान निकाय के आकार अथवा पदार्थ की मात्रा पर निर्भर नहीं करते जिसके लिए उनका मापन किया जा रहा है। उदाहरण के लिए घनत्व, तापमान और दाब। विस्तारात्मक गुणधर्म के विपरीत।
- अवोगाद्रो का नियम (Avogadro's law)
- अष्टक नियम (octet rule)
- कुछ निश्चित अणुओं में परमाणुओं के इलेक्ट्रॉन विन्यास को वर्णित करने का चिरसम्मत नियम: आवर्त सारणी की प्रथम पंक्ति के किसी तत्व के संयोजी कोश में समायोजित किये जा सकने वाले इलेक्ट्रॉन युग्मों की अधिकतम संख्या चार (अथवा कुल इलेक्ट्रॉन आठ) होती है। दूसरी एवं अन्य पंक्तियों के लिए इस नियम के बहुत अपवाद उपलब्ध हैं।
- आक्सीकारक (oxidizing agent)
- 1. एक रासायनिक जाति अन्न्य जाति से एक अथवा अधिक इलेक्ट्रॉनों की वृद्धि अथवा ग्रहण करती है उसे रेडॉक्स अभिक्रिया में अपचायक कहते हैं जिससे अन्य जाति का ऑक्सीकरण होता है एवं स्वयं को अपचायी में बदल लेता है। आक्सीकारकों की ऑक्सीकरण संख्या कम होती है जबकि अपचायकों की बढ़ती है।[1]
- 2. एक रासायनिक जाति जो प्रबलता से विद्युत्-ऋणात्मक परमाणुओं का स्थानान्तरण करती है, सामान्यतः ऑक्सीजन को कम करती है।
- आघातवर्धनीयता (malleability)
- तन्यता देखें।
- आणविक सूत्र (molecular formula)
- आण्विक कक्षक (molecular orbital अथवा MO)
- अणु में पाया जाने वाला वह क्षेत्र जिसमें एक अथवा अधिक इलेक्ट्रॉन पाये जाते हैं (व्यक्तिगत परमाणु में इसका विरोध होता है।)
- आण्विक कक्षक आरेख (molecular orbital diagram)
- आदर्श गैस (ideal gas)
- आदर्श गैस समीकरण (ideal gas law)
- ऐसा रासायनिक नियम जिसके अनुसार किसी गैस का आयतन गैस की मात्रा और इसके केल्विन तापमान के अनुक्रमानुपाती एवं दाब के व्युत्क्रमानुपाती होता है।
- आदर्श विलयन (ideal solution)
- ऐसा विलयन जिसके गैस प्रावस्था के उष्मागतिकीय गुणधर्म आदर्श गैसों के मिश्रण के अनुरूप हों।
- आद्र रसायनशास्त्र (wet chemistry)
- विश्लेषी रसायन का एक रूप जिसमें रसायनों एवं रासायनिक अभिक्रियाओं के अध्यन के लिए मूलभूत रासायनिक परीक्षण व साधारण प्रेक्षण चिरसम्मत प्रयोगशाला विधियों से किये जाते हैं, उदाहरण के लिए परिष्कृत उपकरणों अथवा स्वतः अथवा कंप्यूटरीकृत विशलेष्यों के उपयोग रहित। ये विधियाँ सामान्यतः विद्यालयों में विद्यार्थियों को रसायनशास्त्र के सिद्धान्त पढ़ाने के लिए काम में लिये जाते हैं।
- आद्रकारक कर्मक (wetting agent)
- आनुभविक सूत्र (empirical formula)
- किसी यौगिक में उपस्थित प्रत्येक तत्व के परमाणुओं का सरलतम पूर्ण-संख्या अनुपात।
- आबंध (bond)
- परमाणुओं, आयनों अथवा अणुओं के मध्य कोई भी दृढ़ आकर्षण जो रासायनिक यौगिकों के निर्माण को अनुमत करता है। आबंधों का निर्माण विभिन्न वैद्युत-रासायनिक बलों के परिणामस्वरूप निर्मित होता है जिनकी प्रबलता पर्याप्त रूप से बदलता है; जब इनके बल से अधिक बल आरोपित किया जाता है तो ये आबंध टूट जाते हैं। आबंधों का प्रकार, प्रबलता और मात्रा रासायनिक पदार्थों को साथ में जोड़कर रखते हैं एवं पदार्थ के विस्तृत गुणधर्मों व संरचना को निर्णित करते हैं।
- आयतन (volume)
- बंद सतह से परिबद्ध त्रिविम समष्टि की मात्रा अथवा दिक्काश का वह भाग जो किसी पदार्थ (ठोस, द्रव, गैस अथवा प्लाज़्मा) या आकृति द्वारा घेरा या रखा जाता है। आयतन का एसआई मात्रक घन मीटर (m3) है।
- आयतनी विश्लेषण (volumetric analysis)
- अनुमापन देखें।
- आयन (ion)
- कोई अणु जब अपनी प्राकृतिक अवस्था में एक अथवा अधिक इलेक्ट्रॉनों को प्राप्त करता है अथवा खो देता है जिससे ऋणात्मक अथवा धनात्मक विद्युत आवेश प्राप्त करता है।
- आयनन (ionization)
- रासायनिक यौगिकों का अलग-अलग आयनों में टूटना।
- आयनिक सामर्थ्य (ionic strength)
- विलयन में आयनों की सान्द्रता का एक मापन। इसे सामान्यतः मोलरता (mol/L विलयन) अथवा मोललता (mol/kg विलायक) के पदों में लिखा जाता है।[2]
- आयनी आबन्ध (ionic bond)
- विपरीत आवेशित आयनों के मध्य वैद्युती आकर्षण।
- आर्द्रताग्राही (hygroscopy)
- आवर्त (period)
- तत्वों की आवर्त सारणी की क्षैतिज पंक्ति और तत्व जो इसमें शामिल हैं। समूह से अलग।
- आवृत्ति (frequency)
- एकांक समय में दी गयी प्रक्रिया के चक्रों की संख्या का मापन। आवृत्ति का एसआई मात्र हर्ट्ज़ (Hz) है, 1 Hz = 1 चक्र प्रति सेकेंड होता है।
- आवेश संख्या (charge number)
- आवोगाद्रो संख्या (Avogadro's number)
- किसी पदार्थ के एक मोल में विविक्त घटक कणों (अणुओं, परमाणुओं अथवा आयनों के रूप में) की संख्या जिसे 6.02214076×1023 ऐसे कणों के रूप में परिभाषित किया जाता है।
- आंशिक दाब (partial pressure)
- आंशिक दाब का डॉल्टन का नियम (Dalton's law of partial pressures)
- आसंजन (adhesion)
- अंतराणुक बलों के परिणामस्वरूप दूसरी प्रकृति के कणों अथवा फलकों से एक दूसरे के चिपकने की प्रवृत्ति। संसंजन से विपरीत।
- आसवन (distillation)
- द्रव मिश्रण के घटक द्रव्यों को अलग करने की प्रक्रिया जिसमें मिश्रण के घटकों के क्वथन एवं उसके बाद संघनन को काम में लेते हुये उनकी सापेक्ष वाष्पशीलता के अनुसार अलग किया जाता है। किसी ओअदार्थ के आसवन में काम आने वाले उपकरण को स्टिल कहते हैं और पदार्थ के पुनःसंघनित होने की प्रक्रिया को आसवन कहते हैं।
- इकाई घटक (unit factor)
- इकाइयों के मध्य रूपांतरण के लिए काम आने वाले वाक्य।
- इलेक्ट्रॉन (electron)
- ऋणात्मक नेट आवेश वाले अवपरमाणुक कणों का एक प्रकार।
- इलेक्ट्रॉन आवरण अथवा इलेक्ट्रॉन कोश (electron shell)
- परमाणु के नाभिक के चारों तरफ़ कक्षक जिसमें निश्चित संख्या में इलेक्ट्रॉन (सामान्यतः दो अथवा आठ) हों।
- इलेक्ट्रॉन न्यूनता (electron deficiency)
- इलेक्ट्रॉन युग्म (electron pair)
- समान आण्विक कक्षक लेकिन भिन्न प्रचक्रण वाले दो इलेक्ट्रॉन। रासायनिक आबंधों के इलेक्ट्रॉन युग्म अथवा संयोजी इलेक्ट्रॉन के एकाकी युग्म; यह भी सम्भव है कि अयुग्मित इलेक्ट्रॉन अलग-अलग आते हों।
- इलेक्ट्रॉन विन्यास (electron configuration)
- परमाण्विय अथवा आण्विक कक्षकों में परमाणु अथवा अणु के इलेक्ट्रॉनों का वितरण। प्रत्येक परमाण्विय जाति के इलेक्ट्रॉन विन्यास के बारे में अद्वितीय सूचना प्रदर्शित करने के लिए एक विस्तृत संकेतन प्रणाली काम में ली जाती है। भिन्न परमाणुओं में इलेक्ट्रॉनों के विशिष्ट विन्यास की जानकारी रासायनिक आबंधों की समझ एवं तत्वों की आवर्त सारणी में व्यवस्था के लिए उपयोगी होता है।
- इलेक्ट्रॉनरागी (electrophile)
- कोई भी परमाणु अथवा अणु जो इलेक्ट्रॉन युग्म को स्वीकार करते हैं। मुख्य इलेक्ट्रॉनरागी नेट धनावेश रखते हैं इसमें वो परमाणु भी शामिल हैं जिनपर आंशिक धनावेश हो अथवा वो उदासीन परमाणु भी शामिल हैं जिनका इलेक्ट्रॉनों का अष्टक पूरा नहीं करते और अतएव वो इलेक्ट्रॉन बहुलता वाले क्षेत्र अथवा द्रव्यों को आकर्षित करते हैं; रिक्त कक्षकों वाला कोई इलेक्ट्रॉनरागी, नाभिकरागी द्वारा प्रदत्त इलेक्ट्रॉन युग्म को ग्रहण कर सकता है, एवं अन्य जातियों के मध्य रासायनिक आबंध निर्मित करते हैं। क्योंकि ये इलेक्ट्रॉनों को ग्रहण करते हैं, अतः इलेक्ट्रॉनरागी परिभाषा से लूइस अम्ल होते हैं।
- ईथर (ether)
- कार्बनिक यौगिकों का एक वर्ग और प्रकार्यात्मक समूह जिसमें ऑक्सीजन परमाणु दो ऐल्किल अथवा ऐरिल समूहों से जुड़ा हुआ होता है, इसमें ये दोनों समूह समान भी हो सकते हैं एवं भिन्न भी। ईथर का सामान्य सूत्र R–O–R' होता है जहाँ R एवं R' ऐल्किल अथवा ऐरिल समूहों को वर्णित करते हैं।
- उच्चतापसह अथवा दुर्गलनीय (refractory)
- 1. उच्च गलनांक होना।[1]
- 2. कोई पदार्थ जो ऊष्मा, दाब अथवा रासायनिक आक्षेप से अपघटन का प्रतिरोध करता है एवं अपनी कठोरता को बनाये रखता है एवं उच्च तापमानों पर भी बना रहकर सम्बंधित परिवेश की स्थितियों में में अनुप्रयोगों के लिए उपयुक्त बनाता है। दुर्गलनीय सामान्यतः बहुक्रिस्टलीय, पॉलीफेज, अकार्बनिक, अधात्विक, सरंध्री और विषमांगी यौगिक होते हैं।
- उच्छलन (bumping)
- वो घटना जिसमें समांगी द्रव को इसके क्वथनांक तल लेकर जाया जाता है जिससे अतितापित एवं नाभिकन को प्राप्त होता है, गैसीय अवस्था में जल्दी से उबलने लगता है, एवं पात्र से द्रव के प्रचंड निष्कासन के रूप में परिणत हो; चरम स्थिति में, पात्र भी टूट सकता है। पात्र को बार-बार हिलाना, सही पात्र का चयन करना एवं क्वथन चिपों का उपयोग उच्छलन से बचा सकती है।
- उत्कृष्ट गैस (noble gas)
- आवर्त सारणी के समूह 18 के छः अधात्विक तत्व:: हिलियम (He), नियोन (Ne), आर्गन (Ar), क्रिप्टॉन (Kr), ज़ेनान (Xe) और रेडॉन (Rn)। सभी नोबल गैसों के बाहरी इलेक्ट्रॉन कोश उनकी प्राकृतिक अवस्था में पूर्णतः भरे होते हैं जो इनकी रासायनिक क्रियाशीलता को न्यूनतम कर देता है।
- उत्प्रेरक (catalyst)
- कोई तत्व अथवा यौगिक जो रासायनिक अभिक्रिया की गति में वृद्धि को सुविधाजनक बनाता है लेकिन वो स्वयं अभिक्रिया में भाग नहीं लेता। इसमें अभिक्रिया के अभिकर्मक और उत्पाद दोनों को माना जाता है।
- उपधातु (metalloid)
- धातुओं और अधातुओं दोनों के गुणधर्मों को रखने वाले एक रासायनिक तत्व अथवा पदार्थ।
- उपसहसंयोजक यौगिक (coordination complex)
- एक रासायनिक यौगिक का केन्द्रीय परमाणु अथवा आयन सामान्यतः धात्विक होते हैं और इन्हें उपसहसंयोजी केन्द्र के रूप में जाना जाता है, यह केन्द्र परमाणुओं के अन्य समूह की शृंखला के आबंधों से घिरे हुये रहते हैं। उदाहरण के लिए संलग्नी अथवा संकुलन कर्मक के रूप में पहचाने जाने वाले अणु या आयन। विभिन्न धातुओं वाले यौगिक, विशेषतः वो संक्रमण धातु जिनमें उपसहसंयोजक यौगिक हैं। कोम्प्लेक्स देखें।
- उपसहसंयोजकता रशायनशास्त्र (coordinate chemistry)
- उपसहसंयोजी सहसंयोजक आबंध (coordinate covalent bond)
- उभयधर्मी (amphoteric)
- माध्यम के अनुरूप (किसी रासायनिक जाति के लिए) दोनों अम्ल और क्षार के रूप में व्यवहार करने की प्रवृत्ति; उदाहरण के लिए सल्फ्यूरिक अम्ल (H2SO4) जल में एक प्रबल अम्ल है लेकिन अति अम्लों के लिए क्षार की तरह व्यवहार करता है।
- उभयसंवेदी (amphipathic)
- (किसी अणु से) दोनों जलस्नेही और जलविरोधी समूहों से निर्मित; उदाहरण के लिए आद्रकारक कर्मक और तरल झिल्ली।[3]
- उर्ध्वपातन (sublimation)
- किसी पदार्थ के ठोस से चूने का पानी ईंधन अथवा गैस प्रावस्था संक्रमण बिना मध्यवर्ती संक्रमण अवस्था द्रव में हुये हो जाता है।
- उष्मा-रसायन में हेस के नियम की उपयोगिता (Hess' law of constant ऊष्मा summation)
- भौतिक रसायन का एक नियम जिसमें रासायनिक अभिक्रिया के दौरान कुल एन्थैल्पी किसी एक चरण अथवा विभिन्न चरणों में समान रहती है।
- उष्मागतिक स्थायित्व (thermodynamic stability)
- निकाय की वो अवस्था जब वह परिवेश (साम्य) के साथ निम्नतम ऊर्जा अवस्था में हो।
- उष्मागतिकी (thermodynamics)
- स्थूल पैमाने पर परिवर्तनी तापमान, आयतन अथवा दाब (अथवा कार्य, ऊष्मा और ऊर्जा) के प्रभाव का अध्ययन।
- उष्मीय मान (calorific value)
- किसी दिये गये पदार्थ के सम्पूर्ण दहन में निर्मित प्रति इकाई द्रव्यमान से उत्सर्जित उष्मा का मापन, सामान्यतः इसे किलो-जूल प्रति ग्राम (kJ/g) अथवा मेघाजूल प्रति किलोग्राम में लिखा जाता है।[1]
- ऊर्जा (energy)
- किसी निकाय की कार्य करने की क्षमता।
- ऊर्जा संरक्षण का नियम (law of conservation of energy)
- ऊर्णन (flocculation)
- ऊर्णिक (floc) अथवा पत्रक (flake) के रूप में जाने वाले बड़े संपुंजन के रूप में आने के लिए निलंबन से कोलॉइड में परिक्षेपित कणों के आने की प्रक्रिया, यह या तो स्वतः होता है अथवा निर्मलन कर्मक मिलाने से होता है। यह शब्द सामान्यतः व्युत्क्रमणीय एकत्रीकरण को सन्दर्भित करता है जिसमें कणों को बांधे रखने वाले कण एक दूसरे से दुर्बलता से बंधे होते हैं एवं कोलॉइड पुनःपरिक्षेपित हो सकता है।[1]
- ऊष्मा (heat)
- उष्मीय अन्योन्य क्रिया के दौरान एक निकाय से अन्य में स्थानान्तरित ऊर्जा।
- ऊष्मा चालकता (thermal conductivity)
- पदार्थों के गुणधर्म जो उष्मीय ऊर्जा अथवा ऊष्मा के चालन को अनुमत करते हैं (अक्सर से निरूपित की जाने वाला गुणधर्म।)
- ऊष्माक्षेपी प्रक्रम (exothermic process)
- ऊष्मागतिकी के सिद्धान्त (laws of thermodynamics)
- ऊष्मामापी (calorimeter)
- उष्मीय गुणधर्मों (उदाहरण के लिए ऊष्मा) के मापन के काम आने वाले विभिन्न यंत्रों में से कोई भी जैसे रासायनिक अभिक्रिया में ऊष्मा अथवा उष्मीय मान।[1]
- ऊष्मारसायन (thermochemistry)
- रासायनिक अभिक्रिया के दौरान ऊष्मा के उत्सर्जन अथवा अवशोषण का अध्ययन।
- ऊष्माशोषी प्रक्रम (endothermic process)
- ऋणायन (anion)
- एक ऋणात्मक आवेश वाला आयन; उदाहरण के लिए प्रोटॉनों की तुलना में अतिरिक्त इलेक्ट्रॉनों के कारण कोई अणु अथवा परमाणु जिसपर नेट ऋणात्मक विद्युत आवेश को प्राप्त करता है।
- ऍक्स किरण (X-ray)
- विद्युतचुंबकीय वर्णक्रम में गामा किरणों और पराबैंगनी किरणों के मध्य की विद्युत्चुम्बकीय विकिरणें जो आयनीकरण से प्राप्त होती हैं।
- ऍक्स-किरण प्रकाशिक इलेक्ट्रॉन स्पेक्ट्रमिकी (X-ray photoelectron spectroscopy)
- किसी पदार्थ के रासायनिक संघटन के मापन करने के लिए काम में ली जाने वाली स्पेक्ट्रमी तकनीकी।
- ऍक्स-किरण विवर्तन (X-ray diffraction)
- एकल तरंगदैर्घ्य की ऍक्स-किरणों एवं इसके विभिन्न विवर्तन प्रतिरुपों का उपयोग करते हुये "क्रिस्टलीय" ठोसों की संरचनाओं को स्थापित करने की एक विधि।
- ऍफ़-खण्ड (f-block)
- एकक कोष्ठिका (unit cell)
- क्रिस्ट्लीय जालक की सबसे छोटी पुनरावृत्त इकाई।
- एकपरमाण्विक (monatomic)
- दो या दो से अधिक परमाणुओं से मिलकर बनने वाले अणु के स्थान पर केवल एक ही परमाणु वाला। पर्याप्त रूप से उच्च तापमान पर किसी भी गैस प्रावस्था में काल्पनिक रूप से सभी तत्व एकपरमाण्विक होते हैं। द्वि-परमाणुक और बहुपरमाणुक से अलग।
- एकल-आबंध (single bond)
- ऐसा आबंध जिसमें एक इलेक्ट्रॉनों का जोड़ा साझा होता है।
- एकाधिक अनुपात का नियम (law of multiple proportions)
- एकीकृत परमाण्वीय द्रव्यमान मात्रक (unified atomic mass unit अथवा u)
- द्रव्यमान की एक इकाई जो किसी एक प्रोटॉन अथवा न्यूट्रॉन के द्रव्यमान के लगभग होता है। कभी-कभी इसे तकनीकी रूप से अलग एवं अप्रचलित शब्द परमाण्वीय द्रव्यमान मात्रक में लिखा जाता है और इसका संक्षिप्त रूप एएमयू (amu) लिखा जाता है।
- एटोमिसिटी (atomicity)
- किसी दिये गये पदार्थ के किसी एकल अणु में उपस्थित परमाणुओं की कुल संख्या; उदाहरण के लिए ओज़ोन (O3) की एटोमिसिटी 3 है जबकि बेंजीन (C6H6) की एटोमिसिटी 12 है।[1]
- एन्ट्रॉपी (entropy)
- बन्द उष्मागतिक निकाय में कार्य के लिए अनुपलब्ध ऊर्जा की मात्रा, सामान्यतः S से लिखा जाता है।
- एन्थैल्पी अथवा पूर्ण ऊष्मा (enthalpy)
- उष्मागतिक निकाय की कुल आन्तरिक ऊर्जा का मापन, इसे सामान्यतः H से लिखा जाता है।
- एपपेंडॉर्फ ट्यूब (Eppendorf tube)
- सूक्ष्म अपकेंद्रीय नली को सन्दर्भित करने के लिए काम में लिया जाने वाला व्यापक एवं ट्रेडमार्क नाम।
- एपीमर (epimer)
- एंथेल्पी (enplethy)
- पदार्थ की मात्रा भी।
- एरोमैटिसिटी (aromaticity)
- परमाणुओं की संयुग्मी वलय के रासायनिक गुणधर्म जैसे बेंजीन जो कि सामान्यतः बहुत अधिक स्थायी है। ऐसी वलयों को अरोमैटिक कहते हैं।
- एल्डिहाइड (aldehyde)
- हाइड्रोजन एवं किसी अन्य आर-समूह से जुड़ा हुआ कार्बोनिल समूह को शामिल करने वाला कोई भी कार्बनिक यौगिक।
- एस-खण्ड (s-block)
- आवर्त सारणी के समूह 1 और 2 के तत्वों का सामूहिक नाम इनमें क्षार धातु एवं क्षार मृदा धातु के अतिरिक्त हाइड्रोजन व हिलियम भी शामिल हैं।
- एस्टर (ester)
- ऐल्कोहॉल की अम्ल के साथ अभिक्रिया से व्युत्पन्न कार्बनिक और अकार्बनिक यौगिकों का एक वर्ग जिसमें कम से कम एक हाइड्रॉक्सिल समूह (–OH) को ऐल्कॉक्सी समूह (–O–) से प्रतिस्थापित किया जाता है। एस्टरों का सामान्य सूत्र RCO2R′ होता है जहाँ R एवं R' कोई भी ऐल्किल अथवा ऐरिल समूह है।
- ऐक्टिनाइड (actinides)
- परमाणु संख्या 89 से 103 तक, ऐक्टिनियम से लोरेनसियम तक के धात्विक तत्वों की आवर्ती शृंखला।
- ऐट्मोलिसिस (atmolysis)
- भिन्न-भिन्न विसरण दर की सहायता से गैसों के मिश्रण को अलग करने की विधि जिसमें सामान्यतः गैसों को छिद्रयुक्त वितरण अथवा झिल्ली की दिवारों से गुजारकर प्रसारित किया जाता है।[1]
- ऐनैन्टियोमर (enantiomer)
- ऐमिल (amyl)
- पेन्टिल समूह के लिए सामान्य गैर प्रणालीगत नाम।
- ऐरिल (aryl)
- एरोमैटिसिटी वलय से व्युत्पन कोई प्रकार्यात्मक समूह अथवा प्रतिस्थापी, जैसे फिनाइल अथवा नैफ्थलीन। संरचनात्मक चित्र में सामान्य ऐरिल समूह के लिए Ar प्रतीक के रूप में काम में लिया जात है।
- ऐर्लेनमेयर फ्लास्क (Erlenmeyer flask)
- ऐल्काइन (alkyne)
- ऐसा असंतृप्त हाइड्रोकार्बन जिसमें कम से कम एक त्रि-आबंधी कार्बन युग्म समाहित हो।
- ऐल्किल समूह (alkyl group)
- ऐसा प्रकार्यात्मक समूह जिसमें अल्केन में एक हाइड्रोजन परमाणु की कमी हो।
- ऐल्कीन (alkene)
- कम से कम एक द्वि-आबन्ध कार्बन युग्म वाले असंतृप्त हाइड्रोकार्बन।
- ऐल्कोहॉल (alcohol)
- कोई भी कार्बनिक यौगिक जिसमें संतृप्त कार्बन परमाणु के साथ हाइड्रॉक्सिल प्रकार्यात्मक समूह जुड़ा हुआ हो।
- ऑक्सी अम्ल (oxoacid)
- 1. अम्लीय समूह में ऑक्सीजन के साथ कोई अम्ल।
- 2. कोई भी ऐसा यौगिक जिसमें ऑक्सीजन के अतिरिक्त एक अन्य कोई तत्व हो एवं कम से कम एक हाइड्रोजन ऑक्सीजन के साथ बद्ध हो तथा धन आयनों के ह्रास से वो संयुग्मी क्षार निर्मित करता हो।
- ऑक्सीकरण (oxidation)
- रेडॉक्स अभिक्रिया में किसी रासायनिक जाति की ऑक्सीकरण संख्या में वृद्धि, सामान्यतः इलेक्ट्रॉन ह्रास से। अपचयन के विपरीत।
- ऑक्सीकरण संख्या (oxidation state)
- 1. रासायनिक यौगिक में व्यक्तिगत परमाणु की ऑक्सीकरण की कोटि, इसे तात्विक अवस्थाओं में परमाणु की प्राकृतिक उदासीन स्थिति के सापेक्ष इलेक्ट्रॉनों की संख्या में कमी के रूप में मापा जाता है।
- 2. यदि सभी भिन्न तत्वों के परमाणुओं को 100% आयनी बंधो से प्रतिस्थापित कर दिया जाये और कोई भी सहसंयोजी घटक न हो तब परमाणु का काल्पनिक विद्युत आवेश (धनात्मक, ऋणात्मक अथवा शून्य)।
- ऑक्सीजन (oxygen)
- ओलिफिन (olefin)
- किसी भी ऐल्कीन रूढ़ (गैर-आईयूपीएसी) नाम।
- कंकाली सूत्र (skeletal formula)
- कक्षक (orbital)
- परमाणु अथवा अणु का वो क्षेत्र जिसमें एक अथवा अधिक इलेक्ट्रॉन पाये जा सकते हैं। यह शब्द परमाणु कक्षक अथवा आण्विक कक्षक के लिए काम में लिया जा सकता है।
- कक्षीय संकरण (orbital hybridisation)
- कठोर जल (hard water)
- वह जल जिसमें खनिज की मात्रा बहुत ज्यादा हो, सामान्यतः कैल्सियम, मैग्नीसियम अथवा निश्चित अन्य धातु धनायनों में जल के रिसाव से इसका निर्माण होता है।
- कंडोसीटी (condosity)
- किसी विलयन की विद्युत चालकता का एक तुलनात्मक मापन जिसे सोडियम क्लोराइड (NaCl) विलयन की मोलर सान्द्रता के रूप में परिभाषित किया जाता है; इसमें परीक्षण के दौरान विलयन की विशिष्ट विद्युत चालकता ज्ञात की जाती है। इसकी मापन की इकाई सामान्यतः मोल प्रति लिटर (अथवा किसी अन्य एकांक आयतन विमा) में व्यक्त की जाती है।
- काइरलता (chirality)
- असममिति का एक गुणधर्म जिसमें अणु अथवा आयन अपने दर्पण प्रतिबिंब से इस तरह भेद्य होता है कि इसे इसके किसी भी ज्यामितिय घूर्णन, स्थानान्तरण अथवा कुछ संरूपण परिवर्तन पर अध्यारोपित नहीं किया जा सकता।[4][5] ऐसे अणुओं अथवा आयनों को काइरल (chiral) कहा जाता है और ये दो रूपों में पाये जाते हैं जिन्हें ऐनैन्टियोमर कहते हैं और ये एक दूसरे के त्रिविम समावयवी होते हैं; इन रूपों को इनके निरपेक्ष विन्यास अथवा अन्य मापदंडों के अनुसार या तो "दक्षिण-हस्थ" अथवा "वाम-हस्थ" कहा जाता है। कुछ अन्य तरह की असममिति भी काइरलता का कारण बन सकती है, जिसमें सबसे अधिक कारण अणुओं के स्टीरियोजेनिक तत्वों को धारण करने जैसे एक अथवा अधिक स्टीरियो केन्द्र (केंद्रीय काइरलता), स्टीरियोजेनिक अक्ष (अक्षीय काइरलता) अथवा स्टीरियोजेनिक समतल (समतलीय काइरलता); इसके अतिरिक्त अणु की अंतर्निष्ट वक्रता भी इसमें अंतर्निष्ट काइरलता को उत्पन्न कर सकता है।
- कांच (glass)
- कार्ब-ऋणायन (carbanion)
- कार्बनिक अपचयोपचय अभिक्रिया (organic redox reaction)
- कार्बनिक अम्ल (organic acid)
- अम्लीय गुणधर्म के साथ कोई कार्बनिक यौगिक। जैविक क्षार की तरह उससे अलग।
- कार्बनिक यौगिक (organic compound)
- एक अथवा एक से अधिक कार्बन परमाणु वाला कोई रासायनिक यौगिक। अजैविक यौगिक से अलग।
- कार्बनिक रसायन (organic chemistry)
- कार्बनिक यौगिकों की अभिक्रिया और रासायनिक गुणधर्मों से सम्बंध रखने वाली रसायन विज्ञान की शाखा। अकार्बनिक रसायन से अलग।
- कार्बोकेशन (carbocation)
- कार्बोक्सिलिक अम्ल (carboxylic acid)
- कार्बोनिल (carbonyl)
- कार्य (work)
- कीटोन (ketone)
- कीलेटक (chelation)
- किसी बहुदन्तुर संलग्नी और एक केन्द्रीय धातु आयन के मध्य दो अलग-अलग उपसहसंयोजी सहसंयोजक आबंधों को शामिल करने वाले आबंधन का एक प्रकार। संलग्नी सामान्यतः एक कार्बनिक यौगिक होता है जिसे कीलेट अथवा कीलेटी कर्मक कहते हैं।
- कीलेटी कर्मक (chelating agent)
- कूलॉम (coulomb)
- विद्युत आवेश की एसआई इकाई (चिह्न: C), एक सेकेंड में एक एम्पियर धारा के प्रवाह से स्थानान्तरित आवेश द्वारा इसे परिभाषित किया जाता है।
- कृत्रिम रेडियोऐक्टिवता (induced radioactivity)
- किसी स्थायी नाभिक पर तात्विक कणों की बौछार से निर्मित रेडियोऐक्टिवता जिसमें रेडियोऐक्टिव समस्थानिक निर्मित होता है।
- केल्विन (kelvin अथवा K)
- तापमान की मूलभूत एसआई इकाई (चिह्न: K)। केल्विन पैमाना निरपेक्ष ऊष्मागतिक तापक्रम पैमाना है जिसका शून्य बिन्दु परम शून्य ताप होता है।
- कैथोड (cathode)
- एक इलेक्ट्रोड जिसके माध्यम से पारंपरिक विद्युत धारा (धनायनों का प्रवाह) ध्रुवीय विद्युत् परिपथ को छोड़ती है। धनावेशित धनायन हमेशा कैथोड की तरफ गति करते हैं, यद्यपि कैथोड़ की ध्रुवीयता विद्युत् यंत्र के प्रकार पर एवं इसके संचालन की विधि पर निर्भर धनात्मक अथवा ऋणात्मक हो सकती है। धनाग्र से विपरीत।
- कैल्कस (चूना) (calx)
- हवा में अयस्क को गर्म करके धातु ऑक्साइड का निर्माण।[1]
- कैस पंजीकरण संख्या (CAS Registry Number अथवा CAS RN)
- मुक्त वैज्ञानिक भाषा में वर्णित प्रत्येक रासायनिक पदार्थ के लिए रासायनिक अमूर्त क्षेत्र द्वारा नियत अद्वितीय संख्यात्मक प्राधिकारण, जिसमें सभी 18.2 करोड़ से अधिक कार्बनिक एवं अकार्बनिक यौगिक, खनिज, समस्थानिक, मिश्रधातु, बहुलक तथा मिश्रण सहित तथाकथित "यूवीसीबी" (अज्ञात अथवा परिवर्तनशील रचना, जटिल अभिक्रिया उत्पाद अथवा जैविक मूल के पदार्थ) शामिल हैं। कैस संख्यायें वैज्ञानिकों, उद्योगों और प्राधिकरण निकायों द्वारा काम में लिया जाता है एवं अंतरराष्ट्रीय मानकों के रूप में स्वीकृत है।[6]
- कोम्प्लेक्स (complex)
- आण्विक सत्वों (आयनी अथवा अनावेशित) अथवा सम्बंधित रासायनिक जाति के दो या दो से अधिक घटकों के मध्य कमजोर संगुणन से निर्मित आण्विक सत्व। घटकों के मध्य आबंधन सामान्यतः सहसंयोजी आबंध से कमजोर होते हैं।[7]उपसहसंयोजक यौगिक भी देखें।
- कोलॉइड (colloid)
- एकसमान परिक्षेपित पदार्थों का मिश्रण जैसे विभिन्न तरह के पायस।
- क्रांतिक बिन्दु (critical point)
- प्रावस्था साम्य वक्र अथवा दाब-तापमान वक्र का अन्तिम बिन्दु जिसपर परिस्थितियाँ कुछ इस तरह हों कि प्रावस्था सीमायें खत्म हो जाती हैं और पदार्थ की भिन्न-भिन्न प्रावस्थाओं के मध्य मिश्रण प्राप्त होता है जैसे द्रव एवं वाष्प दोनों सह-अस्तित्व में हो सकते हैं। क्रांतिक बिन्दु को क्रान्तिक तापमान Tc एवं क्रान्तिक दाब pc के मध्य प्रतिच्छेदन से परिभाषित होता है; इससे अधिक तापमान और दाब प्रावस्थाओं के मध्य अन्तर मिट जाता है एवं पदार्थ सुपरक्रिटिकल द्रव बन जाते हैं।
- क्रिस्टल (crystal)
- ऐसा ठोस जिसके घटक कण (जैसे परमाणु, आयन अथवा अणु) क्रमित आवर्ती सूक्ष्म संरचना में होकर एवं जालक का निर्माण करते हैं जो हर दिशा में विस्तृत होता है। ऐसे पदार्थों को अक्सर क्रिस्टलीय के रूप में वर्णित किया जाता है।
- क्रिस्टलकी (crystallography)
- किसी क्रिस्टलीय ठोस के परमाणुओं के संयोजन को ज्ञात करने से सम्बंधित रसायन विज्ञान की शाखा।
- क्रिस्टलन जल (water of crystallization)
- क्रिस्टलों में उपस्थित जल के कण। जल अथवा जलीय विलयन से क्रिस्टलन पर विभिन्न यौगिक उनके क्रिस्टलीय बनावट में जल को शामिल नहीं करते; जल के कण अक्सर रससमीकरणमितिय अनुपात में उपस्थित होते हैं और क्रिस्टल के परमाणुओं के साथ कोण बदलने पर अन्योन्य क्रिया कर सकते हैं।
- क्रिस्टलीकरण बिन्दु (crystallization point)
- हिमांक भी।
- क्रूसिबल (crucible)
- चीनी मिट्टी अथवा धातु पात्र अथवा अन्य पात्र जिसमें पदार्थ को पिघलाया जा सके अथवा बहुत अधिक तापमानों पर गर्म किया जा सके।[1]
- क्लस्टर (cluster)
- क्वथन (boiling)
- वाष्पीकरण देखें।
- क्वथनांक (boiling point)
- वह तापमान जिसपर कोई पदार्थ अपनी अवस्था को द्रव से गैस (अथवा वाष्प) में बदलता है। यह दाब पर निर्भर करता है और इसे विशेषतः किसी पदार्थ के लिए मानक परिस्थितियों के लिये दिया जाता है।
- क्वथनांक उन्नयन (boiling-point elevation)
- वह प्रक्रिया जिसमें किसी पदार्थ के क्वथनांक को अन्य पदार्थ को जोड़कर बढ़ाया जाता है।
- क्वांटम (quantum)
- क्वान्टम यांत्रिकी (quantum mechanics)
- विभिन्न परमाणुओं, अणुओं, अपरमाणुक कणों आदि के व्यवहार और संरचना का अध्ययन।
- क्वार्क (quark)
- पदार्थ का मूलभूत घटक और मूलभूत कण।
- क्षार (base)
- ऐसा पदार्थ जो प्रोटॉन ग्राही हो और जिसका पीएच मान 7.0 से अधिक हो। इसका सामान्य उदाहरण सोडियम हाइड्रॉक्साइड (NaOH) है।
- क्षार ऐनहाइड्राइड (base anhydride)
- समूह I और II के धातु तत्वों के ऑक्साइड।
- क्षार धातु (alkali metal)
- आवर्त सारणी के समूह 1 का कोई भी धात्विक तत्व: लिथियम (Li), सोडियम (Na), पोटैशियम (K), रुबिडियम (Rb), सीज़ियम (Cs), and फ़्रान्सियम (Fr)।
- क्षारीय मृदा धातु (alkaline earth metal)
- आवर्त सारणी के समूह 2 का कोई भी धात्विक तत्व: बेरिलियम (Be), मैग्नीसियम (Mg), कैल्सियम (Ca), स्ट्रोन्शियम (Sr), बेरियम (Ba), and रेडियम (Ra)।
- खनिज (mineral)
- अच्छे से सुपरिभाषित संघटन एवं विशिष्ट क्रिस्टल संरचना के साथ ठोस रासायनिक यौगिक जो शुद्ध रूप में प्राकृतिक रूप से प्राप्त होता है।[8]
- गतिकी (kinetics)
- रसायन विज्ञान का एक उपक्षेत्र जिसमें अभिक्रिया दर का अध्ययन होता है।
- गतिज ऊर्जा (kinetic energy)
- किसी वस्तु की गति के कारण उसकी ऊर्जा।
- गलन (melting)
- किसी पदार्थ का ठोस से द्रव में प्रावस्था संक्रमण।
- गलनक्रांतिक मिश्रण (eutectic mixture)
- दो अथवा अधिक पदार्थों को समाहित करने वाला ठोस विलयन जिसका सामूहिक गलनांक मिश्रण के किसी भी सम्भव घटक से कम हो।[1]
- गलनांक (melting point)
- किसी पदार्थ का वह तापमान जिसपर पदार्थ की अवस्था ठोस से द्रव में बदलती है। यह दाब पर निर्भर करता है और किसी दिये गये पदार्थ के लिए मानक परिस्थितियों के लिए उल्लिखित होता है। किसी पदार्थ का गलन बिन्दु इसके हिमांक के समान होता है।
- गिब्स ऊर्जा (Gibbs energy)
- वह मान जो किसी अभिक्रिया के स्वतः होने का सूचक हो। सामान्यतः प्रतीक चिह्न G से लिखते हैं।
- गै-लुसैक नियम (Gay-Lussac's law)
- फ़्रांसीसी रसायन विज्ञानी जोसेफ लुई गे-लुसाका द्वारा व्युत्पन दो सम्बंधों में प्रत्येक में काम आने वाले रासायनिक नियम, यद्यपि उनका नाम मुख्यतः उनके आयतन को संयुक्त करने वाले नियमों के लिए लागू किया जाता है।
- गैल्वानी सेल (galvanic cell)
- बैट्री का एक प्रकार जो लवण सेतु से जुड़े दो भिन्न-भिन्न धातुओं के विद्युत रसायनों से बना हो।
- गैस (gas)
- पदार्थ की चार मूलभूत अवस्थाओं में से एक जो अधिक ऊर्जा वाले कणों के रूप में चिह्नित की जाती है और इससे पात्र भर जाता है लेकिन इसका आकार अथवा आयतन निश्चित नहीं होता।
- गैस वर्णलेखिकी (gas chromatography)
- विश्लेषी रसायन में काम आने वाले वर्णलेखन का एक प्रकार जिसमें अपघटन रहित वाष्पन वाले रासायनिक यौगिकों को विलगित करके विश्लेषित करता है। गैस वर्णलेखिकी को अक्सर पदार्थ की शुद्धता के परीक्षण के काम में लिया जाता है जिसमें मिश्रण के भिन्न-भिन्न यौगिकों की सापेक्ष मात्रा का मापन एवं अज्ञात पदार्थ की पहचान भी शामिल है।
- गोल पेंदे का फ्लास्क (round-bottom flask)
- ग्राम-परमाणु (gram-atom)
- किसी तत्व के एक ग्राम-परमाणु को इसके 6.023X10^23 परमाणुओं के संग्रह से परिभाषित किया जाता है।
- ग्रीन्यार अभिक्रमक (Grignard reaction)
- घनत्व (density)
- घर्षित कांच संधि (ground glass joint)
- एक ऐसा उपकरण जिसके दो टुकड़ों को रिसाव-रहित कांच के बर्तन के साथ शीघ्रता एवं आसानी से फिट किया जा सके एवं घर्षित कांच के फलक व अक्सर विशिष्ट रूप से निर्मित शंकवाकार टेपर शामिल होते हैं।
- चंचलता (lability)
- चार्ल्स का नियम (Charles's law)
- जब किसी शुष्क गैस का दाब नियत रखा जाता है तो उसका केल्विन पैमाने पर तापमान उसके आयतन के अनुक्रमानुपाती होता है।
- चालक (conductor)
- कोई भी वस्तु अथवा पदार्थ जो एक अथवा अधिक दिशाओं में विद्युत धारा के प्रवाह को अनुमत करता है। विद्युतरोधी से अलग।
- चुंबकीय क्वान्टम संख्या (magnetic quantum number)
- जंग (rust) 
- जल (water)
- रासायनिक सूत्र H2O वाला एक ध्रुवीय अजैविक यौगिक जो मानक ताप एवं दाब पर स्वादहीन, गंधहीन और रंगहीन द्रव होता है, यद्यपि यह पृथ्वी की सतह पर ठोस और गैस प्रावस्थाओं में भी प्राकृतिक रूप से पाया जाता है। यह पृथ्वी पर सबसे प्रचुर मात्रा में पाया जाने वाला पदार्थ है और अतः सभी रासायनिक एवं जैविक निकायों का कल्पित रूप से अभिन्न भाग है। जल को विभिन्न पदार्थों के साथ इसकी अन्तर्निहित घुलने की क्षमता के कारण अक्सर "सार्वत्रिक विलायक" के रूप में वर्णित किया जाता है।
- जलयोजन अभिक्रिया (hydration reaction)
- जलीय (aquation)
- वह प्रक्रिया जिससे जल के अणु घुलते अथवा आयनों के साथ उपसहसंयोजी संकुल निर्मित करते हैं।[1]
- जलीय (hydrous)
- जो जल अणु को रखता है अथवा शामिल करता है, विशेषतः क्रिस्टलन जल को सन्दर्भित करता है। निर्जल से विपरीत।
- जलीय विलयन (aqueous solution)
- एक ऐसा विलयन जिसमें विलायक जल हो। रासायनिक समीकरण में रासायनिक सूत्र के पहले (aq) लगाकर इसे निरूपित किया जाता है।
- जलीय विश्लेषण (hydrolysis)
- रासायनिक आबंध को जल के संयोजन से तोड़ना।
- जस्ता (zinc)
- परमाण्विक संख्या 30 और परमाण्विक चिह्न Zn के साथ धात्विक रासायनिक तत्व।
- उभयाविष्ट आयन अथवा त्स्विटर आयन (zwitterion)
- एक रासायनिक पदार्थ जिसका कुल आवेश शून्य है और अतः यह वैद्युतिक उदासीन है। लेकिन इसके अन्दर धनात्मक एवं ऋणात्मक आवेश हैं अतः पदार्थ के घटक आवेश आंशिक रूप से अपने उपर औपचारिक आवेश रखते हैं।
- जालक (lattice)
- क्रिस्टलीय द्रव अथवा ठोस के अणुओं अथवा परमाणुओं की अद्वितीय व्यवस्था।
- जालक ऊर्जा (lattice energy)
- जीवरसायन (biochemistry)
- जैविक निकाय अथवा जीवों का रासायनिक अध्ययन करने वाला विषय।
- जूल (joule अथवा J)
- ऊर्जा की एसआई इकाई का मात्रक जिसका प्रतीक चिह्न J है। एक जूल को एक न्यूटन-मीटर से परिभाषित किया जाता है। 
- जैविक क्षार (organic base)
- क्षारीय गुणधर्मों के साथ कोई कार्बनिक यौगिक। कार्बनिक अम्ल से विपरीत।
- ज्यामितीय समावयवता (cis–trans isomerism)
- टिण्डल प्रभाव (Tyndall effect)
- कोलॉइडी अथवा निलंबित कणों के साथ प्रकाश का प्रकीर्णन प्रभाव। 
- टॉर (torr)
- 133.322 पास्कल अथवा 1.3158×10−3 वायुमण्डल दाब के समान मापन इकाई।
- ट्रांसयूरेनिक तत्व (transuranic element)
- परमाणु क्रमांक 92 से अधिक वाला (आवर्त सारणी में यूरेनियम के बाद आने वाले) कोई भी तत्व। प्राकृतिक परिस्थितियों में कोई भी ट्रांसयूरेनिक तत्व स्थायी नहीं होता है।
- ठोस (solid)
- पदार्थ की चार मूलभूत अवस्थाओं में से एक जिसे सापेक्षिकीय रूप से कम ऊर्जा वाले कणों के रूप में उल्लिखित किया जाता है एवं जिसके कण निश्चित आकृति एवं आयतन के साथ दृढ़ संरचना में एक दूसरे से बंधे होते हैं। यंग मापांक देखें।
- ठोस प्रावस्था निष्कर्षण (solid-phase extraction अथवा SPE)
- डायास्टीरियोमर (diastereomer) अप्रतिबिंबी त्रिविम समावयव भी।
- डी-खण्ड (d-block)
- डेंटीसीटी (denticity)
- एकल संलग्नी में दाता समूहों की संख्या जो उपसहसंयोजक यौगिक में केन्द्रीय परमाणु के साथ बंधे होते हैं।
- ड्यूअर फ्लास्क (Dewar flask)
- निर्वात फ्लास्क देखें।
- तत्व (element)
- एक तरह के परमाणुओं का समूह जिनके आण्विक नाभिक में प्रोटॉनों की संख्या समान होती और अतः परमाणु क्रमांक समान रहता है। रासायनिक तत्व ब्रह्माण्ड में पूरा सामान्य पदार्थ संगठित करते हैं; अब तक 118 तत्वों को पहचाना जा चुका है और उनके विभिन्न रासायनिक गुणधर्मों के अनुसार तत्वों की आवर्त सारणी में सूचिबद्ध किया जा चुका है।
- तत्वों की आवर्त सारणी (periodic table of the elements)
- रासायनिक तत्वों को उनके परमाणु क्रमांक, इलेक्ट्रॉन विन्यास और अन्य रासायनिक गुणधर्मों के क्रम में व्यवस्थित एक सारणी रूप, इसके स्वीकृत रूप को आवर्त नियम कहते हैं और रसायन विज्ञानी विभिन्न तत्वों के सम्बंधो की व्युत्पन्न करते हैं और इसी तरह से अज्ञात अथवा कृत्रिम तत्वों के गुणधर्म और व्यवहार को प्रागुक्त किया जाता है। तत्वों की पहली आवर्त सारणी वर्ष 1869 में रूसी रसायन विज्ञानी डेमीत्रि मेडेलीफ़ ने प्रकाशित की थी।
- तनु अम्ल (weak acid)
- विलायक में मिलाने पर विशेषतः वियोजित होने वाले अम्ल क्योंकि अभिक्रिया के अनुसार नहीं मिलने वाले की सान्द्रता पर्याप्त रूप से सार्थक मात्रा उपलब्ध होने पर भी साम्य तक पहुँचता है; इसका एक उदाहरण एसिटिक अम्ल (CH3COOH) है। प्रबल अम्ल के विपरीत।
- तनु क्षार (weak base)
- तनूकरण (dilution)
- तन्यता (ductility)
- किसी पदार्थ की उस क्षमता का मापन जो टूटने से पहले प्लास्टिक विकृति से गुजर सकता है, सामान्यतः इसे प्रतिशत दीर्घीकरण अथवा लचीलापन परीक्षण से प्रतिशत क्षेत्रफल अपचयन के रूप में वर्णित किया जाता है जिसे लोकप्रिय रूप में किसी पदार्थ को तार के रूप में बदलने की क्षमता के रूप में पहचाना जाता है।
- तरंग फलन (wave function)
- त्रिविम समष्टि में इलेक्ट्रॉन की स्थिति को वर्णित करने वाला गणितीय फलन।
- ताप-विघटन (pyrolysis)
- किसी पदार्थ का अक्रिय परिवेश में उच्च तापमान पर उष्ण अपघटन जैसे निर्वात गैस।
- तापमान (temperature)
- किसी निकाय के घटक स्थूल कणों की यादृच्छिक गति की औसत गतिज ऊर्जा के मापन का अनुक्रमानुपाती मापन। तापमान की एसआई इकाई मूलभूत इकाइयों में आती है और इसे केल्विन कहते हैं।
- तापमापी (thermometer)
- तापमान के मापन के लिए काम लिया जाने वाला उपकरण।
- त्रि-आबंध (triple bond)
- एक आबंध जिसमें तीन इलेक्ट्रॉन युग्म एक सहसयोंजी साझाकरण में शामिल हों (उदाहरण के लिए, द्विपरमाणुक नाइट्रोजन अणु, N2, त्रि-आबंध के साथ दो नाइट्रोजन परमाणुओं से बना होता है)।
- त्रिअंगी पदार्थ (ternary compound)
- एक रासायनिक यौगिक जिसमें तीन अलग-अलग तत्व शामिल हों।[1]
- त्रिक बिन्दु (triple point)
- ऐसा बिन्दु जहाँ तीनों प्रावस्थाओं के लिए तापमान और दाब समान हों। जल इसके लिए विशेष प्रावस्था आरेख रखता है।
- त्रिविम रसायन (stereochemistry)
- त्रिविम समावयवी (stereoisomer)
- समरूप रासायनिक संघटन के साथ समावयव लेकिन परमाणुओं के आकाशीय विन्यास में भिन्नता रखते हों।
- दर अभिक्रिया (rate equation)
- दर निर्धारक पद (rate-determining step)
- रासायनिक अभिक्रिया का सबसे धीमा पद जो एक से अधिक चरण में शामिल हो। इस चरण से कुल अभिक्रिया दर का निर्धारण होता है।[1]
- दहन (combustion)
- किसी ऑक्सीकारक और ईंधन के मध्य होने वाली ऊष्माक्षेपी अभिक्रिया जिसमें बड़ी मात्रा में ऊष्मा एवं सामान्यतः प्रकाश भी निर्मित होता है।
- दहनांक अथवा ज्वलनांक (fire point)
- वाष्पशील पदार्थों के लिए वह न्यूनतम तापमान जिसपर मानक आकार की खुली ज्वाला से प्रज्वलित करने पर उसकी वाष्प कम से कम पाँच सेकेंड तक लगातार जलेगा।[9] दहन बिन्दु को प्रज्वलन-तापन के साथ भ्रमित न करें, जो कि थोड़ा सा कम तापमान होता है और पदार्थ संक्षिप्त रूप से प्रज्वलित होता है लेकिन वाष्पन पर्याप्त स्थायी दर से प्राप्त नहीं होता है।
- दाब (pressure)
- किसी वस्तु के इकाई क्षेत्रफल वाले पृष्ठ पर लम्बवत दिशा में लगने वाले बल को ही दाब कहते हैं। दाब का एसआई मात्रक पास्कल (Pa) है, यद्यपि रसायन विज्ञान में दाब की अन्य इकाइयाँ भी आम तौर पर काम में ली जाती हैं।
- दुर्लभ मृदा तत्व (rare-earth element)
- स्कैण्डियम तथा इट्रियम सहित, लैन्थनाइड श्रेणी (परमाणु क्रमांक 57 से 71 तक) के 17 लगभग अभेद्य, चाँदी जैसे श्वेत, नरम, भारी धात्विक तत्वों में से कोई भी।
- द्रव (liquid)
- पदार्थ की मूलभूत चार अवस्थाओं में से एक जिसके तरल कण लगभग असंपीड्य होते हैं जिससे आयतन समान रहता है लेकिन आकृति नहीं।
- द्रव–द्रव निष्कर्षण (liquid–liquid extraction अथवा LLE)
- द्रवण (liquefaction)
- द्रवणांक (liquefaction point)
- गलनांक देखें।
- द्रव्यमान (mass)
- भौतिक पदार्थ का एक गुणधर्म जो नेट बल लगने पर उत्पन्न त्वरण में लगने वाले प्रतिरोध का मापन करता है। द्रव्यमान का एसआई मात्रकों में मूलभूत मात्रक किलोग्राम (kg) है।
- द्रव्यमान अंश (mass fraction)
- द्रव्यमान संख्या (mass number अथवा A)
- परमाणु के नाभिक में उपस्थित प्रोटॉनों और न्यूट्रॉनों (इनको संयुक्त रूप से न्यूक्लिऑन भी कहते हैं) की कुल संख्या। इससे परमाणु का परमाणु द्रव्यमान ज्ञात किया जाता है। समान रासायनिक तत्व के समस्थानिकों की द्रव्यमान संख्या बदल जाती है और अक्सर ऐसे तत्वों के विशिष्ट समस्थानिक को पहचानने के लिए उनके नामों के पश्चात् (कार्बन-12 के रूप में) लिखा जाता है अथवा तत्व के प्रतीक के बायें तरफ पादांक के रूप में (12C के रूप में) लिखा जाता है।
- द्रव्यमान संरक्षण का नियम (law of conservation of mass)
- द्रव्यमान सांद्रण (mass concentration)
- द्रव्यमान स्पेक्ट्रममिति (mass spectrometry अथवा MS)
- आयनन के लिए किसी रासायनिक नमूने पर इलेक्ट्रॉनों की बौछार करके आयनों के द्रव्यमान-आवेश अनुपात को मापन करने की एक विश्लेषी तकनीक; इस तकनीक में आयनों के आवेशित खंडों को विद्युत् और चुम्बकीय क्षेत्र लगाकर अलग कर लिया जाता है एवं अज्ञात पदार्थ की समस्थानिक पहचान अथवा तात्विक पहचान ज्ञात कर सकते हैं तथा/अथवा इससे अणु के अन्दर इनकी संरचना या पहचान समझी जा सकती है। इन परिणामों को द्रव्यमान स्पेक्ट्रम के रूप में प्रस्तुत किया जाता है, ऐसा आरेख जिसमें आयन सिग्नल को द्रव्यमान-आवेश अनुपात के फलन के रूप में आरेखित किया जाता है।
- द्रोणिका (cuvette)
- स्पेक्ट्रमिकी प्रयोगों में काम आने वाला कांच का पात्र। यह सामान्यतः प्लास्टिक, कांच अथवा क्वार्ट्ज़ से निर्मित होता है और जहाँ तक सम्भव हो इसे साफ-सुथरा होना चाहिए।
- द्वि-आबन्ध (double bond)
- दो इकेट्रॉनों के जोड़ों के सहसंयोजी साझाकरण वाला एक आबंध।
- द्वि-ध्रुवी आबंध (dipolar bond)
- द्वि-परमाणुक (diatomic)
- समान अथवा भिन्न तत्वों के दो परमाणुओं से निर्मित। एकपरमाण्विक और बहुपरमाणुक से अलग।
- द्वि-परमाणुक अणु (diatomic molecule)
- समान अथवा भिन्न तत्वों के दो परमाणुओं से मिलकर बना कोई अणु।
- द्वि-प्रतिस्थापन अभिक्रिया (double-replacement reaction)
- द्वितय (dimer)
- दो एकलकों को रासायनिक आबंधों से जोड़कर बनने वाला स्वल्पलक जो प्रबल अथवा दुर्बल, सहसंयोजी अथवा अंतराअणुक के परिवर्तित हो सकते हैं। होमोडीमर में दो समरूप अणु शामिल होते हैं; हेटेरोडिमर में दो अलग-अलग अणु शामिल होते हैं।
- द्वितीय कोटि अभिक्रिया (second-order reaction)
- द्विध्रुव (dipole)
- विद्युत् आवेश का विद्युत् अथवा चुम्बकीय पृथक्करण।
- द्विध्रुव आघूर्ण (dipole moment)
- ध्रुवीय सहसंयोजक आबंध की ध्रुवता।
- धनाग्र (anode)
- 1. एक इलेक्ट्रोड जिसके माध्यम से पारंपरिक विद्युत धारा (धनायनों का प्रवाह) ध्रुवीय विद्युत् परिपथ में प्रवेश करती है।
- 2. वैद्युत-रासायनिक सेल का वो तार अथवा प्लेट जिसके पास धनावेशों की पर्याप्त मात्रा हो। ऋणावेशित कण अथवा ऋणायन हमेशा धनाग्र/एनोड की तरफ गति करते हैं। कैथोड से विपरीत।
- धनायन (cation)
- धनावेशित आयन।
- धातु (metal)
- रासायनिक तत्व जो विद्युत और ऊष्मा दोनों के अच्छे चालक होते हैं तथा जो शीघ्रता से अधातुओं के साथ आयनी आबन्ध एवं धनायन निर्मित करते हैं।
- ध्रुवण घूर्णकता (optical activity)
- ध्रुवीयता (polarity)
- नाइट्रोजन (nitrogen)
- नाभिकीय (nuclear)
- परमाण्विय नाभिक से अथवा का सम्बंधित।
- नाभिक (nucleus)
- परमाणु का केन्द्र जो न्यूट्रॉनों और प्रोटॉनों से मिलकर बना होता है एवं नेट धनात्मक विद्युत आवेश रखता है।
- नाभिकरागी (nucleophile)
- कोई परमाणु अथवा अणु जो दूसरे परमाणु अथवा अणु को इलेक्ट्रॉन युग्म दान कर सकता है। मुक्त इलेक्ट्रॉन युग्म के साथ सभी अणु अथवा आयन अथवा कम से कम एक पाई बंध नाभिकरागी के रूप में कार्य कर सकता है जो अन्य इलेक्ट्रॉन न्यूनता की जातियों के क्षेत्र आकर्षित होता है; नाभिकरागी को समाहित करने वाली रासायनिक अभिक्रिया में इलेक्ट्रॉनरागी को इलेक्ट्रॉन युग्म दान किया जाता है तो इसे नाभिकरागी आक्षेप के रूप में सन्दर्भित किया जा सकता है। क्योंकि ये इलेक्ट्रॉनों का दान करते हैं अतः परिभाषा के अनुसार नाभिकरागी लूइस क्षार हैं।
- नाभिकीय चुंबकीय अनुनाद स्पेक्ट्रमिकी (nuclear magnetic resonance spectroscopy)
- अज्ञात यौजकों को पहचान्नने में उपयुक्त ऐसी तकनीक जो निश्चित परमाण्वीय नाभिक के चुम्बकीय गुणधर्मों को काम में लेती है। नाभिकीय चुंबकीय अनुनाद स्पेक्ट्रमिकी को अक्सर एनएमआर अथवा NMR के रूप में संक्षिप्तिकरण किया जाता है।
- नाभिकीय तत्वान्तरण (nuclear transmutation)
- नाभिकीय रसायन (nuclear chemistry)
- रसायन विज्ञान की वह शाखा जिसमें रेडियोऐक्टिवता सहित परमाण्वीय नाभिक से सम्बंधित गुणधर्मों और विभिन्न प्रक्रियाओं का अध्ययन किया जाता है।
- निक्षालन (elution)
- एक पदार्थ को विलायक से धोकर दूसरे से अलग करने की प्रक्रिया। निक्षालन की प्रक्रिया विश्लेष्य को समाहित करने वाले विलयन को अधिशोषण आधात्री संरचना में चलाया जाता है जो विश्लेष्य अणुओं को चयन करके बांध लेता है और उसके बाद अधिशोषण/विश्लेष्य यौगिक को विलायक से धोया जाता है, इस प्रक्रिया को निक्षालन कहा जाता है। विलायक अणु अधिशोषण के द्वारा विश्लेष्य को हटा देते हैं एवं विश्लेष्य को अब निक्षालन के लिए अथवा विश्लेषण के लिए यौगिक से अलग किया जाता है।
- निक्षेपण (deposition)
- किसी विलयन अथवा मिश्रण में कणों का समागम।
- नियमनिष्ठ आवेश (formal charge अथवा FC)
- किसी अणु में किसी परमाणु को समुनदेशित विद्युत आवेश जो प्रत्येक परमाणु की आपेक्षिक विद्युत्-ऋणात्मकता के विपरीत सभी परमाणुओं के मध्य सभी आबंधों में इलेक्ट्रॉन समान रूप से साझा होते हैं। किसी अणु के परमाणु के नियमनिष्ठ आवेश की से गणना की जाती है जहाँ उदासीन परमाणु की प्रारम्भिक अवस्था में संयोजकता इलेक्ट्रॉनों की संख्या है; अणु में आबंधों में भाग नहीं लेने वाले परमाणु में संयोजकता इलेक्ट्रॉनों की संख्या; और अणु के अन्य परमाणुओं के साथ आबंधों में इलेक्ट्रॉनों की संख्या है।
- निर्जल (anhydrous)
- जिसमें जल का कोई भी अणु नहीं हो, विशेषतः जल के जलयोजन को सन्दर्भित करता है।[3] क्योंकि रसायन विज्ञान में विभिन्न प्रक्रियायें जल की उपस्थिति में बाधित होती हैं अतः क्रान्तिक महत्त्व की स्थिति में अक्सर जलरहित अभिकारकों और तकनीकों को काम में लिया जाता है। निर्जल यौगिक धीरे धीरे वायुमण्डल से जल को अवशोषित कर लेते हैं। जलीय से अलग।
- निर्वात फ्लास्क (vacuum flask)
- दो फ्लास्कों अथवा अन्य बरतनों वाला एक संग्रह पात्र, जो एक दूसरे के अन्दर रखे हों और गरदन से जुड़े हों, विशेष रूप से इनके मध्य के भाग से हवा को खाली करके इसे लगभग निर्वात बनाया जाता है जो पात्र के आन्तरिक भाग और भिन्न वातावरण वाले बाहरी भाग के मध्य ऊष्मा के स्थानान्तरण को पर्याप्त रूप से कम कर देता है। निर्वात फ्लास्कों में इनके अन्दर रखे सामान को बाहरी वातावरण के विपरीत बहुत लम्बे समय तक ठण्डा अथवा गरम रखा जा सकता है।
- निलंबन (suspension)
- एक विषमांगी मिश्रण जिसमें ठोस कण इतनी मात्रा में हों कि अवसादन हो जाये और इससे तरल में ऐसे कण अलग होकर नीचे बैठ जायें एवं समय के साथ समान रूप से वितरित न रहें। निलंबन में विलय घुलता नहीं है लेकिन विलायक में परिक्षेपित अथवा निलंबित रहता है एवं केवल यांत्रिक विधि से और क्षणिक रूप से मिलता है। कोलॉइड और विलयन से विपरीत।
- निश्चेष्टकरण (passivation)
- निष्कर्षण (extraction)
- चयनित विलेयता के द्वारा मिश्रण से किसी घटक को अलग करने की प्रक्रिया।[1] वितरण भी देखें।
- आधात्री से विश्लेष्य घटक को अलग करना।
- निस्यंदन अथवा फिल्टरन (filtration)
- कोई भी भौतिक, जैविक अथवा रासायनिक संक्रिया जिसमें बड़े कणों (सामान्यतः ठोस पदार्थ) को छोटे कणों (अक्सर तरल) से अलग करने के लिए मिश्रण को जालक संकुल संरचना से गुजारा जाता है जिसमें पर्याप्त रूप से छोटे कण इससे निकल जाता हैं, इस माध्यम जालक को फिल्टर अथवा निस्यंदक कहते हैं। तरल अथवा छोटे कण जो फिल्टर से निकल जाते हैं उन्हें निस्यंद कहते हैं।
- नैज गुणधर्म (intrinsic property)
- न्यूक्लाइड (nuclide)
- परमाणु का वह भाग जो इसकी द्रव्यमान संख्या, परमाणु क्रमांक और नाभिकीय ऊर्जा अवस्था को निर्धारित करता है तथा यह निर्धारित करता है कि प्रेक्षण के लिये इसकी औसत आयु पर्याप्त है।
- न्यूक्लिऑन (nucleon)
- परमाण्वीय नाभिक के घटक के रूप में या तो प्रोटॉन या फिर न्यूट्रॉन।
- न्यूट्रॉन (neutron)
- अवपरमाणुक कणों का एक प्रकार जो वैद्युत उदासीन होता है और उसपर कोई नेट आवेश नहीं होता।
- पदशः अभिक्रिया (stepwise reaction)
- द्रव्य (matter)
- कोई पदार्थ जिसमें द्रव्यमान होता है और यह आयतन के रूप में जगह घेरता है।
- पदार्थ की अवस्थाएँ (state of matter)
- विशिष्ट, सजातीय, सुक्ष्म रूप की पदार्थ में मौजूद स्थितियाँ। पदार्थ की ठोस, द्रव, गैस और प्लाज़्मा चार पारम्परिक अवस्थायें और जो अच्छे से विख्यात हैं। प्रावस्था भी देखें।
- पदार्थ की मात्रा (amount of substance)
- किसी दिये गये पदार्थ के नमूने में विविक्त कणों (जैसे अणु, परमाणु, आयन, इलेक्ट्रॉन अत्गवा परमाण्वीय-पैमाने वाला अन्य कुछ) की संख्या को अवोगाद्रो संख्या से भाग देने पर प्राप्त संख्या। पदार्थ की मात्रा का एसआई प्रणाली में मूलभूत मात्रक मोल (mol) है।
- परतंत्र चर (dependent variable)
- परम शून्य (absolute zero)
- ऊष्मागतिक तापक्रम पैमाने पर किसी निकाय के निम्नतम मान अथवा शून्य केल्विन की सैद्धान्तिक स्थिति, जिसमें निकाय न ही तो ऊर्जा उत्सर्जित करता है अथवा न ही अवशोषित करता है (अर्थात् सभी परमाणु विरामावस्था में हैं)। आदर्श गैस नियम के बहीर्वेशन से, अन्तरराष्ट्रीय रूप से स्वीकृत परम शून्य मान −273.15 °से. (−459.67 °फ़ै; 0.00 के) है।
- परमाणु (atom)
- रासायनिक तत्व की वह छोटी से छोटी इकाई जिसका मध्य भाग नाभिक प्रोटोनों और न्यूट्रोनों से मिलकर तथा नाभिक के चारों और इलेक्ट्रॉनों का परिक्रमण होता है।
- परमाणु कक्षक (atomic orbital)
- किसी एकल परमाणु का वह क्षेत्र जिसमें एक या एक से अधिक इलेक्ट्रॉन पाये जा सकते हैं (एक अणु में इसका विरोध होता है)।
- परमाणु क्रमांक (atomic number) (Z)
- किसी दिये गये रासायनिक तत्व के परमाणु के नाभिक में पाये जाने वाले प्रोटॉनों संख्या। यह नाभिक की आवेश संख्या के समान होता है और आवर्त सारणी में प्रत्येक रासायनिक तत्व को अद्वितीय रूप से पहचानने के लिए काम में लिया जाता है।
- परमाणु त्रिज्या (atomic radius)
- परमाणु द्रव्यमान (atomic mass)
- किसी परमाणु का द्रव्यमान, सामान्यतः इसे एकीकृत परमाण्वीय द्रव्यमान इकाई में लिखा जाता है और द्रव्यमान संख्या के तुल्य होता है।
- परमाणु भार (atomic weight)
- सापेक्ष परमाणु द्रव्यमान देखें।
- परमाण्वीय द्रव्यमान मात्रक (atomic mass unit)
- एकीकृत परमाण्वीय द्रव्यमान मात्रक देखें।
- परासरण दाब (osmotic pressure)
- परिक्षेपण (dispersion)
- एक निकाय जिसमें किसी पदार्थ के कण किसी अन्य पदार्थ की सतत प्रावस्था में वितरित होते हैं; दोनों प्रावस्थायें पदार्थ की समान अथवा भिन्न अवस्था में हो सकती हैं। अवसादन के लिए पर्याप्त बड़े कणों का परिक्षेपण निलंबन कहलाता है जबकि छोटे कणों के लिए इसे कोलॉइड अथवा विलयन कहते हैं।
- परिशुद्धता (precision)
- प्रेक्षणों अथवा बहु-प्रायोगिक परीक्षणों के परिणाम एक दूसरे के कितने निकट हैं। यथार्थता से तुलना करें।
- पर्यावरण रसायन विज्ञान (environmental chemistry)
- पाई बंध (pi bond)
- पायस अथव इमल्शन (emulsion)
- एक तरह का कोलॉइड जिसमें द्रव के छोटे कण दूसरे द्रव में परिक्षेपित होते हैं; उदाहरण के लिए तेल में जल का परिक्षेपण, अथवा जल में तेल का परिक्षेपण। इमल्शन को स्थायी बनाने के लिए पायसीकारक के रूप में अतिरिक्त पदार्थ जोड़ा जाता है जिसमें द्रवरागी और द्रव-विरागी दोनों तरह के अणु होते हैं।[1]
- पार्श्व शृंखला (side chain)
- एक रासायनिक प्रतिस्थापी समूह जो बड़े अणु के मुख्य भाग अथवा "रीढ़" से जुड़ा हो; विशेषतः स्वल्पलक अथवा बहुलकीय हाइड्रोकार्बन शृंखला जो वृहदणु की लम्बी मुख्य शृंखला शाखायें बन्द होती हैं एवं जैसा कि जीवरसायन और अकार्बनिक रसायन में काम में आते हैं।
- पास्कल (pascal अथवा Pa)
- पिपेट (pipette)
- एक प्रयोगशाला उपकरण जो रसायनशास्त्र, जीवविज्ञान और चिकित्साविज्ञान में किसी द्रव का शुद्धता से मापित किया हुआ आयतन स्थानांतरित और बांटने के काम आता है।
- पी-खण्ड (p-block)
- पीएच (pH)
- किसी जलीय विलयन की अम्लीयता अथवा क्षारीयता उल्लिखित करने के लिए काम में लिया जाने वाला लघुगणकीय पैमाना। पीएच पैमाना किसी विलयन में हाइड्रोजन आयनों की मोलर सान्द्रता के 10-आधारी लघुगणकीय मान के ऋणात्मक मानों को सन्निकटन करता है। कमरे के ताप पर शुद्ध जल उदासीन (pH = 7) होता है; वो विलयन जिनका पीऍच मान 7 से कम हो वो अम्लीय होते हैं और जिनका पीऍच मान 7 से अधिक हो वो क्षारीय होते हैं।
- पृष्ठ विज्ञान (surface science)
- पैराफिन (paraffin)
- 1. किसी भी अल्केन का रूढ़ (गैर-आईयूपीएसी) नाम।
- 2. केरोसीन के लिए अन्य नाम।
- प्रकार्यात्मक समूह (functional group)
- प्रकाश (light)
- विद्युतचुंबकीय वर्णक्रम का वो भाग जो खुली मानव आँखो से दृश्य हो।
- प्रकिण्व (enzyme)
- एक जैविक प्रोटीन उत्प्रेरक जो रासायनिक अभिक्रिया की गति को बढ़ाते हैं।
- प्रचुरता (abundance)
- प्रच्छादक (masking agent)
- रासायनिक विश्लेषण में काम आने वाला अभिकारक जो एक अथवा एक से अधिक रासायनिक जाति से अभिक्रिया करता है जो विश्लेषण में हस्तक्षेप कर सकता है।
- प्रतिघाती मध्यक (reactive intermediate)
- प्रतिबिंब रूप (enantiomorph)
- प्रतिस्थापी (substituent)
- प्रथम-कोटि की अभिक्रिया (first-order reaction)
- प्रबल अम्ल (strong acid)
- ऐसा अम्ल जो अभिक्रिया के अनुसार विलय में पूर्णतः वियोजित होता है अथवा अवियोजित जाति की सान्द्रता इतनी अधिक कम है कि इसका मापन सम्भव न हो। कोई भी अम्ल जिसके pKa का मान लगभग -2 से कम हो को सामान्यतः प्रबल अम्ल माना जाता है; इसका एक उदाहरण हाइड्रोक्लोरिक अम्ल (HCl) है। इसका विपरीत तनु अम्ल है।
- प्रबल क्षार (strong base)
- प्रभाजन (fractionation)
- एक पृथक्करण की प्रक्रिया जिसमें मिश्रण की निश्चित मात्रा को प्रावस्था संक्रमण के दौरान छोटी मात्राओं में विभाजित किया जाता है, इसे प्रभाजी के नाम से जाना जाता है जिसमें रासायनिक संघटन प्रवणता के अनुसार बदलता है। प्रभाजन की प्रक्रिया में मिश्रण के घटक यौगिकों के कुछ विशिष्ट गुणधर्मों (उदाहरण के लिए द्रव्यमान, क्वथनांक, विलेयता, इत्यादि) में सूक्ष्म अन्तरों को काम में लिया जाता है, इससे एक ही समय पर मिश्रण के दो से अधिक घटकों को एक साथ अलग करना सम्भव कर होता है। विज्ञान और तकनीकी की विभिन्न शाखाओं में प्रभाजन के विभिन्न प्रकार हैं।
- प्रभाजी (fraction)
- प्रभाजी आसवन (fractional distillation)
- आसवन द्वारा द्रवों के मिश्रण का घटकों में प्रभाजन अथवा अंशन, इसमें सामान्य रूप में लम्बा उर्ध्वाधर स्तम्भ में कांच के मनके भरे होते हैं और वह आसवन पात्र से जुड़ा होता है। मिश्रण को एक तापमान तक गर्म किया जाता है जिसपर एक अथवा अधिक यौगिक घटकों का वाष्पन होगा; वाष्प तब तक स्तम्भ में उपर जाती है जबतक कि संघनित हो जाता है और पुनः पात्र में चली जाती है, इससे एक तापमान एवं वाष्पशीलता प्रवणता निर्मित होती है जो विभिन्न प्रभाजी अनुमत करता है एवं इसका अंशाकन स्तम्भ पर किया जाता है।[1] औद्योगिक रसायन में सामान्यतः यह तकनीक भिन्न क्वथनांक वाले यौगिकों को अलग-अलग करने के लिए पर्याप्त रूप से सुग्राही होती है जो मानक दाब पर एक दूसरे से 25 °से. (45 °फ़ै) भिन्नता रखते हैं।
- प्रसामान्यता (normality)
- प्रस्वेदन (deliquescence)
- किसी पदार्थ की जल बंधुता, सामान्यतः वायुमंडल से नमी को अवशोषित करके जलीय विलयन बनाने की प्रवृत्ति से वर्णित किया जाता है। सबसे प्रबल प्रस्वेदी पदार्थ लवण होते हैं जैसे कैल्सियम क्लोराइड और पोटासियम कार्बोनेट।
- प्राकृतिक प्रचुरता (natural abundance)
- प्रावस्था (phase)
- दिक्काश का वो क्षेत्र जिसमें पदार्थ के सभी गुणधर्म आवश्यक रूप से समरूप हों अथवा पदार्थ का वह क्षेत्र जो रासायनिक रूप से समरूप, भौतिक रूप से अलग और अक्सर यांत्रिक रूप से पृथक हो। प्रावस्था शब्द को रसायन विज्ञान में विभिन्न अर्थों में काम में लिया जा सकता है; आम रूप में इसे पदार्थ की अवस्थाओं के साथ काम में लिया जाता है लेकिन पदार्थ की एक ही अवस्था के लिए भिन्न-भिन्न प्रावस्थायें उपस्थित हो सकती हैं।
- प्रावस्था संक्रमण (phase transition)
- 1. किसी रासायनिक पदार्थ का ठोस, द्रव और गैसीय अवस्थाओं एवं बहुत ही कम स्थितियों में प्लाज़्मा में रूपान्तरण।
- 2. ऐसे रूपांतरणों के घटित होने के समय बाहरी स्थितियों के मापनीय मान।
- प्रोटॉन (proton)
- धनात्मक आवेश के साथ एक अवपरमाणुक कण जो परमाणु के नाभिक के अन्दर पाया जाता है। सामान्यतः इसे H+ से लिखा जाता है।
- प्रोटॉनीकरण (protonation)
- किसी परमाणु, अणु अथवा आयन में एक प्रोटॉन (H+) को जोड़ना।
- प्लाज़्मा (plasma)
- पदार्थ की चार मूलभूत अवस्थाओं में से सबसे अधिक ऊर्जा वाले कणों वाली अवस्था जिसमें कण आंशिक अथवा पूर्णतः आयनीत होते हैं जिससे यह अन्य तीन अवस्थाओं से अलग अद्वितीय गुणधर्म एवं व्यवहार प्रदर्शित करता है। प्लाज़्मा अवस्था पृथ्वी के मुक्त फलक पर प्राकृतिक अवस्थाओं में नहीं मिलता।
- फाइ आबंध (phi bond)
- फिक के विसरण के नियम (Fick's laws of diffusion)
- फैराडे का विद्युत अपघटन का नियम (Faraday's laws of electrolysis)
- विद्युत अपघटन से सम्बंधित दो नियमों का समुच्चय जिनके अनुसार: क) किसी इलेक्ट्रोड पर स्थानान्तरित विद्युत की मात्रा उस इलेक्ट्रोड पर जमा होने वाले पदार्थ के द्रव्यमान की मात्रा के अनुक्रमानुपाती होता है; और ख) इलेक्ट्रोड पर आने वाले तात्विक पदार्थ का द्रव्यमान उस तत्व के तुल्य भार के अनुक्रमानुपाती होता है।
- फैराडे स्थिरांक (Faraday constant)
- विद्युत्-रसायन में काम आने वाली विद्युत आवेश की एक इकाई जो इलक्ट्रॉनों के 1 मोल को निरुपित करता है: 6.022 × 1023 इलेक्ट्रॉन। यह लगभग 96,500 कूलॉम (F = 96 485.339 9(24) C/mol) के समान होता है।
- फोटॉन (photon)
- विद्युतचुंबकीय विकिरण की सभी तरंगदैर्घ्यों (जैसे कि गामा किरणें और रेडियो तरंगे) का संवाहक।
- फ्लास्क (flask)
- एक ऐसा पात्र अथवा बरतन जो सामान्यतः कांच का बरतन होता है एवं जिसे प्रयोगशाला में विभिन्न कार्यों में काम आता है यथा रासायनिक अभिक्रिया के लिये उपयुक्त कक्ष, विलयन अथवा नमूने अथवा आयतनीय मापक रसायनों को बनाने, रखने अथवा संग्रहित किया जाता है। फ्लास्क विभिन्न आकारों और संरचनाओं में आते हैं लेकिन सामान्यतः मुख्य भाग के रूप में बड़े पेट वाले बरतन के रूप में होते हैं जिसके एक अथवा एक से अधिक गर्दननुमा भाग होते हैं जिनका दूसरा अथवा उपरी भाग खुला होता है।
- बफर विलयन (buffered solution)
- एक जलीय विलयन जिसमें तनु अम्ल के साथ उसका संयुग्मी क्षार अथवा तनु क्षार के साथ उसका संयुग्मी अम्ल होता है तथा सांद्र अम्ल अथवा क्षार जोड़ने पर पीएच में परिवर्तन का विरोध करता है।
- बहुपरमाणुक (polyatomic)
- समान अथवा भिन्न तत्वों के दो या दो से अधिक परमाणुओं से मिलकर बना हुआ। एकपरमाण्विक और द्वि-परमाणुक उलटा।
- बहुपरमाणुक आयन (polyatomic ion)
- एक ऐसा अणु जो दो या दो से अधिक सहसंयोजी आबंधों वाले परमाणुओं से मिलकर बना हो एवं सम्मिलित रूप से नेट विद्युत आवेश रखता हो एवं अतः आयन के रूप में कार्य करता हो।
- बाह्य गुणधर्म (extrinsic property)
- बीकर (beaker)
- एक बेलनाकार पात्र अथवा बरतन जिसका तल चपटा हो, मुख्य रूप से सामान्यतः कांच का बना होता है और प्रयोगशाला में विभिन्न कार्यों में काम आता है यथा रासायनिक अभिक्रिया के लिये उपयुक्त कक्ष, विलयन अथवा नमूने अथवा आयतनीय मापक रसायनों को बनाने, रखने अथवा संग्रहित किया जाता है। बीकरों और फ्लास्कों को उनके बाहरी बनावट से अलग-अलग समझा जाता है। बीकर में बाहरी भाग सीधा होता है जबकि फ्लास्क में यह पूर्णतः वक्राकार होता है; अधिकतर बीकरों के उपरी किनारे पर एक चोंचनुमा भाग बनाया जाता है जो बहाव में सहायक होता है।
- बुकनर फ्लास्क (Büchner flask)
- बुंग (bung)
- बेयर–लैम्बर्ट नियम (Beer–Lambert law)
- बैरोमीटर (barometer)
- वायुमंडलीय दाब के मापन के लिए काम में लिया जाने वाला एक यंत्र।
- बॉयल का नियम (Boyle's law)
- किसी नियत तापमान पर दी गयी गैस का आयतन उस गैसे पर आरोपित दाब के व्युत्क्रमानुपाती होता है।
- बोर मॉडल (Bohr model)
- ब्यूरेट (burette)
- ब्राउनी गति (Brownian motion)
- ब्रान्स्टेड-लॉरी अम्ल (Brønsted–Lowry acid)
- कोई भी रासायनिक जाति जो तेजी से प्रोटॉन का दान करती है।
- ब्रान्स्टेड-लॉरी अम्ल-क्षार अभिक्रिया (Brønsted–Lowry acid–base reaction)
- ब्रान्स्टेड-लॉरी क्षार (Brønsted–Lowry base)
- कोई भी रासायनिक जाति जो तीव्रता से प्रोटॉन ग्रहण करती है।
- ब्रैग नियम (Bragg's law)
- भूरसायन (geochemistry)
- पृथ्वी एवं भूवैज्ञानीय प्रक्रम के रसायन विज्ञान और रासायनिक संघटन का अध्ययन।
- भौतिक रसायन (physical chemistry)
- रसायन शास्त्र की वह शाखा जिसमें रासायनिक निकाय का सैद्धान्तिक, कार्यविधि एवं भौतिकी अवधारणाओं के अनुसार अध्ययन किया जाता है जैसे गति, ऊर्जा, बल, समय, उष्मागतिकी, रासायनिक साम्य और सांख्यिकीय यांत्रिकी आदि गुणधर्म। रासायनिक भौतिकी के विपरीत भौतिक रसायन मुख्य रूप से (पूर्णतः नहीं) एक स्थूल विज्ञान है जिसमें पदार्थ का बड़ी मात्रा में रासायनिक और भौतिक अन्योन्य क्रियाओं का अध्ययन किया जाता है।
- मानक ताप एवं दाब (STP)
- प्रायोगिक परिणामों के तुलनात्मक अध्ययन के लिये काम में लिया जाने वाला व्यापक ताप और दाब का मानकीकरण स्वरूप। मानक तापमान 25 डिग्री सेल्सियस (°C) और मानक दाब 100.000 किलो पास्कल (kPa) होता है। मानक स्थितियों को अक्सर मातादा अथवा एसटीपी (STP) अथवा एसएटीपी (SATP) संक्षिप्ताक्षरों के रूप में लिखा जाता है।
- मानक विलयन (standard solution)
- मिश्रण (mixture)
- दो या दो से अधिक पदार्थों से मिलकर बनाया गया ऐसा पदार्थ जो भौतिक रूप से घुल गया हो लेकिन रासायनिक रूप से नहीं मिला हो (अर्थात् रासायनिक अभिक्रिया नहीं हुई है जो मिलने वाले पदार्थों के अणुओं के मध्य अभिक्रिया करके नया पदार्थ बना सकती है।)
- मिश्रणीयता (miscibility)
- मिश्रातु (alloy)
- धातुओं अथवा धातु एवं अन्य तत्व का मिश्रण जिसमें साथ में धात्विक बंधन बन गया हो। इसके सामान्य उदाहरणों में कांसा, पीतल और प्यूटर शामिल हैं।
- मुक्त मूलक (free radical)
- मूलक देखें।
- मूलक (radical)
- कोई भी परमाणु, अणु अथवा आयन जिनमे कम से कम एक अयुग्मित संयोजकता इलेक्ट्रॉन हो। कुछ अपवादों के अतिरिक्त जिनमें अयुग्मित इलेक्ट्रॉन होते हैं, उच्च रासायनिक क्रियाशीलता रखते हैं और अतः कार्बनिक मूलक सामान्यतः लघु-कालिक होते हैं।
- मूलभूत अभिक्रिया (elementary reaction)
- कोई भी रासायनिक अभिक्रिया जिसमें एकल अभिक्रिया चरण और एकल संक्रमण-अवस्था के साथ एक अथवा अधिक रासायनिक जाति सीधे उत्पादों के निर्माण के लिए अभिक्रिया करते हैं; उदाहरण के लिए बिना किसी मध्यवर्ती के। पदशः अभिक्रिया के विपरीत।
- मृदा धातु (earth metal)
- क्षारीय मृदा धातु भी।
- मेथिलीन नील (methylene blue)
- A विषमचक्रीय अरोमैटिक यौगिक जिसका आणविक सूत्र C16H18N3SCl है।
- मैनोमीटर अथवा दाबांतरमापी (manometer)
- एक ऐसा उपकरण जिसे दाब के मापन के लिए काम में लिया जाता है, इसका आविष्कार वर्ष 1643 में इवान टाँरीसेली ने किया।
- मोल (mole अथवा mol)
- एक इकाई (चिह्न: mol) जो पदार्थ की मात्रा का मापन पदार्थ को निर्मित करने वाली इकाइयों अथवा कणों की संख्या के निरपेक्ष संख्या के रूप में करता है। एक एकल मोल में लगभग 6.022×1023 कण अथवा इकाइयाँ होती हैं।
- मोल अंश (molar fraction)
- मोलर क्षरण गुणांक (molar attenuation coefficient)
- मोलर द्रव्यमान (molar mass)
- मोलर सान्द्रता (molar concentration)
- रासायनिक जाति की सान्द्रता का एक मापन, मुख्यतः किसी विलयन में विलय, विलयन के इकाई आयतन में उपस्थित नमूने की मात्रा के शब्दों में। मोलरता को सामान्यतः मोल प्रति लिटर (mol/L) में लिखा जाता है; ठीक 1 मोल प्रति लिटर सान्द्रता वाले विलयन को सामान्यतः 1 मोलर कहा जाता है और 1 M के रूप में लिखा जाता है। मोललता से विपरीत।
- मोललता (molality)
- विलायक के इकाई द्रव्यमान में विलय की मात्रा के पदों में, विलयन में विलय की सान्द्रता का मापन। मोललता को सामान्यतः मोल प्रति किलोग्राम (mol/kg) के रूप में लिखा जाता है; 1 मोल प्रति किग्रा की सान्द्रता वाले विलयन को कभी-कभी 1 मोलल कहा जाता है। मोलरता से विपरीत।
- यथार्थता (accuracy)
- वास्तविक अथवा सत्य मान के कितना निकटा से मान का मापन किया गया है। परिशुद्धता से तुलना करें।
- यूएन संख्या (UN number)
- खतरनाक और ज्वलनशील पदार्थों को निर्देशित करने के लिए काम में ली जाने वाली चार अंकों की संख्या।
- योगज अभिक्रिया (addition reaction)
- कार्बनिक रसायन विज्ञान में जब अणु मिलकर एक बड़ा अणु निर्मित करते हैं।
- यौगिक (compound)
- दो या दो से अधिक रासायनिक आबंधो वाले तत्वों से मिलकर बना पदार्थ।
- रक्षी समूह (protective group)
- रससमीकरणमिति (stoichiometry)
- रासायनिक अभिक्रियाओं में अभिकर्मकों और उत्पादों की मात्रा की गणना। रससमीकरणमिति द्रव्यमान संरक्षण का नियम और अभिकर्मकों एवं उत्पादों की मात्रा के अक्सर धनात्मक पूर्णांकों के अनुपात के रूप में प्रेक्षित होने पर आधारित होती है जिसका तात्पर्य यह है कि यदि हमें सभी अभिकर्मकों की मात्रा अलग-अलग ज्ञात है तो उत्पादों की मात्रा की गणना की जा सकती है और इसी तरह उत्पादों से अभिकर्मकों की।
- रसायन विज्ञान (chemistry)
- एक वैज्ञानिक अध्ययन अथवा शिक्षण जिसमें विभिन्न रासायनिक तत्वों के अणुओं से मिलकर बनने वाले रासायनिक पदार्थों, यौगिकों और अणुओं का अध्ययन किया जाता है और इससे इनके संघटन, संरचना, गुणधर्म, व्यवहार और अन्य पदार्थों के साथ उनकी अभिक्रियाओं के दौरन आने वाले बदलावों को समझा जाता है।
- राउल्ट का नियम (Raoult's law)
- एक उष्मागतिकीय नियम है जिसके अनुसार द्रवों के आदर्श विलयन के प्रत्येक गैसीय घटक का आंशिक दाब का मान शुद्ध घटक के वाष्प दाब को मिश्रण में उसके मोल अंश से गुणा के बराबर होता है।
- रासायनिक अपघटन (chemical decomposition)
- एकल कण अथवा इकाई (जैसा कि एक अणु अथवा प्रतिघाती मध्यक) का दो या दो से अधिक घटकों में टूटना अथवा ऐसी रासायनिक अभिक्रिया जिसमें एक ही अभिकर्मक से दो या दो से अधिक उत्पाद प्राप्त होते हैं। रासायनिक संश्लेषण का उलट।
- रासायनिक अभिक्रिया (chemical reaction)
- एक अथवा एक से अधिक पदार्थों का एक अथवा अधिक भिन्न पदार्थों में परिवर्तन।
- रासायनिक जाति (chemical species)
- रासायनिक रूप से समरूप आण्विक इकाइयों से निर्मित रासायनिक पदार्थ अथवा पदार्थों का समुदाय जो अभिलाक्षणिक अथवा समय पैमाने के चित्रण पर समान आण्विक ऊर्जा स्तरों के समुच्चय को अन्वेषित करता है।
- रासायनिक नामकरण (chemical nomenclature)
- रासायनिक नियम (chemical law)
- रसायन विज्ञान से सम्बंधित प्राकृतिक नियम जैसे द्रव्यमान संरक्षण का नियम।
- रासायनिक पदार्थ (chemical substance)
- पदार्थ का एक रूप जिसके रासायनिक संघटन और अभिलाक्षणिक गुणधर्म स्थिर हों और उनके घटकों को किसी शुद्ध भौतिक विधि से अलग नहीं किया जा सकता (अर्थात् रासायनिक आबंधों को तोड़े बिना)। इसे अक्सर मिश्रण से विशुद्ध पदार्थ को अलग पहचानने में काम में लिया जाता है।
- पदार्थ (substance)
- रासायनिक पदार्थ भी।
- रासायनिक प्रक्रम (chemical process)
- एक या एक से अधिक रसायनों अथवा रासायनिक यौगिकों के होने वाले परिवर्तन अथवा कोई विधि जिसमें या तो प्राकृतिक रूप से या कृत्रिम रूप से, या तो स्वतः या फिर बाह्य बलों से होता है।
- रासायनिक अभियान्त्रिकी में, एक अथवा एक से अधिक रसायनों अथवा पदार्थों के संघटकों को परिवर्तित करने के लिए औद्योगिक स्तर (विशेषतः विनिर्माण में) पर काम आने वाली एक विधि।
- रासायनिक संघटन (chemical composition)
- तत्वों की सापेक्ष संख्या और पहचान जो रासायनिक यौगिकों का निर्माण करती है, इसे सामान्यतः रासायनिक सूत्र के साथ लिखा जाता है।
- रासायनिक संश्लेषण (chemical synthesis)
- एक अथवा एक से अधिक रासायनिक अभिक्रियाओं से उत्पादों को प्राप्त करने का कृत्रिम निष्पादन। आधुनिक प्रायोगिक प्रसंगों में विशिष्ट रासायनिक संश्लेषण विश्वसनीय और पुनरुत्पादनीय होती हैं।
- रासायनिक सूत्र (chemical formula)
- किसी यौगिक अथवा अणु के रासायनिक संघटन के बारे में सूचना को पूर्णतः प्रदर्शित करने के लिए कुछ वर्णों, संख्याओं और/अथवा टंकणीय चिह्नों की सहायता से अर्थपूर्ण तरिका। आनुभाविक और आण्विक सूत्र जैसे रासायनिक सूत्र किसी यौगिक के परमाणुओं के अनुक्रमानुपाती संख्या और पहचान को निरूपित कर सकते हैं और इससे रासायनिक नामों एवं संरचनात्मक सूत्रों में कम विस्तार में अच्छे से उल्लिखित किया जा सकता है।
- रिटॉर्ट (retort)
- रासायनिक पदार्थों के आसवन अथवा शुष्क आसवन के लिए काम में आने वाला उपकरण, पारम्परिक रूप से यह एक गोलीय पात्र होता था जिसके उपर लम्बी, नीचे की तरफ घुमकर पतला होने वाला भाग होता था जिसमें आसवन द्वारा वाष्प को संघनित करके दूसरे पात्र में इक्कठा किया जा सके।
- रेडियोसक्रिय क्षय (radioactive decay)
- अस्थायी परमाण्विय नाभिक की एक प्रक्रिया जिसमें विकिरण उत्सर्जित करके नाभिक अपनी ऊर्जा ह्रास करता है।
- रेडॉक्स (redox)
- रेसिमेट (racemate)
- ऐनैन्टियोमरों के युग्म का सममोलर मिश्रण जो ध्रुवण घूर्णकता प्रदर्शित नहीं करता। रेसिमेट के सूत्र अथवा रासायनिक नाम को ऐनैन्टियोमरों के पूर्वनाम (±)- अथवा प्रतीक चिह्न RS और SR से विभेद्य किया जाता है।
- रोटामापी (rotamer)
- लंदन परिक्षेपण बल (London dispersion forces)
- एक तरह का दुर्बल अंतराअणुक बल।
- लब्धि (yield)
- रासायनिक अभिक्रिया के दौरान निर्मित उत्पाद की मापने योग्य मात्रा।
- लवण (salt)
- एक या एक से अधिक ऋणायनों अथवा एक या एक से अधिक धनायनों से मिलकर बना आयनी यौगिक
- लवण सेतु (salt bridge)
- वैद्युत-रासायनिक सेल में अपचयन को ऑक्सीकारक अर्ध-सेल से जोड़ने वाला यंत्र।
- लवणीय विलयन (saline solution)
- सोडियम क्लोराइड (NaCl) को जल (H2O) में मिलाने पर बनने वाले विलयन का सामान्य नाम।
- लूइस अम्ल (Lewis acid)
- लूइस क्षार (Lewis base)
- लूइस संरचना (Lewis structure)
- लैन्थनाइड (lanthanides)
- लैन्थनम से लुटीशियम तक अर्थात् परमाणु संख्या 57 से 71 तक के धात्विक तत्वों की आवर्तिक श्रेणी।
- लोकेंट (locant)
- वर्णलेखन (chromatography)
- वर्न विकृति (tarnish)
- वाच-ग्लास (watch glass)
- रसायन विज्ञान की प्रयोगशाला में काम आने वाला काँच का एक वृत्ताकार, अवतल टुकड़ा जिसे सामान्यतः विभिन्न कामों जैसे वाष्पीकरण द्रव, भार मापन करने के समय ठोस को रखने, कम मात्रा में किसी पदार्थ को गर्म करने अथवा बीकर को ढकने के काम में लिया जाता है।
- वातन (aeration)
- किसी द्रव अथवा ठोस में हवा को मिश्रित करना।
- वान डर वाल्स बल (van der Waals force)
- अणुओं के मध्य का एक बल (आकर्षन/प्रतिकर्षण)।
- वान्ट हाफ गुणक (van 't Hoff factor)
- विलयन में कणों की मोलों की संख्या का विलय में मोलों की संख्या के साथ अनुपात।
- वाष्प (vapor)
- जब कोई पदार्थ क्रान्तिक तापमान से कम पर है जबकि यह गैस प्रावस्था में है।
- वाष्प दाब (vapor pressure)
- वाष्प से लगने वाला दाब जो किसी संवृत तंत्र में दिये गये तापमान पर अपनी संघनित प्रावस्था (ठोस अथवा द्रव) के साथ उष्मीय साम्य में होता है। यह सामान्यतः कणों के द्रव अथवा ठोस अवस्था से गैसीय अवस्था में स्वतः पलायन की प्रवृत्ति के लिए वर्णित किया जाता है और द्रव के वाष्पन दर को इंगित करने के काम में भी आता है।
- वाष्पशीलता (volatility)
- पदार्थ की गुणवत्ता जो उसके वाष्पन की दर को उल्लिखित करता है। किसी पदार्थ की उच्च वाष्पशीलता किसी दिये गये ताप और दाब पर गैस के रूप में अधिक सम्भावित है जबकि कम वाष्पशीलता वाले पदार्थ द्रव अथवा ठोस के रूप में होने की सम्भावना है; इसी तरह कम वाष्पशील पदार्थ तेजी से गैसीय अवस्था से संघनित होते हैं, जबकि अधिक वाष्पशीलता वाले धीमी गति से संघनित होते हैं।
- वाष्पीकरण (vaporization)
- द्रव से गैस में किसी पदार्थ का प्रावस्था संक्रमण।
- वाष्पीकरण बिन्दु (vaporization point)
- क्वथनांक देखें।
- वास्तविक उत्पाद (actual yield)
- विआयनन (deionization)
- आयनों को हटाने की प्रक्रिया, और जल की स्थिति में खनिज आयनों जैसे सोडियम, लोहा और कैल्सियम को हटाना।
- विकिरण (radiation)
- अवपरमाणुक कणों का उच्च ऊर्जा स्तर से निम्न ऊर्जा स्तर में परिवर्तन के समय तरंग रूप में उत्सर्जित होने वाली ऊर्जा।
- विद्युत अपघट्य (electrolyte)
- ऐसा विलयन जो निश्चित मात्रा में विद्युत् धारा का चालन करता है और स्पष्टतः दुर्बल एवं प्रबल विद्युत अपघट्यों के रूप में विभाजित हो सकते हैं।
- विद्युत आवेश (electric charge)
- विद्युत-चुम्बकीय अन्योन्य क्रिया का एक मापित गुणधर्म (कूलाम)।
- विद्युतचुंबकीय वर्णक्रम (electromagnetic spectrum)
- विद्युतचुंबकीय विकिरण (electromagnetic radiation)
- एक ऐसी तरंग जो निर्वात और पदार्थों में समान रूप से गति कर सकती है और जिसे स्वतः प्रगामी तरंग के रूप में वर्गिकृत किया जाता है।
- विद्युतरोधी (insulator)
- कोई भी पदार्थ जो विद्युत धारा के प्रवाह को अवरोधित करता है। चालक के उलट।
- विद्युतवाहक बल (विवाब अथवा electromotive force अथवा emf)
- विद्युत्-ऋणात्मकता (χ अथवा electronegativity)
- एक रासायनिक गुणधर्म जो किसी अणु की इलेक्ट्रॉनों के साझा युग्म (अथवा इलेक्ट्रॉन घनत्व) को अपनी तरफ आकर्षित करने की प्रवृति को वर्णित करता है। एक परमाणु की विद्युत्-ऋणात्मकता इसके नाभिकीय आवेश (जो इसके नाभिक में उपस्थित प्रोटोनों की संख्या के अनुक्रमानुपाती होता है) और इसके आण्विक कोश में उपस्थित इलेक्ट्रॉन एवं इनकी स्थिति (इससे नाभिक की इसके संयोजी इलेक्ट्रॉन से दूरी को प्रभावित होती है।) से प्रभावित होती है। उच्चतर परमाणु अथवा विद्युत्-ऋणात्मकता का प्रतिस्थापी इलेक्ट्रॉनों को अपनी तरफ अधिक आकर्षित करता है। जैसा की सामान्यतः इसकी गणना की जाती है, विद्युत्-ऋणात्मकता एक अकेले परमाणु का गुणधर्म नहीं है जबकि अणु में एक परमाणु का गुणधर्म है; अतः यह तत्व के रासायनिक वातावरन के अनुसार ये बदलते हैं यद्यपि इसे सामान्यतः अंतरणीय गुणधर्म माना जाता है।
- विद्युत्चुम्बकत्व (electromagnetism)
- विद्युत आवेश और वैद्युत गुणधर्मों के साथ क्षेत्र जो गतिशील अथवा अन्योन्य क्रिया करने वाले कण की राह परिवर्तित कर सकता है।
- वियोजन (dissociation)
- विलय (solute)
- विलयन का वो भाग जो विलायक में मिलाया जाता है। उदाहरण के लिए लवणीय जल के विलयन में सोडियम क्लोराइड (NaCl) विलय है।
- विलयन (dissolution)
- विलायक की विलय के अणुओं अथवा आयनों के साथ अन्योन्य क्रिया जिसमें आबंध निर्माण, हाइड्रोजन आबंधन और वान डर वाल्स बल शामिल हैं।
- विलयन (solution)
- विलय. एक समांगी मिश्रण जो {gli और विलायकों जैसे विभिन्न पदार्थों से मिलकर बना हो।}}
- विलायक (solvent)
- विलयन का वो भाग जिसमें विलय को मिलाया जाता है। उदाहरण के लिए लवणीय जल के विलयन में जल (H2O) विलायक है।
- विलायकयोजन (solvation)
- विलयन (dissolution) देखें।
- विलायकयोजन कोश (solvation shell)
- विलायकयोजित इलेक्ट्रॉन (solvated electron)
- विलेयता (solubility)
- ठोस, द्रव अथवा गैसीय विलयों का ठोस, द्रव अथवा गैसीय विलायकों में मिलने का गुणधर्म। इसे सामान्यतः संतृप्त विलयन में विलायक में मिलने वाले विलय के समानुपाती के रूप में उल्लिखित किया जाता है।
- विशिष्ट ऊष्मा धारिता (specific heat capicity)
- किसी पदार्थ के नमूने के इकाई द्रव्यमान की उष्मा धारिता अर्थात् किसी पदार्थ के नमूने की उष्मा धारिता को उस नमूने के द्रव्यमान से विभाजित करके इसे प्राप्त किया जाता है। सामान्यतः हम ऊष्मा की उस मात्रा को विशिष्ट उष्मा धारिता कहते हैं जो किसी पदार्थ के इकाई द्रव्यमान के तापमान में इकाई वृद्धि करने के लिए जो देनी होती है। विशिष्ट उष्मा धारिता का एसआई मात्रक जूल प्रति केल्विन प्रति किलोग्राम (J/K/kg) है। विशिष्ट उष्मा धारिता का मान तापमान और पदार्थ की प्रत्येक अवस्थाओं के साथ बदल जाता है।
- विश्लेषी रसायन (analytical chemistry)
- रसयनशास्त्र की वह शाखा जिसमें रासायनिक पदार्थों को अलग करने की विधि, परिमाणित करना एवं पहचाने की विधि और इनका अध्ययन किया जाता है जिसमें अवक्षेपण, निष्कर्षण, आसवन और प्रेक्षणीय विश्लेष्ण जैसी चिरसम्मत आद्र रसायनशास्त्र तकनीक और वर्णलेखन, स्पेक्ट्रोस्कोपी और विद्युत्-रसायन जैसी आधुनिक यांत्रिक तकनीक शामिल हैं।
- विश्लेष्य (analyte)
- विशिष्ट पदार्थ अथवा रासायनिक घटक जो रासायनिक विश्लेषण की रूचि का हो।
- विसरण (diffusion)
- उच्च सान्द्रता क्षेत्र से निम्न सान्द्रता क्षेत्रा की तरफ परमाणुओं अथवा अणुओं की कुल गति। विसरण कणों के यादृच्छिक भ्रमण पर निर्भर करता है तथा विसरित होने वाले पदार्थों के रासायनिक विभव की प्रवणता द्वारा संचालित होता है; अतः यह मिश्रण के रूप में परिणत होता है अथवा बिना बड़े हिस्से की गति के द्रव्यमान परिवहन होता है।
- विस्तारात्मक गुणधर्म (extensive property)
- ऐसी भौतिक राशि जिसका मान निकाय के आकार जो इसे वर्णित करता है अथवा निकाय में पदार्थ की मात्रा के अनुक्रमानुपाती होता है। इसके उदाहरणों में द्रव्यमान, आयतन, एन्थैल्पी और एन्ट्रॉपी शामिल हैं। अविस्तारात्मक गुणधर्म के विपरीत।
- विस्थानित इलेक्ट्रॉन (delocalized electron)
- किसी अणु, आयन अथवा ठोस धातु में कोई इलेक्ट्रॉन जो किसी अकेले परमाणु अथवा सहसंयोजी आबंध से जुड़ा हुआ न हो। यह शब्द उन इलेक्ट्रोनों के लिए भी काम में ली जा सकती है जो एरोमैटिक यौगिकों अथवा संयुग्मी निकायों में अनुनाद में शामिल हों; विद्युत चालकता में शामिल मुक्त इलेक्ट्रॉनों; अथवा स्थानीयकृत आण्विक कक्षकों के वो इलेक्ट्रॉन जो विभिन्न निकटस्थ परमाणुओं के चक्कर लगाते हैं।
- विस्फारी (dilatant)
- ऐसा पदार्थ जिसकी आकृति बदलने पर आयतन परिवर्तन करने की क्षमता रखता हो।[3]
- वैद्युत संश्लेषण (electrosynthesis)
- वैद्युत-रासायनिक सेल (electrochemical cell)
- रासायनिक अभिक्रिया की धारा को काम में लेते हुये, विद्युतवाहक बल निर्मित करना।
- वोल्ट (volt अथवा V)
- विद्युत विभव, विद्युत विभवांतर और विद्युतवाहक बल की एक व्युत्पन्न इकाई, जो एकांक कूलॉम आवेश पर किये गये जूल में कार्य द्वारा परिभाषित किया जाता है।
- वोल्टमीटर (voltmeter)
- एक ऐसा उपकरण जो विद्युत सेल विभव मापन के काम में लिया जाता है।
- शर अपकर्षण (arrow pushing)
- शीतलन वक्र (cooling curve)
- शुद्ध और अनुप्रयोगिक रसायन का अंतरराष्ट्रीय संघ (International Union of Pure and Applied Chemistry अथवा IUPAC)
- रसायन विज्ञानियों का एक अंतर्राष्ट्रीय संघ जिसे रसायन विज्ञान में रासायनिक नामकरण और अन्य कार्यप्रणालियों के मानक विकास के विश्व प्राधिकरण के रूप में जाना जाता है।
- शुद्ध पदार्थ (pure substance)
- रासायनिक पदार्थ देखें।
- शृंखला अभिक्रिया (chain reaction)
- श्यानता (viscosity)
- द्रव के बहाव में प्रतिरोध का मापन।
- श्रोडिंगर समीकरण (Schrödinger equation)
- एक क्वांटम अवस्था समीकरण जो परमाणुअ के चारों तरफ इलेक्ट्रॉन के व्यवहार को निरूपित करती है।
- संक्रमण धातु (transition metal)
- एक तत्व जिसके परमाणु प्राकृतिक रूप से "d" उपकोश अपूरित प्राप्त होता है। इन सभी तत्वों को आवर्त सारणी में संयुक्त रूप से डी-खण्ड के तत्वों के रूप में समूहित किया जाता है।
- सक्रियण ऊर्जा (activation energy)
- न्यूनतम ऊर्जा जो किसी रासायनिक अभिक्रिया को परिणाम तक पहुँचने के लिए रासायनिक निकाय के महत्त्वपूर्ण अभिकर्मकों के लिए आवश्यक है।
- सक्रियता श्रेणी (activity series)
- अभिक्रिया श्रेणी देखें।
- सक्रियित संकुल (activated complex)
- नये आबन्धों के निर्माण के समय अणुओं के मध्य टक्कर के कारण निर्मित होने वाली संरचना।
- संक्षारण (corrosion)
- पदार्थों की अनुत्क्रमणीय अंतरापृष्ठीय रासायनिक अभिक्रिया, विशेषतः एक धातु का इसके परिवेश के साथ अभिक्रिया जिसमें परिवेश के घटकों के पदार्थ का उपरोक्त पदार्थ में क्षय अथवा विलयन।
- संख्या घनत्व (number density)
- दिक्काश में गणनीय वस्तुओं (परमाणु, अणु आदि) की सान्द्रता का मापन जिसे संख्या प्रति इकाई आयतन में प्रदर्शित किया जाता है।
- संघनन (condensation)
- किसी पदार्थ का गैस से द्रव में प्रावस्था संक्रमण।
- संपीड़न (compression)
- अनुदैर्घ्य तरंगो में वो क्षेत्रफल जिसमें कण पास में आते हैं या धकेले जाते हैं।
- सम-इलेक्ट्रॉनिकी (isoelectronicity)
- समान संरचनात्मक व्यवस्था (अर्थात् समान सम्बद्धता के साथ समान संख्या में परमाणु) और समान संख्या में संयोजकता इलेक्ट्रॉनों वाले दो या दो से अधिक रासायनिक जाति (परमाणुओं, अणुओं, आयनों, आदि) के भिन्न तत्वों से निर्मित होने वाली घटना। समइलेक्ट्रॉनी जाति अक्सर उनके रासायनिक गुणधर्मों की संगतता एवं पूर्वगुतता को प्रदर्शित करता है।
- समक्रिस्टल (allomer)
- एक पदार्थ जो किसी अन्य पदार्थ के साथ भिन्न रासायनिक संघटन रखता है लेकिन उनकी क्रिस्टलीय संरचना समान होती है।
- समतलन प्रभाव (leveling effect)
- अम्लों अथवा क्षारों के रासायनिक गुण्धर्मों का विलायक पर प्रभाव जो विलायक को मिलाये जाते हैं। प्रबल अम्लों की प्रबलता को विलायक की क्षारीयता से और इसी तरह प्रबल क्षार की क्षारीयता को विलायक की अम्लीयता से इस तरह समतलनीत किया जाता है, कि विलयन का प्रभावी पीएच अम्ल अथवा क्षार के वियोजन स्थिरांक के अनुसार अधिक अथवा कम हो सकता है।
- समस्थानिक (isotope)
- रासायनिक तत्व का एक विशेष रूपांतर जिसके नाभिक में न्यूट्रॉनों की संख्या भिन्न हो। किसी दिये गये तत्व के सभी समस्थानिकों के प्रत्येक परमाणु में प्रोटॉनों की संख्या समान रहती है।
- समस्थानिक बहुतायत और परमाणु भार आयोग (Commission on Isotopic Abundances and Atomic Weights अथवा CIAAW)
- समावयव (isomers)
- भिन्न संरचना अथवा दिक्काशीय व्यवस्था वाले समरूप रासायनिक सूत्रों वाले आयनों अथवा अणुओं की संरचना। समावयवों के गुणों का समरूप होना आवश्यक नहीं है। दो मुख्य प्रकार के समावयव संरचनात्मक समावयव और त्रिविम समावयव हैं।
- समावयवन (isomerization)
- समूह (group)
- तत्वों की आवर्त सारणी का उर्ध्वाधर स्तम्भ और इसमें शामिल तत्व। आवर्त से विपरीत।
- संयुग्मी अम्ल (conjugate acid)
- संयुग्मी क्षार (conjugate base)
- संयुग्मी निकाय (conjugated system)
- संयोजकता (valency)
- किसी तत्व की संयोजन क्षमता।
- संयोजकता आबंध सिद्धान्त (valence bond theory)
- किसी परमाणु के रासायनिक आबन्धों अथवा संयोजकताओं की चर्चा के साथ अणुओं के रासायनिक आबंधों की व्याख्या करने वाला सिद्धान्त।
- संयोजकता इलेक्ट्रॉन (valence electron)
- किसी परमाणु के सबसे बाहरी इलेक्ट्रॉन जो इलेक्ट्रॉन कोशों में उपस्थित होते हैं।
- संरचना सूत्र (structural formula)
- किसी विशिष्ट रासायनिक यौगिक की आण्विक संरचना और ज्यामिति का आरेखीय निरूपण जो त्रिविम दिक्काश में परमाणुओं की वास्तविक व्यवस्था को दर्शाता है। अणुओं के मध्य रासायनिक आबंधों को भी या तो परोक्ष रूप से या स्पष्ट रूप से दर्शाया जाता है। यदि संरचना सूत्र का निश्चित ज्ञान हो तो यह बहुत उपयोगी होता है क्योंकि वो रसायन विज्ञानियों को रासायनिक अभिक्रियाओं के दौरान होने वाले आण्विक अथवा संरचनात्मक बदलावों को देखने में सहायक होता है।
- संरचनात्मक समावयव (structural isomer)
- संरूपण (conformation)
- त्रिविम समावयवों के मध्य वहन भेद परमाणुओं का आकाशीय आसंजन जो सामान्य एकल-आबंधों के घूर्णन से अंतर्परिवर्तित कर सकता है।
- संलग्नी (ligand)
- आयन, प्रकार्यात्मक समूह अथवा अन्य अणु जो केन्द्रीय धातु परमाणु के साथ बंध बनाकर उपसहसंयोजक यौगिक निर्मित करते हों। ऐसे आबंध सहसंयोजी से आयनी आबंधो तक होते हैं लेकिन सामान्यतः इसमें एक अथवा अधिक संलग्नों (लिजेंडों) के इलेक्ट्रॉन युग्मों का दान धातु को होत है।
- संलयन की ऊष्मा (heat of fusion)
- संलयन की ऐन्थैल्पी भी।
- संलयन की एन्थैल्पी (enthalpy of fusion)
- संवृत तंत्र (closed system)
- संसंजन (cohesion)
- अंतराअणुक बलों के परिणाम के रूप में समरूप कणों अथवा सतहों के मध्य आकर्षण की प्रवृत्ति। आसंजन से उलट।
- सहसंयोजी आबंध (covalent bond)
- एक ऐसा आबंध जो परमाणुओं के मध्य इलेक्ट्रॉन युग्मों का साझाकरण शामिल होता है। परमाणुओं के मध्य आकर्षण और प्रतिकर्षण बलों का स्थायी संतुलन जब सहसयोंजी आबंधन के नाम से जाने वाले इलेक्ट्रॉनों का साझाकरण होता है।
- सान्द्रता (concentration)
- किसी मिश्रण की इकाई मात्रा में मिश्रण के घटकों की मात्रा अथवा प्रचुरता; उदाहरण के लिए मोलरता के रूप में जाना जाने वाला मापन जिसमें किसी विलयन के इकाई आयतन में घुले हुये विलेय की मात्रा। रसायन विज्ञान में द्रव्यमान सान्द्रता, आयतन सान्द्रता और मोलर सान्द्रता सहित भिन्न-भिन्न सान्द्रता की परिभाषायें व्यापक स्तर पर काम में आती हैं।
- साम्य (equilibrium)
- निकाय की वो अवस्था जिसमें प्रतिस्पर्धी प्रभाव साम्य में होते हैं। रासायनिक साम्य समय के साथ अभिक्रिया निकाय की उस नियत अवस्था को कहते हैं जिसमें अभिकर्मकों और उत्पादों की सान्द्रता नियत हो जाती है।
- सार्वत्रिक गैस नियतांक (ideal gas constant)
- आदर्श गैस समीकरण में अनुक्रमानुपाती नियतांक जिसका मान 0.08206 L·atm/(K·mol) होता है।
- सूक्ष्म अपकेंद्रीय नली (microcentrifuge tube)
- एक छोटी प्लास्टिक पात्र जिसे बंद किया जा सके और अल्प मात्रा में द्रव को रखने के लिए काम में लिया जाता है, सामान्यतः इसका आयतन 2 मिलीलिटर होता है।
- सूचक (indicator)
- किसी विलयन में किसी विशेष यौगिक को जोड़ना जिससे विलयन की अम्लीयता के अनुसार रंग बदल जाता है। भिन्न सूचकों के भिन्न रंग होते हैं जो भिन्न पीएच परास में प्रभावी होते हैं।
- सूत्र भार (formula weight अथवा FW)
- मोलर द्रव्यमान और अणु भार का पर्याय, गैर-आण्विक यौगिकों जैसे आयनी लवणों में अक्सर देखे जाते हैं।
- सेल विभव (cell potential)
- गैल्वानी सेल में बल जो अपचायक से ऑक्सीकारक जे माध्यम से इलेक्ट्रॉनों को खींचता है।
- सैद्धान्तिक लब्धि (theoretical yield)
- लब्धि देखें।
- सॉल (sol)
- द्रव में ठोस कणों का निलंबन जिसके कृत्रिम उदाहरणों में सॉल-जेल शामिल हैं।
- स्टीरियोजेनिक केंद्र (stereogenic center)
- स्थितिज ऊर्जा (potential energy)
- किसी वस्तु अथवा निकाय में संग्रहित ऊर्जा जो उसकी किसी बल अथवा इसके विन्यास में स्थित होने के कारण होती है।
- स्थिरक्वाथी मिश्रण (azeotrope)
- द्रवों का मिश्रण जिसमें आसवन द्वारा रासायनिक संघटन को अपरिवर्तित रखा जाता है।
- स्पेक्ट्रममिति (spectrometry)
- द्रव्यमान स्पेक्ट्रममिति.
- स्पेक्ट्रमी रसायन (spectrochemistry)
- स्पेक्ट्रोस्कोपी (spectroscopy)
- विकिरण और पदार्थ का अध्ययन, जैसे ऍक्स किरण अवशोषण और उत्सर्जन वर्णक्रमापी।
- स्फुरांक अथवा प्रज्वलन-तापन (flash point)
- वह न्यूनतम ताप जिसपर वाष्पशील पदार्थों के उपर वाष्पें जलेंगे यदि उन्हें एक ज्वलनशील स्रोत दिया जाये। प्रज्वलन-ताप पर मुक्त ज्वाला का अनुप्रयोग निरंतर दहन के स्थान पर केवल क्षणिक "ज्वाला" निर्मित करती है, जिसके लिए व्यापक ताप अभी भी बहुत कम है। प्रज्वलन ताप और ज्वलनांक में भ्रमित नहीं होना चाहिए जो थोड़ा सा अधिक तापमान पर घटित होता है ना ही किंडलिंग बिन्दु के साथ भ्रमित हों जो भी थोड़ा सा अधिक है।
- स्वतंत्र चर (independent variable)
- स्वतःप्रज्वलन ताप (autoignition temperature)
- किंडलिंग बिन्दु (kindling point)
- स्वतःप्रज्वलन ताप देखें।
- हाइड्रेट (hydrate)
- कोई पदार्थ अथवा उसका घटक तत्व जिसमें जल शामिल हो या कोई यौगिक जो जल अथवा अन्य कणों को जोड़कर निर्मित किया जाता है।
- हाइड्रोजन (hydrogen)
- हाइड्रोजन आबंध (hydrogen bond)
- विद्युत् स्थैतिक अन्योन्यक्रिया का एक रूप जिसमें विद्युत् ऋणात्मक परमाणु और एक हाइड्रोजन परमाणु दूसरे विद्युत् ऋणात्मक परमाणु से आबंधित हो जाते हैं। हाइड्रोजन आबंध अद्वितीय होता है क्योंकि हाइड्रोजन परमाणुओं का छोटा आकार विद्युत आवेशों की समीप से अन्योन्यक्रिया को अनुमत करता है जिससे अंतराअणुक बल अथवा अंतःअणुक बल प्रभावी हो सकते हैं।
- हाइड्रोजनन (hydrogenation)
- हिमांक (freezing point)
- वह ताप जिसपर किसी पदार्थ की द्रव से ठोस अवस्था में परिवर्तन होता है। चूँकि हिमीकरण, गलन का विपरीत होता है एवं किसी पदार्थ का हिमांग उसके गलनांक के समान होता है लेकिन परम्परा के अनुसार केवल गलनांक को ही पदार्थ के अभिलाक्षणिक गुणधर्म के रूप में सन्दर्भित किया जाता है।
- हिमांक अवनमन (freezing-point depression)
- हिमीकरण (freezing)
- किसी पदार्थ का द्रव से ठोस में प्रावस्था संक्रमण।
- हुण्ड का नियम (Hund's rules)
- हेनरी का नियम (Henry's law)
- हैड्रॉन (hadron)
- बरिऑनों और मेसॉनों तरक के कणों सहित अपरमाणुक कण जो प्रबल अन्योन्य क्रिया में भाग लेते हैं।
- हैलोजन (halogen)
- आवर्त सारणी के समूह 17 के पाँच अधात्विक तत्वों में से कोई भी:: फ्लोरीन (F), क्लोरीन (Cl), ब्रोमीन (Br), आयोडिन (I), और ऐस्टाटीन (At)
- रसायन शास्त्र की रूपरेखा
- रसायन विज्ञान लेखों का सूचकांक
- रासायनिक तत्वों की सूची
- गणित के क्षेत्रों की शब्दावली
- जीव विज्ञान की शब्दावली
- इंजीनियरिंग की शब्दावली
- भौतिकी की शब्दावली
- ↑ अ आ इ ई उ ऊ ए ऐ ओ औ क ख ग घ ङ च छ ज झ डैन्टिथ, जॉन, संपा॰ (2004). A Dictionary of Chemistry [रसायनशास्त्र का शब्दकोश] (5th संस्करण). ऑक्सफोर्ड: ऑक्सफोर्ड यूनिवर्सिटी प्रेस. आई॰ऍस॰बी॰ऍन॰ 0-19-860918-3.
- ↑ सोलोमन, थीयोडोरस (2001). "The definition and unit of ionic strength" [आयनी सामर्थ्य की इकाई और परिभाषा]. जर्नल ऑफ़ केमिकल एडुकेशन. 78 (12): 1691. डीओआइ:10.1021/ed078p1691. बिबकोड:2001JChEd..78.1691S.
- ↑ अ आ इ Dictionary of Chemistry [रसायन विज्ञान का शब्दकोश] (2nd संस्करण). न्यूयॉर्क: मैकग्रॉ-हिल. 2003. आई॰ऍस॰बी॰ऍन॰ 0-07-141046-5.
- ↑ Carbonic Chemistory [कार्बनिक रसायन] (तीसरा संस्करण) मेरी एन्नी फॉक्स, जेम्स के॰ व्हिटसेल जोन्स & बर्टलेट पब्लिशर्स (2004) ISBN 0763721972
- ↑ IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). Online corrected version: (2006–) "Chirality".
- ↑ अमेरिकन केमिकल सोसाइटी. "CAS Registry and CASRNs" [कैस पंजीकरण एवं सीएएसआरएन] (अंग्रेज़ी में). मूल से 25 जुलाई 2008 को पुरालेखित.
- ↑ आईयूपीएसी, Compendium of Chemical Terminology, दूसरा संस्करण ("गोल्ड बुक"). एडी मैकनौट और विल्किन्सन द्वारा संकलित, ब्लैकवेल साइंटिफिक पब्लिकेशन्स, ऑक्सफोर्ड (1997); एसजे चॉक द्वारा निर्मित ऑनलाइन संस्करण (2019-) ISBN 0-9678550-9-8. https://doi.org/10.1351/goldbook.
- ↑ जॉन पी॰ रैफ्फर्टी, संस्करण (2011): Minerals (खनिज); पृष्ठ 1; Geology: Landforms, minerals, and Rocks [भूमिसुधार, खनिज और चट्टान] की शृंखला में रोसेन पब्लिशिंग समूह; ISBN 978-1615304899
- ↑ स्टीवन ए॰, त्रिसे; पीटर आर॰, पुजादो; डेविड एसजे, जोन्स (2015). Handbook of Petroleum Processing [पेट्रोलियम प्रसंस्करण की हैंडबुक] (अंग्रेज़ी में) (2 संस्करण). स्प्रिंगर. पृ॰ 1736. आई॰ऍस॰बी॰ऍन॰ 978-3-319-14528-0.


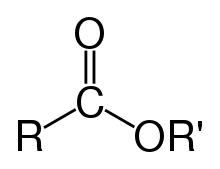
क-वर्ग से आरम्भ होने वाले[संपादित करें]

च-वर्ग से आरम्भ होने वाले[संपादित करें]
ट-वर्ग से आरम्भ होने वाले[संपादित करें]
त-वर्ग से आरम्भ होने वाले[संपादित करें]
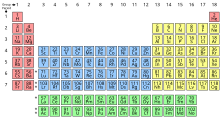
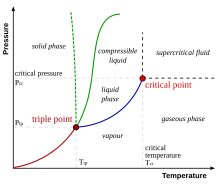

प-वर्ग से आरम्भ होने वाले[संपादित करें]



य-व से आरम्भ होने वाले[संपादित करें]

श-ह से आरम्भ होने वाले[संपादित करें]










