प्रोटिओसोमस


प्रोटिओसोमस सभी यूकेरियोट्स और आर्चिया और कुछ बैक्टीरिया में प्रोटीन कॉम्प्लेक्स हैं। यूकेरियोट्स में, प्रोटिओसोमस न्यूक्लियस और साइटोप्लाज्म में स्थित हैं। [१] प्रोटिओसोम का मुख्य कार्य प्रोटीलाइज़िस द्वारा अनावश्यक या क्षतिग्रस्त प्रोटीन को अवक्रमित करना है, जो पेप्टाइड बांड टूटने वाली एक रासायनिक प्रतिक्रिया है। ऐसी प्रतिक्रियाओं में मदद करने वाले एंजाइमों को प्रोटीज़ कहा जाता है। प्रोटिओसोमस एक प्रमुख तंत्र का हिस्सा हैं जिसके द्वारा कोशिकाओं को विशेष प्रोटीनों की एकाग्रता को विनियमित करने और मिसफॉल्टेड प्रोटीन को अवक्रमित करता है। अवक्रमिता की प्रक्रिया में लगभग सात से आठ अमीनो एसिड की पेप्टाइड्स पैदा होती है, जो बाद में कम अमीनो एसिड अनुक्रमों में अवक्रमित किया जा सकता है और नए प्रोटीन को संश्लेषण में इस्तेमाल किया जा सकता है। [२] युबिक्यूटिन नामक एक छोटी प्रोटीन, प्रोटीन को गिरावट के लिए टैग करता है। टैगिंग प्रतिक्रिया युबिक्यूटिन लाईगेसिस नामक एंजाइमों द्वारा उत्प्रेरित होती है। एक बार प्रोटीन को एक युबिक्यूटिन अणु के साथ टैग किया जाना, अतिरिक्त युबिक्यूटिन अणुओं को संलग्न करने के लिए अन्य लाईगेसिस के लिए एक संकेत है। नतीजा एक पॉलीब्यूविटीन श्रृंखला है जो प्रोटीसॉम द्वारा बाध्य है, जो टैग प्रोटीन को अवक्रमित करने मैं सक्ष्म है। [२]
खोज[संपादित करें]
संरचना और संगठन[संपादित करें]
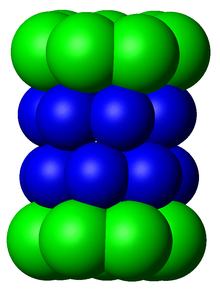
२० एस कोर कण[संपादित करें]
१९ ऐस नियामक कण[संपादित करें]
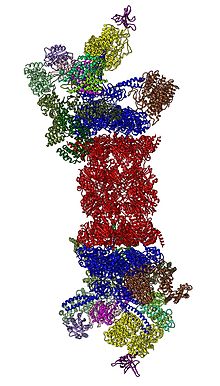
१९ ऐस का गठनात्मक परिवर्तन [संपादित करें]
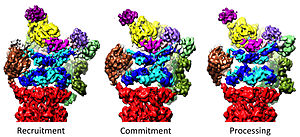
१९ एस द्वारा २० एस का विनियमन[संपादित करें]
11S नियामक कण[संपादित करें]
असेंबली[संपादित करें]
प्रोटीन की गिरावट की प्रक्रिया[संपादित करें]
युबिक्यूटनेशन और लक्ष्यीकरण[संपादित करें]
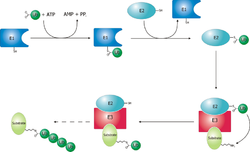
खोलना और स्थानान्तरण[संपादित करें]
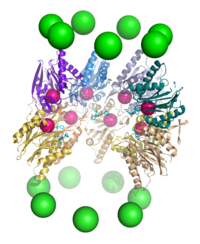
प्रोटियोलिसिस[संपादित करें]
यूबिक्वीटिन-स्वतंत्र गिरावट[संपादित करें]
विकास[संपादित करें]

कोशिका चक्र नियंत्रण[संपादित करें]
पौधे की वृद्धि का नियमन[संपादित करें]
एपोपटोसिस[संपादित करें]
सेलुलर तनाव की प्रतिक्रिया[संपादित करें]
प्रतिरक्षा प्रणाली में भूमिका[संपादित करें]
प्रोटिआसोम के अवरोधक[संपादित करें]
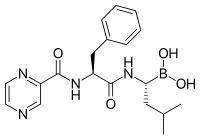
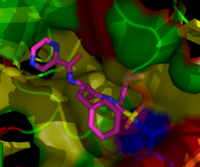
नैदानिक महत्व[संपादित करें]
इन्हें भी देखें[संपादित करें]
सन्दर्भ[संपादित करें]
- ↑ (वीर गडरिया) पाल बघेल धनगर
